作者简介:杨 建,1979年生,男,辽宁省北镇市人,高级工程师,研究方向为催化化学、工业催化、催化材料和化工工艺。
丁烯氧化脱氢是工业生产丁二烯常用的工艺,其中,铁系催化剂是丁烯氧化脱氢工业使用的主流催化剂,为满足清洁生产的需要,了解催化剂制备过程中产生的NOx及废水等排放物的组成尤为重要。对铁系催化剂生产过程中前驱体制备步骤的气体生成及组成进行研究,同时对沉淀洗涤步骤产生的废液成分进行检测。通过XRD、TG-DSC、ICP和TPC等技术对催化剂性质及制备排放物进行分析,考察制备条件对催化剂结构和性能的影响及废物排放的变化规律。结果表明,在前驱体制备溶铁过程中,空气气氛下提高硝酸浓度可有效抑制氢气的产生;不同焙烧温度阶段,生成NOx种类有较大差别;排放废水中含有较多的Zn离子。焙烧条件试验表明,最佳焙烧温度为(650~700) ℃,焙烧时间低于9 h。
Oxidative dehydrogenation of butene is commonly used in industrial process of butadiene production.Fe-based catalyst is one of the main commercial catalysts for oxidative dehydrogenation of butene.In order to meet the need of clean production,it is particularly important to understand the composition of the generated NOx,wastewater and other emissions during the catalyst preparation process.In this paper, the production and composition of gas during the process of Fe-based catalyst preparation were studied,and the composition of the waste liquid during the precipitation and washing processes was analyzed.The catalyst properties and emissions were characterized by XRD,TG-DSC,ICP and TPC,etc.The influence of preparation conditions on the structure and properties of the catalyst and the change law of waste emission were investigated.The results showed that improvement of the concentration of nitric acid could effectively inhibit the generation of hydrogen under air atmosphere during the process of dissolving iron for the precursor preparation.There were more different NOx species under different calcination temperatures.The discharge wastewater contained more zinc ions.The experimental results of calcination condition indicated that the optimal calcination temperature was (650-700) ℃ and calcination time was less than 9 h.
丁二烯主要用于合成顺丁橡胶、丁苯橡胶和ABS树脂。近年来, 由于汽车等行业的快速发展, 顺丁橡胶和丁苯橡胶产能增大, 导致丁二烯需求增长迅猛[1]。丁二烯主要来自于乙烯裂解的副产碳四馏分, 随着低碳烯烃新路线不断推出, 如页岩气轻烃生产乙烯、以煤和天然气为原料的MTO/MTP技术等, 丁二烯生产量与新建乙烯能力不再具有关联性。丁二烯供不应求的局面将持续存在, 20世纪60年代工业化脱氢法生产丁二烯工艺成为丁二烯工业重要的补充路线, 与丁烷催化脱氢制丁二烯工艺相比, 丁烯氧化脱氢工艺原料转化率和产品丁二烯选择性均较高, 反应温度约低100 ℃, 装置投资成本低[2]。
丁烯氧化脱氢催化剂的研究涉及多种复合氧化物体系, 如Mo-Bi体系、V/Al2O3以及铁酸盐体系等[3, 4, 5, 6], 我国自主研发的以炼油厂LPG重碳生产丁二烯技术在1998年以前已成熟, 主要有流化床工艺和固定床工艺, 催化剂均采用铁系尖晶石结构[7, 8, 9]。铁系催化剂具有丁烯转化率高和选择性好的优势, 在工业化技术中具有优异的技术指标, 我国未来几年建设的丁烯氧化脱氢装置将全部采用铁系催化剂。铁系催化剂制备通常采用共沉淀法, 在制备过程中, 由于反复进行过滤-水洗, 产生大量氨氮废水, 前驱体焙烧活化步骤短时间产生少量氮氧化合物(NOx)。为了达到绿色清洁生产, 必须进行环保处理, 使废气和废水达到排放要求; 另一方面, 在实际工业生产中, 铁源一般以稀硝酸溶解金属铁产生[10], 若催化剂为铁酸锌, 则可能用酸溶解金属锌获得锌源, 此过程中NOx生成对整个绿色生产也将产生较大影响。以往的制备过程研究[11, 12, 13]报道针对催化剂制备方法的改进较多 , 忽视了绿色制备过程和废气处理工艺的考察[14]。
本文以铁酸锌尖晶石结构的铁系催化剂为代表, 对制备过程可能产生的废气、废液中的氨氮进行研究。
催化剂制备所用试剂包括硝酸铁(工业级, 纯度> 98.5%)、硝酸锌(分析纯)、硝酸钙(分析纯)和氨水(分析纯)等, 溶铁和溶锌过程采用锌粒/锌粉(分析纯), 铁钉(直径2.5 mm, 切为5 mm小段)以及质量分数为10%和20%的稀硝酸。
催化剂制备采用共沉淀法, 九水硝酸铁、六水硝酸锌及氯化钙按一定配比溶于蒸馏水中, 搅拌下滴加质量分数10%的氨水溶液至pH=8~9, 在60 ℃水溶液中老化1 h, 室温静置1 h, 抽滤、洗涤沉淀至滤液为中性。滤饼在120 ℃烘干过夜, 一定温度焙烧活化。催化剂经破碎筛分为(20~60)目颗粒, 用于反应性能评价。
丁烯氧化脱氢反应评价在固定床反应装置上进行, (20~60)目催化剂装填量为10 mL, 采用石英反应器, 尾气经过冷凝后, 用气相色谱分析组成, 以碳归一化法计算反应结果。以水蒸汽为稀释气, 丁烯空速400 mL· (g· h)-1, V(O2):V(C4H8)=0.66:1, V(H2O):V(C4H8)=(12~13):1, 反应温度(300~340) ℃。实验所用丁烯原料为工业品, 丁烯总体积分数约94.5%, 杂质主要为丁烷和丁二烯, 体积分数分别为4%和0.5%。
原料及反应后气体分析采用两根色谱柱和两个检测器, TDX-01填充柱(ϕ 3 mm× 2 m)分析空气、CO、CH4和CO2, 热导检测器, 自制的轻烃柱(ϕ 3 mm× 2 m)分析C1~C4烃, 甲烷作为内标物, 氢火焰检测器。
催化剂物相结构分析在X'Pert Pro多功能衍射仪上进行, CuKα , λ =0.154 184 nm, 工作电压40 kV, 工作电流40 mA, 扫描范围10° ~80° , 步幅0.02° , 扫描速率4° · min-1。
热重-差示扫描量热表征在德国NETZSCH STA NETZSCH 449F3同步热分析仪上进行, 样品在空气气氛从室温以10 ℃· min-1升温至800 ℃。
程序升温分解在AMI-100微反表征装置上进行, 将200 mg于120 ℃烘干的催化剂装入U形石英管中, 从室温以20 ℃· min-1升至800 ℃, 尾气由AMETEK Dycor MASS SPECTROMETER四极质谱检测。
在圆底烧瓶中, 加入制成片状的铁钉1 g或直径5 mm、厚(1~2) mm的锌粒1 g, 在室温或加热条件下, 以不同浓度的硝酸溶液或与硝酸铁的混合溶液进行溶解, 硝酸与金属物质的量比为4, 直至金属完全溶解。氮气气氛溶解时, 首先用氮气置换反应器中的空气, 至无氧, 在室温下完全溶解铁或锌后, 取气体进行检测。空气气氛下溶解时, 直接用硝酸在50 ℃溶解铁至完全, 期间定量补充空气, 保证溶解过程在充足氧的气氛中进行, 然后冷却至室温后, 取气体进行质谱检测。
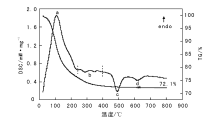
经共沉淀法制备的催化剂, 虽然大多数硝酸盐已被洗去, 但仍然残留少量以硝酸铵形式存在的和未沉淀完全的硝酸盐, 这些硝酸盐在焙烧活化过程中将产生包括NOx在内的一些气体, 因此, 了解胶体在热处理过程中的变化对绿色制备催化剂非常重要。将沉淀和洗涤后的胶体进行TG-DSC分析, 结果如图1所示。由图1可以看出, 催化剂在温度低于450 ℃基本完成失重, 但从热量变化看, 室温~250 ℃有非常大的吸热峰(a), (250~400) ℃有一组小的放热峰(b), (450~550) ℃(c)和(580~680) ℃(d)分别有两个明显的放热峰。
根据沉淀成胶过程和焙烧活化过程中的物理和化学变化, 催化剂DSC测试的吸放热峰见表1。
| 表 1 催化剂DSC测试的吸放热峰 Table 1 Endothermic and exothermic peaks of the catalyst at different temperatures by DSC analysis |
沉淀形成的胶体主要是Fe(OH)3和Zn(OH)2, 少量的Ca(OH)2, Fe(OH)3室温下即可逐渐失水, 至500 ℃完全脱水为Fe2O3。Zn(OH)2的分解温度为125 ℃, 因此, 低于250 ℃的失重和吸热峰既有胶体中的H2O, 也包含两种氢氧化物分解脱出的H2O。沉淀过程生成的NH4NO3, 分解过程比较复杂:
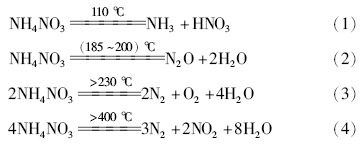
(250~380) ℃出现的放热峰和失重, 包含了Fe(OH)3的脱水和NH4NO3的分解; 高于450 ℃, 基本上没有失重, 表明物质的分解过程基本结束, 出现的两个放热峰可能是Fe2O3和ZnO生成ZnFe2O4以及尖晶石结构相变。
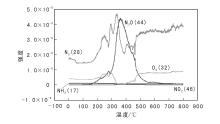
为进一步明确催化剂在焙烧过程中产生的气体组分, 采用AMI-100微反动力学装置进行程序升温分解试验(TPC), 并用质谱对质量数分别为O2(32)、N2(28)、NH3(17)、N2O(44)、NO2(46)进行跟踪检测。120 ℃将催化剂烘干12 h后, 以10 ℃· min-1升温, 气体检测结果如图2所示。
由图2可见, 150 ℃开始有气体分解产物, 在(150~300) ℃, 出现O2、N2、N2O; 在(300~550) ℃出现N2、NO2、N2O; 在(550~600) ℃只有极少量的N2O, 整个过程中未检测到NH3。
催化剂程序升温分解产物如表2所示。由表2可以看出, 500 ℃时绝大部分NOx已出完。
| 表 2 催化剂程序升温分解产物 Table 2 Products analysis by TPC-MS |
沉淀成胶后, 溶液中存在的金属离子和形成的溶于水的盐(NH4NO3)将在过滤洗涤过程进入各级滤液, 对不同洗涤次数产生的滤液成分进行分析, 以ICP分析滤液中的Fe和Zn离子, 结果见表3。由表3可见, 沉淀成胶后, Fe离子基本完全沉淀, 而Zn离子未完全沉淀, 根据原料浓度计算, Zn离子沉淀率约为85%。随着洗涤次数增加, Zn离子浓度急剧降低, 洗涤3次后, 可降至3 μ g· mL-1以下。
| 表 3 各级滤液中的Fe离子和Zn离子浓度 Table 3 Concentration of Fe and Zn ions in different filtrates |
采用离子色谱分析技术测试滤液中Ca2+、N
| 表 4 各级滤液中的阴阳离子浓度及COD值 Table 4 Various ions concentrations and COD values in different filtrates |
2.3.1 氮气气氛溶铁和溶锌的研究
工业中常用的以硝酸溶解铁或锌来获得铁系催化剂前驱物, 在溶解过程中, 如果发生置换反应, 将生成H2, 对安全生产带来影响, 有必要对溶解过程的废气进行检测。分别以质量分数为10%和20%的HNO3溶液在室温进行铁和锌的溶解, 为模拟两种金属混合溶解后期的过程, 氮气气氛和50 ℃条件下, 以质量分数为10%的HNO3与质量分数为20%的Fe(NO3)3溶液分别溶解铁和锌至完全溶解, 不同浓度硝酸溶液溶铁、溶锌产氢情况如表5所示。
| 表 5 氮气气氛硝酸溶液溶铁、溶锌产氢情况 Table 5 Hydrogen production by dissolving Fe and Zn in nitric acid solution under N2 atmosphere |
由表5可以看出, 在任何情况下, 用不同浓度硝酸溶解金属Zn时, 均无氢气产生, 而溶解铁时, 硝酸浓度不同, 产生氢气的量不同, 除了少量氢气, 气体中的主要组分为NO。
2.3.2 空气气氛溶铁的研究
因在氮气气氛溶锌时未检测到氢气生成, 故在空气气氛下仅考虑溶铁过程。室温溶铁比较缓慢, 在原料配比与氮气气氛相同条件下, 在50 ℃和80 ℃进行两种硝酸浓度的溶铁反应, 结果见表6。
| 表 6 空气气氛硝酸溶液溶铁产氢情况 Table 6 Hydrogen production by dissolving Fe in nitric acid solution under air atmosphere |
由表6可以看出, 空气气氛用质量分数为10%的硝酸溶解铁时, 有氢气生成, 生成量与氮气气氛结果相差不大。采用质量分数为20%硝酸溶解时, 温度对溶解产氢有一定影响, 50 ℃, 生成的氢气几乎检测不到, 80 ℃没有氢气产生, 溶解气体中以NO为主要组分, 有极少量的NO2, 表明在空气介质的氧化气氛中, 低浓度硝酸溶解铁时不能消除生成的氢气, 高浓度和一定温度下, 可以避免产生氢气。在实际溶铁过程中, 用浓硝酸溶铁, 气体除水汽外以NO为主, 可以考虑NO氧化为NO2, 然后循环的工艺路线。
2.4.1 焙烧温度
丁烯氧化脱氢铁系催化剂的活性相通常认为是铁酸盐尖晶石结构[15], 根据TG-DSC表征结果, (580~680) ℃出现相变, 焙烧温度可能对催化剂结构和活性影响较大。不同焙烧温度制备的催化剂的XRD图如图3所示。各衍射峰的信息列于表7。由图3可见, 600 ℃焙烧后, ZnFe2O4尖晶石结构已形成, 同时存在α -Fe2O3物相, 随着焙烧温度升高, α -Fe2O3峰强度减弱, 温度升至750 ℃时, ZnFe2O4与α -Fe2O3峰强度之比由600 ℃时的6.4增至11.1, ZnFe2O4晶体颗粒度亦有所增加, 由30.6 nm提高至39.2 nm。根据以往研究结果, 催化剂中α -Fe2O3量是影响催化剂活性的一个重要指标, 控制焙烧温度和焙烧时间, 实质上是控制α -Fe2O3与ZnFe2O4的适宜比例。
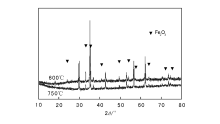 | 图 3 不同焙烧温度制备的催化剂的XRD图Figure 3 XRD patterns of the catalysts prepared at different calcination temperatures |
| 表 7 催化剂的XRD衍射峰信息 Table 7 XRD diffraction peak information of the catalysts |
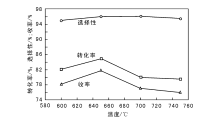
考察在焙烧时间10 h条件下, 焙烧温度对催化剂活性的影响, 结果如图4所示。
由图4可见, 随着焙烧温度升高, 催化剂活性呈先升后降的趋势。丁烯转化率在650 ℃达到最高, 丁二烯选择性变化幅度较小, 最高值出现在(650~700) ℃; 焙烧温度高于700 ℃, 活性显著下降, 焙烧温度不宜超过700 ℃。
2.4.2 焙烧时间
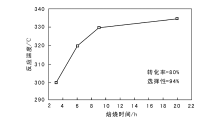
将焙烧温度控制在650 ℃, 焙烧时间对催化剂性能影响如图5所示。
由图5可以看出, 达到同样活性需要的反应温度随着焙烧时间延长而增加。焙烧时间从3 h延长至9 h, 反应温度急剧升高, 之后变得缓慢。表明焙烧时间越短, 达到同样活性的反应温度越低, 催化剂活性越好, 焙烧时间控制在低于9 h。
(1) 硝酸溶铁和溶锌试验表明, 硝酸溶解锌的过程中不生成氢气, 而无论是氮气或空气气氛, 质量分数为10%的稀硝酸溶解铁时将生成体积分数为2%的氢气, 同时有NO生成; 当硝酸浓度提高至20%, 氢气生成量显著降低, 空气介质中几乎检测不到。
(2) 催化剂焙烧过程中, 不同温度阶段, 废气组成不同, (150~600) ℃, 始终有N2O, 而NO2出现在(300~500) ℃。由于催化剂制备条件的限定, Fe可以完全沉淀, 但母液中仍然存在较大量的Zn离子, 需要在实际工业生产中加以回收利用。焙烧条件试验表明, 最佳焙烧温度为(650~700) ℃, 焙烧时间低于9 h。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|