作者简介:李曼弯,1988年生,女,云南省蒙自市人,硕士,研究方向为催化化学。
在[Bmim]PF6离子液体介质中微波辅助制备稀土元素Ce掺杂改性的TiO2光催化剂TiO2-Ce,以甲基橙溶液和苯酚溶液为模拟污染物,在紫外光照和微波辐射-紫外光照降解条件下考察TiO2-Ce催化剂的光催化活性。利用荧光技术以对苯二甲酸作为荧光探针检测TiO2-Ce催化剂表面产生的羟基自由基,并对光催化降解反应进行动力学分析,以了解光催化降解反应机理。结果表明,通过优化反应条件制得的TiO2-Ce催化剂具有较高光催化降解活性和热稳定性,在紫外光照和微波辐射-紫外光照条件下降解60 min后,甲基橙降解率分别为98.6%和99.3%,苯酚降解率分别为96.6%和97.2%。荧光光谱分析表明,TiO2-Ce在微波辐射-紫外光照条件下产生的羟基自由基比紫外光照多,因而微波辐射-紫外光照具有强化TiO2-Ce降解模拟污染物作用的效果。反应动力学数据表明,TiO2-Ce光催化降解甲基橙溶液反应呈一级反应动力学规律,其表观速率常数 k最大值为0.056 2 min-1。
Using room temperature ionic liquid [Bmim]PF6 as the reaction medium,cerium doped TiO2 photocatalyst TiO2-Ce was prepared by microwave drying method and sol-gel method.The activity of TiO2-Ce photocatalyst for photocatalytic degradation of methyl orange and phenol solutions as simulated pollutants was respectively investigated under ultraviolet irradiation(UV) and microwave irradiation with ultraviolet irradiation (MW-UV).With terephthalic acid as the fluorescence probe,the influence of ·OH on the surface of TiO2-Ce on its photocatalytic activity was investigated by the fluorescence technology.In order to understand the reaction mechanism,the photocatalytic degradation kinetics was experimentally determined.The results showed that TiO2-Ce catalysts prepared under the optimum condition had higher photocatalytic activity and heat stability.The degradation rates of methyl orange and phenol solution reached 98.6%,99.3%, 96.6%,and 97.2%,respectively,under the condition of UV and MW-UV irradiation for 60 min.The results of fluorescence spectra characterization indicated that the UV irradiation combining with MW technology could effectively improve the catalytic efficiency of TiO2-Ce catalyst due to more amount of hydroxyl radicals produced under MW-UV irradiation than that under UV irradiation.The reaction kinetics data showed that the photocatalytic degradation of methyl orange on TiO2-Ce catalyst fitted the first order kinetics model,and the maximum of apparent rate constant k was 0.056 2 min-1.
纳米TiO2催化剂在处理环境污染方面具有良好的应用前景, 但TiO2催化剂自身存在的缺陷使其应用范围受到限制。为提高TiO2催化剂的催化活性, 研究者对其进行了大量的掺杂改性, 其中, 稀土元素在改性TiO2催化剂方面因其独特的4d和5f电子组态, 具有许多特殊物化性能而备受关注, 4f电子还可以在f-f组态之间或f-d组态之间发生跃迁[1, 2, 3]。据文献[4, 5, 6]报道, 稀土元素掺入TiO2催化剂可以较好地抑制TiO2晶型转变和晶粒生长, 同时, 稀土离子因半径较大, 难以进入TiO2晶格, 主要附着于催化剂表面, 对有机污染物有较强的吸附作用, 可进一步提高TiO2催化剂的光催化反应效率。
稀土元素铈能够通过导带和价带进行氧化还原反应, 在CeO2和Ce2O3之间转换, 还能形成氧空位[1, 2, 3]。CeO2禁带宽度较小(能量为5.5 eV), 电子发生跃迁的能级较为容易, 对紫外线有较强吸收能力, 因此, 稀土元素铈的掺杂极有可能提高TiO2催化剂的光催化活性; 另外, 稀土离子Ce4+的4f和5d轨道均无电子, 可极化性强, 变形性大, 更易于使TiO2晶格畸变, 造成键长和键角发生变化, 分子极性增大, 晶面不对称性提高, 产生更多电子-空穴对, 导致TiO2催化剂的光催化活性进一步提高[4, 5, 6]。本课题组在微波助离子液体条件下, 制备了稀土元素钕和铈掺杂改性的TiO2光催化剂, 并利用微波辐射对模拟污染物甲基橙进行降解测试, 考察稀土元素掺杂制得TiO2光催化剂的活性[7, 8]。文献[8]报道了微波助离子液体条件下铈元素掺杂改性TiO2光催化剂的制备, 并分别在紫外光照和微波辐射-紫外光照条件下考察了催化剂对甲基橙的降解率。本文考察铈掺杂改性TiO2-Ce催化剂对苯酚的降解情况, 并利用荧光技术以对苯二甲酸为荧光探针, 检测TiO2-Ce催化剂表面产生的羟基自由基, 通过光催化降解反应动力学数据测试光催化反应降解机理。
硝酸铈铵、钛酸丁酯、1-甲基咪唑、溴代正丁烷和对苯二甲酸等均为分析纯。
XH-300UL电脑微波超声波紫外光组合催化合成仪, 北京祥鹄科技发展有限公司; XH-200A电脑微波固液相合成/萃取仪, 北京祥鹄科技发展有限公司; 美国康塔公司NOVE2000-e型表面分析仪; 日本日立高技术公司HITACHI(日立)F-4600日立荧光光谱仪。
离子液体制备、TiO2-Ce催化剂的制备及制备过程中离子液体用量、微波干燥功率和时间、焙烧温度和时间等条件的确定、催化剂结构测试与表征方法和催化剂降解甲基橙溶液的光催化活性测试等见文献[7, 8, 9, 10, 11]。
催化剂降解苯酚溶液的光催化活性测试:称取50 mg的TiO2-Ce光催化剂投入盛有10 mg· L-1苯酚溶液50 mL的烧杯中, 置于催化合成仪进行降解反应。实验结束后, 取适量降解液放入离心机, 以4 000 r· min-1离心20 min后, 吸取上层清液测定溶液吸光度。
苯酚溶液吸光度测定:采用4-氨基安替比林分光光度法, 酚类化合物与pH=10± 0.2的显色剂作用后生成橙红色安替比林染料, 选取K2S2O8与4-氨基安替比林为显色剂, NH4Cl-NH3为缓冲溶液。量取0.5 mL的NH4Cl-NH3缓冲溶液于盛有10 mL上层清液的比色管中摇匀, 加入30 g· L-1的K2S2O8溶液1 mL, 20 g· L-1的4-氨基安替比林溶液1 mL, 充分混合, 静置10 min, 510 nm处测定吸光度A, 计算苯酚降解率。
空白实验表明, 无TiO2-Ce催化剂只有紫外光照时, 苯酚溶液浓度不变; 有TiO2-Ce催化剂无紫外光照时, 室温放置相同时间, 苯酚溶液浓度无明显变化。
TiO2-Ce催化过程中以对苯二甲酸作为荧光探针, 可测定生成羟基自由基, 因其可与· OH快速反应生成具有特征荧光的2-羟基对苯二甲酸, 因此, 可通过测定荧光光谱强度确定光催化剂与水界面生成· OH自由基的量[12, 13]。分别测定紫外光照(UV)(P=250 W)、微波辐射(MW)(P=500 W)和微波辐射-紫外光照(MW-UV)条件下产生的羟基自由基, 室温25 ℃, 时间分别设为0、5 min、10 min、15 min和20 min。
取50 mg的TiO2-Ce光催化剂于盛有25 mL适量浓度的对苯二甲酸溶液与氢氧化钠溶液混合液中, 分别测定UV、MW和MW-UV条件下· OH自由基。实验结束后, 离心混合物并取上层清液, 采用HitachiF-4600型荧光光谱仪分别测定邻羟基对苯二甲酸产生的荧光光谱强度(激发波长为312 nm)变化。
甲基橙是一种化学性质稳定的含氮染料, 可通过光催化降解甲基橙溶液检测不同样品的光催化活性。选取TiO2-Ce催化剂50 mg, 对10 g· L-1甲基橙溶液50 mL进行降解, 降解前将催化剂与甲基橙溶液混合体置于黑暗中避光搅拌, 使二者达到吸附平衡。待光催化降解完成后离心取上层清液, 用722N型可见分光光度计测定不同时间光照后甲基橙溶液的吸光度, 计算甲基橙降解率。
根据一级反应动力学方程:ln
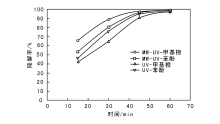
取最佳条件下制得的TiO2-Ce催化剂, 在UV和MW-UV降解条件下, 考察对模拟污染物的降解率, 结果如图1所示。由图1可以看出, 模拟污染物降解率随着降解时间的延长而逐渐升高, 降解时间60 min时, UV和MW-UV照射条件下甲基橙降解率分别为98.6%和99.3%, 苯酚降解率分别为96.6%和97.2%; 降解时间超过70 min, 两种模拟污染物成为无色透明溶液, 表明模拟污染物几乎达到完全降解, 此时模拟污染物降解率约100%。在整个降解反应过程中, TiO2-Ce催化剂对模拟污染物降解率始终为MW-UV条件下高于UV条件, 表明MW-UV照射具有强化TiO2-Ce降解模拟污染物的作用。298 K恒温条件下, 仅用微波辐射降解模拟污染物时只能生成中间产物, 模拟污染物降解率极低, 表明只有极少部分模拟污染物发生降解; 但在UV照射条件下, 使用微波辐射能够显著提高模拟污染物降解率, 表明MW-UV照射下的降解率比UV光照或MW辐射高。微波辐射能够增加催化剂催化活性, 可能原因是在微波场的作用下, TiO2-Ce催化剂表面能够产生更多的· OH自由基, 有利于降解和矿化模拟污染物, 同时能够抑制光生电子-空穴复合, 提高光催化降解活性。表明微波辐射加热除有利于掺杂型TiO2-Ce催化剂的合成外, 还具有强化掺杂型TiO2-Ce催化剂光催化降解模拟污染物的作用。
TiO2-Ce催化剂在UV和MW-UV条件下的荧光光谱图如图2所示。由图2可以看出, 在波长约429 nm处, 荧光强度随光照时间延长而增强, 但是无TiO2-Ce光催化剂或无紫外光照射时均没有荧光信号, 表明荧光来自于由光催化降解反应生成的· OH与对苯二甲酸反应生成的邻羟基对苯二甲酸。Ishibashi K等[13]在使用荧光法测定TiO2表面氧化物种时指出, H· 和HO2· 等自由基诱导产生荧光影响不及· OH起的作用。荧光强度逐渐增强进一步表明, 光催化降解体系中生成的· OH有所增加, 而这些· OH活性基团参与了光催化反应过程, 使模拟污染物发生降解和矿化。从图2还可见, UV和MW-UV条件下· OH活性基团生成量随着降解时间延长而增加, 降解时间相同时, MW-UV条件下产生的· OH活性基团更多, 表明微波辐照可促进光催化体系生成更多· OH活性基团, 而催化剂表面生成更多· OH活性基团将有利于光催化活性的提高, 进一步表明微波辐照具有强化TiO2-Ce催化剂降解模拟污染物的作用。
取最佳条件下制得的TiO2-Ce催化剂, 在UV光照模拟污染物60 min后, 将降解液静置24 h除去上层清液, 用二次蒸馏水清洗催化剂并进行烘干, 100 ℃真空干燥30 min, 取出后进行重复实验, 测试催化剂稳定性, 催化剂重复使用5次, 稳定性测试结果如表1所示。由表1可以看出, TiO2-Ce催化剂重复使用5次后, 模拟污染物甲基橙降解率为98.8%, 苯酚降解率为97.0%, 表明微波辅助离子液体介质中制得的掺杂型TiO2-Ce催化剂具有较好的稳定性。
| 表 1 TiO2-Ce催化剂降解甲基橙和苯酚溶液稳定性测试结果 Table 1 Stability testing results of TiO2-Ce catalyst for degradation of methyl orange and phenol |
TiO2-Ce催化剂对甲基橙溶液光催化降解反应, 假设遵从一级反应动力学反应, 由于甲基橙浓度较小, 则表征速率常数ka可忽略不计, 依据反应动力学表达式:
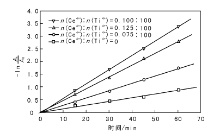 | 图 3 不同Ce4+与Ti4+物质的量比的TiO2-Ce催化剂降解甲基橙溶液的光催化活性Figure 3 Photocatalytic activity of TiO2-Ce catalysts with different different molar ratios of Ce4+ to Ti4+ for methyl orange degradation |
| 表 2 不同Ce4+与Ti4+物质的量比的TiO2-Ce催化剂光催化降解甲基橙溶液动力学参数 Table 2 Kinetics parameters of photocatalytic degradation of methyl orange over TiO2-Ce catalysts with different molar ratios of Ce4+ to Ti4+ |
由图3和表2可以看出, 铈掺杂TiO2-Ce催化剂光催化降解活性明显高于纯TiO2光催化剂, 当n(Ce4+):n(Ti4+)=0.100:100时, TiO2-Ce催化剂光催化活性较高, 其表观速率常数k为最大值0.056 2 min-1; 随着k值增加, 催化剂光催化活性增强, 表明铈掺杂显著提高TiO2催化剂的光催化活性, n(Ce4+):n(Ti4+)=0.100:100为最佳铈掺杂量。原因可能是由于铈掺杂量过多时, Ce4+在催化剂表面堆积过多形成电子和空穴复合中心, 不利于载流子向TiO2-Ce催化剂界面传递, 使催化活性降低。
(1) 微波辅助离子液体介质中最佳条件下制得的TiO2-Ce催化剂具有较高的光催化降解活性和热稳定性, 在UV和MW-UV条件下降解60 min后, 甲基橙降解率分别为98.6%和99.3%, 苯酚降解率分别为96.6%和97.2%。
(2) 羟基自由基检测的荧光光谱结果表明, 微波辐射一定程度上促使TiO2-Ce催化剂表面生成更多的· OH, · OH活性基团有利于催化剂光催化活性的提高, 因而微波辐射具有强化TiO2-Ce降解模拟污染物的作用效果。
(3) 光催化反应动力学数据分析表明, TiO2-Ce催化剂对甲基橙溶液的光催化降解反应呈一级反应动力学规律, 当n(Ce4+):n(Ti4+)=0.100:100时, 其表观速率常数k具有最大值0.056 2 min-1, 催化剂表现出较高的光催化降解活性。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|