作者简介:刘树森,1982年生,男,博士,讲师,研究方向为多相催化和环境催化。
CO2是造成温室效应的主要气体,作为碳基能源使用的末端形态,CO2也是种重要的基础碳源。因此,将CO2转化为能源产品可以快速实现碳的循环,对环境与能源领域意义重大。介绍了CO2的排放、回收以及资源化利用现状,从催化剂体系、反应机理、合成工艺以及工业化现状等方面系统地介绍了CO2甲烷化的发展。针对H2供给对CO2甲烷化应用的限制,分析了电解水制氢再与CO2进行甲烷化反应的电制气(PtG)技术的发展现状、工艺路线及其经济性,讨论了该技术在我国应用的可行性。提出随着CO2捕集与新能源相关技术的发展,PtG技术会更加成熟,将有望成为未来CO2资源化利用的重要形式。
Carbon dioxide (CO2) is not only the main greenhouse gas,but one of the most important carbon source in the world as the used form of carbon-based energy.Therefore,as an anthropogenic chemical carbon cycle,converting CO2 into energy products will be of great significance for environment and energy.CO2 emission,recovery and resource utilization were reviewed,as well as development of CO2 methanation in terms of catalyst system, reaction mechanisms,synthesis process,industrial status.In addition,the development,route and economy of the Power-to-Gas(PtG) technology were introduced and analyzed considering the restrictions of H2 supply in the industrial application of CO2 methanation.And the PtG technology will become more mature with the development of CO2 capture and CO2 methanation technics.Thus,it is proposed that PtG technology will become as a very important form of future CO2 utilization.
CO2是大气中主要温室气体, 而化石燃料的燃烧则是CO2排放的主要来源[1]。以煤、石油和天然气为主的不可再生能源消费量占2016年全球能源消费的85.52%, 产生的CO2排放量高达33 432 Mt[2]。全球人年均CO2排放量约为4.9 t, 2010年空气中的CO2浓度已经达到390× 10-6。根据联合国政府间气候变化专门委员会预测, 到2100年大气中CO2含量将达到570× 10-6[3]。CO2浓度升高促进了全球气候变暖, 也诱发了一系列生态环境问题, 如酸雨等极端天气状况, 动物迁徙以及粮食短缺等[4, 5]。因此, CO2减排及其资源化利用越来越受到关注。除对环境影响较大, CO2作为碳基能源使用的末端形式, 将其转化为能源产品, 可以快速实现碳循环, 对能源领域同样意义重大。本文简述CO2的回收与利用方式, 着重总结包括催化剂、反应机理以及工艺等CO2甲烷化研究现状, 并对其发展前景进行展望。
目前, 对CO2进行回收比较成熟的方法有吸收法, 吸附分离法和膜分离法等[6, 7]。
1.1.1 吸收法
吸收法可分为物理吸收法和化学吸收法, 物理吸收法是将CO2溶解在吸收液中, 原料气中的CO2溶解度较大, 而其他气体溶解度较小, 由溶解度的差异除去CO2。该方法核心在于吸附剂的选择, 所选的吸收剂必须对 CO2溶解度大、沸点高、选择性好、无毒性、无腐蚀性, 并且性能较稳定。典型的吸收剂有环丁砜, 聚乙二醇二甲醚和碳酸丙烯酯等。化学吸收法是利用CO2与化学溶剂反应, 再通过加热方式破坏产物分解成 CO2和溶剂, 使溶剂得到循环使用, CO2连续排出, 从而达到CO2与其他混合气分离的目的。目前, 应用最广泛的CO2吸收剂是有机胺溶液, 工业上主要是乙醇胺。
1.1.2 吸附分离法
吸附分离法是利用吸附剂对混合气中的CO2选择性可逆吸附。通过对温度与压力的调控, 在低温、高压条件下吸附CO2, 并在升温、降压后解吸CO2, 通过周期性的温度和压力变化, 实现CO2与其他气体的分离。常用的吸附剂有活性炭、分子筛、活性氧化铝和硅胶等。
1.1.3 膜分离法
膜分离法是目前发展较为迅速的一种节能型分离技术, 利用薄膜对不同气体的渗透率使混合气中的CO2通过薄膜从而得以分离。气体分离膜主要分为多孔结构的无机膜和无孔结构的有机膜[8]。
1.1.4 CCS技术
除几种主要的捕集技术外, 由于CO2的释放量远大于其可被利用的量, 因此也有研究团队在开发系统的CO2捕集、运输和封存一体化技术:Carbon Dioxide Capture and Storage(CCS)技术。该技术可将原料转化、工厂和电力行业中因使用化石燃料而产生的CO2减排70%~82%[9, 10]。CCS关键环节是碳的捕集, 工业上通过燃烧前捕集、燃烧后捕集以及富氧燃烧[11]等方法对CO2进行捕获。CO2的封存主要有地质封存技术、CO2-EOR(CO2 Enhanced Oil Recovery)技术、CO2-ECBM(CO2 Enhanced Coal Bed Methane)技术以及海洋封存技术等[12]。CCS技术作为集成化的CO2处理技术, 其发展取决于独立CO2捕集、封存以及应用技术的发展。随着技术的发展, CCS将有可能衍生出更多的组合, 有较好的发展前景。
目前, 全球对CO2的有效利用十分重视, 已有多种应用技术被相继开发出, 从利用方式上可分为物理应用与化学应用。相对成熟的CO2直接应用途径有添加到饮料中制碳酸饮料; 作为制冷剂用于食品冷藏和制冷; 作为保护气体用于焊接; 替代氟利昂用作烟丝膨胀剂; 注入油藏中提高原油采收率等[13, 14]。同时, CO2也是重要的化学原料, 己在应用的将CO2作为原料生产出的有机产品有尿素(用于氮肥和塑料)、水杨酸(药物原料)及聚碳酸酯(用于塑料)[15], 作为碳源可经过化学反应合成一系列化学产品, 如图1所示[16]。
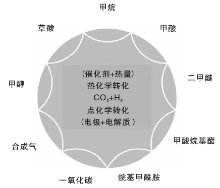 | 图1 CO2加氢过程所生产的化学产品[16]Figure 1 Products from CO2 hydrogenation via thermochemical and electrochemical routes[16] |
相比物理应用, 化学转化应用技术所获得的产品附加值更高, 目前该类应用约占CO2利用量的40%[13, 14]。长远来看, CO2转化应用技术途径多、方向广, 受产品需求的局限小, 作为CO2资源化利用的发展方向, 前景广阔。
1.2.1 加氢反应
CO2催化加氢反应依据活性金属种类及其还原程度, 可得到甲烷、甲醇、甲酸和二甲醚等。采用铜基催化剂可以合成甲醇[17, 18], 目前研究主要集中在反应机理和催化剂设计方面, 鲁奇公司已建成年产百万吨级甲醇工艺[19]。利用水溶性催化剂可用于CO2均相催化加氢制备甲酸[20, 21], 但该过程复杂, 催化剂分离回收困难, 不利于工业应用[22]。此外, CO2在铜基催化剂的作用下还可直接加氢合成二甲醚[23], 该反应过程还停留在实验室研究阶段, 重点考察催化剂助剂改性及反应条件的优化等[24]。
CO2加氢甲烷化是CO2与H2合成CH4的过程, 可将碳的完全氧化产物转化为CH4, 对能源领域意义重大。催化剂开发是CO2甲烷化的研究重点, 目前, 催化剂活性组分以过渡金属为主, 尤其以Ni基催化剂研究最多, 而载体则以Si和Al类材料为主[25, 26, 27]。
1.2.2 重整反应
CO2与CH4催化重整反应可用来制取富CO的合成气[28], 产生的合成气CO与H2约为1: 1, 进而通过F-T合成转化为烃或含氧化合物。该反应的强吸热性在化学储能方面应用广阔, 同时也是减少CO2和CH4排放的一条有效措施[29, 30, 31, 32]。目前, 对该反应主要集中在活性组分为贵金属和Ⅷ 族过渡金属催化剂的研究上以及提高其抗积炭性和活性等性能研究上[33, 34, 35]。
1.2.3 电化学转化
CO2电化学还原过程, 在一定条件下可得到相应的酸、醇或烃类[36], 如甲酸、甲醇、甲烷和乙烯等, 产物类型取决于CO2还原时的电极电位或电流密度[37]。常温和常压下即可实现反应, 反应条件温和、操作简单; 且在电还原过程中可通过控制电极及反应条件实现对产物的选择性合成。因此相对于其他还原方法, 电化学还原CO2具有更好的应用前景[38, 39]。
1.2.4 其他反应
CO2可以与环氧化合物聚合成环状碳酸酯[40]或聚碳酸酯[41]。日本触媒公司研发工业化规模的碳酸乙烯酯水解合成乙二醇工艺, 环氧乙烷转化率为99.9%, 碳酸乙烯酯选择性为100%, 乙二醇收率可达到99.8%[42]。此外, 通过CO2聚合成的聚丙烯碳酸酯各项性能优于聚丙烯, 而且工艺简单, 易操作, 无污染[41]。此外, 尿素是种重要的无机化工产品, 主要用于肥料以及动物饲料, CO2和氨气在22 MPa下反应可以用来合成尿素[43]。
利用CO2合成代用天然气一方面可以缓解CO2日趋增长带来的环境压力; 另一方面可以解决天然气供应短缺问题。因此, 将CO2转化为甲烷技术具有广阔的发展前景[44]。
H2是甲烷化反应的主要反应物, 制氢过程也是整个甲烷化主要的能耗过程。为了解决氢的来源问题, 可以通过风能、水能和太阳能等新能源发电进一步电解水来获得[45, 46]。与此同时, 富CO2气田以及煤电厂、煤化工厂等排放的CO2都可以提供可靠的碳源。新能源和可再生资源[47, 48]包含太阳能、地热能、风能、潮汐能及水能等[49]。与传统能源相比, 新能源具有安全、绿色、清洁等优势, 从根本上降低了CO2的排放量。
CO2甲烷化是指H2和CO2在(150~500) oC, (0.1~10) MPa及金属催化剂的作用下, 生成CH4和H2O的强放热反应过程[50, 51]。表1列出了CO2甲烷化反应过程中进行的基本反应。
2.1.1 活性金属
通过对催化剂性能考察[53, 54], 得出不同金属的CO2甲烷化反应活性为Ru> Rh> Ni> Fe> Co> Os> Pt> Ir> Mo> Pd> Ag> Au; 选择性为Pd> Pt> Ir> Ni> Rh> Co> Fe> Ru> Mo> Ag> Au。从以上规律可以看出, Ru的催化性能最好。研究发现, Ru催化剂在较低反应温度下就表现出较高的甲烷化性能。Abe T等[55]用离子溅射方法制备了TiO2负载高分散的Ru纳米颗粒Ru/TiO2催化剂, 在160 ℃时, CH4产率达到了100%。然而金属Ru价格较高, 不能满足工业化大规模生产需求[56]。
除贵金属外, 过渡金属因为廉价易得而逐渐成为CO2甲烷化反应催化剂开发的重要组成。Fe基催化剂研究较早, 工业化应用也较早, 但操作条件一般为高温高压, 易造成催化剂积炭失活, 逐渐被其他活性金属所取代[57]。而Co基催化剂对甲烷化活性相对较低且对反应环境要求较苛刻[58]。
与其他过渡金属相比, Ni基催化剂具有较高的甲烷化催化活性、反应条件相对容易控制, 研究较多[59]。活性物种流失、烧结、中毒等均可能导致催化剂失活[60], Ni基催化剂因导热性能较差, 在反应过程中容易发生烧结而失活, 因此抗烧结性能的研究也是Ni基催化剂开发的重点。多种技术被开发用来提升催化剂的抗烧结性能, 如采用MgO为载体, 利用形成的MgNiO2结构稳定性防止Ni物种的烧结[61] ; 将Ni物种负载到碳纳米管内, 利用管壁限制Ni物种的长大与团聚[62]; 使用导热性能强的SiC为载体, 减少热量聚集, 防止Ni物种高温烧结[63]。同时为了克服单一活性组分催化剂在反应过程中的弊端, 也有研究双活性金属甚至多活性金属的催化剂用于CO2甲烷化, 如Zhen W等[64]制备的Ni-Ru/Al2O3催化剂对CO2转化率和CH4选择性分别达到82.7%和100%。虽然Ni基催化剂研究较多, 在CO2甲烷化中最有可能实现工业化应用, 但目前稳定性较差, 因此继续开展催化剂的研发, 在保证催化剂活性的前提下提高催化剂稳定性仍十分必要。
2.1.2 载 体
甲烷化催化剂使用的载体通常具备以下条件:(1)高比表面积; (2)载体和金属之间有较强的相互作用; (3)多孔的孔道结构[65]。用于CO2甲烷化研究的载体较多, 包括Al2O3、CeO2、ZrO2、TiO2、SiO2和CNT等。γ -Al2O3因表面离子与活性组分较强的相互作用能使活性组分很好的分散, 而且形成了镍铝尖晶石使催化剂还原度降低, 但在反应过程中易形成积炭。Rahmani S等[66]将Al2O3制成介孔载体, 提高了反应活性。SiO2以其非常大的比表面积、高溶点和多孔性而被用作CO2氢化催化剂载体[67]。Lu B等[68]将Ni负载在SBA-15上用于CO2甲烷化, CH4选择性高达100%。Du G等[69]制备了不同Ni负载量的Ni/MCM-41催化剂, 并用于CO2甲烷化, 结果表明, Ni负载量为3%的Ni/MCM-41催化剂表现出更好的CH4选择性(99%)和时空收率[91.4 g· (kg· h)-1]。除铝氧化物和硅氧化物, CeO2和V2O5等由于丰富的氧空缺有利于CO2活化而被用于CO2甲烷化研究。Tada S等[70]采用浸渍法制备的Ni/CeO2催化剂在低温下(300 ℃)CH4选择性可达100%。ZrO2具有两性特征, 也具有较高的热稳定性和吸附CO2的性能, 因此, 常被用作CO2甲烷化载体。Yamasaki M等[71]用氧化还原方法处理无定形Ni-Zr合金制备了Ni/ZrO2催化剂, 研究发现ZrO2晶相变化会引起催化剂甲烷化活性的变化。四方相ZrO2较单斜相ZrO2表现出更高的TOF和更好的CO2吸附能力。
除金属与非金属氧化物, 某些碳基材料也因较好的稳定性被用做CO2甲烷化催化剂载体, 如碳纳米管[72], 但从工业应用看, 碳基材料并非最佳选择。金属与过渡金属氧化物虽然活性较好, 但制备过程相对复杂, 且结构控制较为困难, 研究方向应在复杂结构的开发上; Si、Al材料更符合工业应用的要求, 制备过程也相对简单, 研究方向应在催化剂活性与稳定性提高的制备方法开发上。
2.1.3 助 剂
添加助剂可以调变催化剂的物化性能, 进而改善反应性能。CO2甲烷化催化剂的添加助剂主要包括结构助剂和电子助剂。
结构助剂可以调变催化剂的织构参数, 如比表面积和孔尺寸等。文献[73]考察了Fe助剂对Ni/ZrO2催化剂的CO2甲烷化性能的影响, 发现Fe2+较强的给电子能力促进了样品对CO2的吸附, 同时抑制副反应的进行。Hwang S等[74]考察了Ru含量对于Ni-Fe/Al2O3催化剂CO2甲烷化的作用, 发现添加Ru可以改变催化剂的比表面积。此外, 活性组分Ni与助剂通过相互作用产生的协同作用阻止了活性组分Ni粒子的长大, 防止了Ni粒子的团聚, 提高了催化剂导热性能, 增加了催化剂稳定性和使用寿命。
电子助剂可以改变催化剂与CO2分子间的电子效应, 促进催化剂与CO2分子间的作用, 从而影响整个反应过程。电子助剂的加入可以调节催化剂表面酸和碱以及氧空穴的数量, 在一定程度上促进反应的进行, 提高CO2甲烷化活性。邓庚凤等[75]考察了助剂Sm对Ni/海泡石催化剂在CO2甲烷化中的影响, 结果发现, 催化剂中Sm3+具有较强的给电子能力, 使NiO更容易被还原, 并且提高了Ni的分散度, 使催化剂表面具有较多的CO2吸附中心。
2.1.4 制备方法
催化剂制备在整个催化剂设计过程中发挥着决定性作用。即使化学组成相同的催化剂, 其催化性能也会受到制备方法的影响而呈现较大差异[76, 77]。CO2甲烷化催化剂的主要制备方法有溶胶凝胶法、微乳液合成法、等体积浸渍法和双重浸渍法等。
甲烷化催化剂通常需要将金属与特定的金属盐进行结合制备[78], 采用溶胶凝胶法制备的催化剂耐热性能好, 在较高温度下也可进行甲烷化反应[79]。
通过微乳液合成的有机或无机的纳米催化剂, 导热性能良好, 且拥有大的比表面积及很高的金属分散性, 有利于CO2甲烷化反应的进行[80]。
等体积浸渍法通常用于合成多相催化剂, 活性金属前驱体首先溶于水或有机溶剂中, 然后逐滴加至载体孔内, 使滴加的金属溶液体积等于载体孔体积[81]。等体积浸渍法由于可以更好地控制金属负载量以及制备过程没有废液产生的优点, 是制备甲烷化催化剂理想的方法。Zamani A H等[82]利用等体积浸渍法制备了高分散高活性的Ru/Mn/Cu-Al2O3催化剂, 在1 000 ℃下CO2转化率将近100%。
负载型金属催化剂活性和选择性不仅受金属负载量的影响, 而且与分散在载体表面的金属颗粒大小有关。双重浸渍法用于金属负载量较大以及金属颗粒分散较好的催化剂制备。双重浸渍法需要经过两个阶段:第一阶段, 无机物载体的初步浸渍[83]。第二阶段, 将初步浸渍后的载体通过简单浸渍法浸渍于含有金属离子的溶液中。通过两个阶段的浸渍, 无机载体性质发生变化, 使得载体和金属结合在一起, 该方法有利于活性金属的分散, 并且减小了金属晶粒尺寸[84]。因此, 通过双重浸渍法制备的CO2甲烷化催化剂可以调控催化剂和反应中的参数, 如金属分散、颗粒尺寸以及催化循环。Ryczkowski J等[83]利用双重浸渍法制备了高分散的Ni/γ -Al2O3催化剂。
此外, 还有其他方法可用于CO2甲烷化催化剂的制备, 不能孤立地评价催化剂制备方法, 需要考虑其催化剂体系以及反应工艺条件, 因此, 在催化剂开发过程中还需要针对具体情况进行制备方法的筛选与优化。
2.1.5 催化剂失活
甲烷化催化剂失活的原因可分为化学失活和物理失活。在CO2甲烷化过程中催化剂的化学失活是指催化剂中毒。甲烷化反应中催化剂对含有氯化物、焦油、氨、硫化物以及碱质等气体杂质特别敏感。由于反应气流中的杂质吸附在样品的体表上, 进而填充了反应活性位点, 导致催化剂中毒[85]。催化剂物理失活主要是指热降解、催化剂污染以及催化剂磨损。催化剂寿命不仅与催化剂组成有关, 而且与反应条件有关。高温高压会促进催化剂团聚、热降解和烧结, 导致催化剂使用寿命和活性急剧下降。烧结会导致催化剂表面积减小从而导致催化剂活性下降[47]。因此, 为了避免催化剂热降解, 甲烷化反应温度应不高于500 ℃, 尽管有文献在700 ℃的高温条件下研究过甲烷化反应[86]。催化剂污垢是通过反应气流吸附在催化剂表面的物种, 进而阻塞了催化剂表面活性位点以及孔道, 最终导致催化剂失活。另外, 在流化床、移动床以及三相浆态床反应器中, 由于反应物和催化剂的磨损, 造成催化剂活性物种损失, 进而导致催化剂失活。添加助剂以及优化催化剂的制备方法能有效抑制甲烷化反应中催化剂的失活[87]。
目前, 针对高温反应催化剂的失活问题主要有以下解决途径:(1)选择导热性能优良的载体, 如ZrO2; (2)载体改性, 通过添加助剂提高催化剂的耐热性能; (3)设计和制备有序介孔或者核壳等限域结构的催化剂。
研究表明, CO2甲烷化反应可能经过两种机理发生:一种是CO中间体机理, 即CO2第一步先转变为CO, CO加氢得到CH4; 另一种是CO2直接与解离后的H* 反应得到CH4[88, 89]。
2.2.1 CO中间体机理
对于CO中间体机理, CO2解离为CO存在两种不同的途径:
(1)CO2先与反应中解离出的H* (* 代表催化剂活性位点)反应生成HCOO* , 随后HCOO* 进一步在催化剂表面分解产生CO* 。反应方程式为:
CO2+H* → HCOO* (1)
HCOO* → CO* +OH* (2)
(2)CO2在催化剂表面直接解离成为CO* 和O* 。反应方程式为:
CO2* → CO* +O* (3)
最终, 由生成的CO* 经过加氢反应生成甲烷[90]。多数研究者赞成CO2直接解离成为CO* 和O* , 而不是解离为HCOO* 。本课题组[91]通过密度泛函理论方法计算了Cu(111)面上发生这两种反应的能量关系, 通过比较每一个基元反应的活化能和能垒, 得出HCOO* 物种解离生成CO* +OH* 的反应更为困难, 该反应活化能垒为306.8 kJ· mol-1, 反应能为-1.9 kJ· mol-1, 为放热反应; 而CO* 解离生成C* +O* 的反应能垒为237.4 kJ· mol-1, 反应能为125.6 kJ· mol-1, 为吸热反应。显然, 通过计算结果可以推断, CO2甲烷化反应中CO2很可能是直接解离为CO* 和O* , 而非解离为HCOO* 。因此, CO2甲烷化反应的过程可以表示为:
CO2+H2⇌CO+H2O (4)
CO+3H2⇌CH4+H2O (5)
由于CO2分子结构相对稳定, 甲烷化过程所需活化能较高, 因此, 开发高效的催化剂体系, 构建合适的催化反应路径降低活化能, 才能有效促进甲烷化反应的进行[92]。
2.2.2 直接加氢机理
Vesselli A等[93]利用超高真空表面科学技术结合密度泛函理论计算, 考察了CO2在Ni(100)面上的加氢作用。通过高压活性测试证实了CO2直接氢化的机理, 即反应过程中没有CO中间体生成。本课题组[91]通过密度泛函理论计算显示, CO2先加氢生成C(OH
2.3.1 固定床工艺
绝热固定床装置简易、塔板间压降小、反应过程中的条件和参数容易控制[94], 广泛应用于工业生产。Beuls A等[90]研究证实, CO2甲烷化反应可以在(50~150) ℃和0.2 MPa条件下进行; 通常在一定范围内, 升高温度可以提高CO2转化率和CH4选择性, 但温度高于550 ℃时, 催化剂可能会发生烧结而失活。此外, 温度大于300 ℃时, 由于压力的限制[94], CH4选择性会达到热力学平衡。因此, 对于固定床甲烷化反应工艺, 通常需要配套一系列的散热装置来控制床层温度。
2.3.2 流化床工艺
流化床装置也可以用于甲烷化反应过程, 并且实现工业大规模生产。流化床反应器流动性较好, 固体催化剂和反应气充分均匀混合[94], 传热可以有效进行, 使得反应器内部变成一个等温环境。但由于反应过程中气泡的存在以及催化剂的磨损, 导致反应过程中催化剂与反应气不能充分接触以及催化剂磨损使得活性组分流失, 造成催化剂失活, 反应物不能完全转化[95]。
2.3.3 三相浆态床工艺
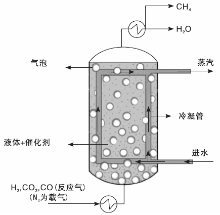
对于固定床和流化床甲烷化工艺, 反应过程中都存在催化剂烧结问题。三相浆态床装置能有效控制传热, 解决催化剂的烧结。通常三相浆态床装置所用催化剂颗粒粒径一般不大于100 μ m, 悬浮于温度恒定不变的溶剂中, 如二苄基甲苯。图2为三相浆态泡罩塔反应装置的构造图[96]。由于液体溶剂的高热容量使反应中的温度波动能被及时处理。然而由于液体介质的存在, 会影响固体催化剂颗粒和反应气体的有效接触。
PtG技术是指通过太阳能或者风能等新能源发电制氢, 然后与CO2反应合成CH4, 多余的H2用于燃料电池。早在1980-1990年, 日本就提出了电制气(PtG)技术[97], 并于2003年建成第一个PtG技术生产线[98]。PtG技术的关键在于电解技术, 目前工业上主要电解技术有3种:
(1) 碱性电解(AEL)技术。以氢氧化钾或者氢氧化钠为电解质, 在高压下电解水制取氢气, 该技术已工业应用了几十年, 发展较为成熟。采用该技术可以电解出纯度较高的氢气, 并可以调节生产能力, 被认为是PtG项目的最佳选择。然而AEL技术最大的缺点是碱性溶液的强腐蚀性会对工业设备造成一定的损耗[99]。
(2) 高分子电解质膜(PEM)电解技术。该技术以固体高分子聚合膜为基础[100], 优点是能在低温下快速启动以及具备很高的灵活性, 同时电解的氢气纯度很高。与AEL技术相比, 成本太高, 并且使用寿命较短[99, 100]。
(3) 固体氧化物电解池(SOEC)技术。该技术利用ZrO2优良的导热性能, 可以在高温下进行电解水反应[101, 102], 是近几年才发展的电解技术, 处于实验室研究阶段。对于水电解过程中产生的H2可以压缩在气体罐存储或者装入物理储存器中埋藏在地下[103]。
PtG所用的碳源主要来自于CCS技术对大气中CO2捕集储存的部分。近年来, 通过利用太阳能和风能等新能源, 欧洲建成了一些PtG项目, 尤其是德国, 表2[96]列出了当前工业化规模的PtG项目。
目前, 工业上利用CO2生产CH4包括两个关键步骤:电解制氢和甲烷化反应。通过可再生能源发电电解水产生氢[99], 催化H2与CO2生成C
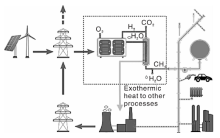 | 图3 新能源发电甲烷化过程示意图[96]Figure 3 Modern concept of integrated system of the renewable energy and CO2 methanation process[96] |
对于PtG技术, 主要的能耗过程有电解制氢、氢储存和压缩以及甲烷化反应, 其中电解制氢在整个过程能量消耗中的占比最大, 其次是氢储存和压缩过程。同时, 由于电解过程中, 电解阻力的存在, 约20%的电能在转换为化学能的过程中损失, 转化为热能; 而在H2参与CO2甲烷化的过程中, 损失了约64%的能量, 整个过程的转化效率约为35%~50%[99], 整体看, 与天然气的开发成本相比, PtG技术制取CH4成本较高, 而开车时间与单位电价都会影响到PtG技术的经济性, 只有选择合适的作业时间以及控制较低的电价才能获得理想的经济可行性[106]。
与德国、日本和美国等相比, 我国对PtG技术研究较少, 过程的效率和经济性制约着PtG技术的研究与发展。结合国内电解装置和甲烷化过程的效率, 整个PtG技术的效率可能低于40%[107]。电价、气价、装置年运行时间以及电解制氢成本对总成本影响最大, 同时, CO2的捕集纯化技术也在很大程度上影响PtG的成本[108]。当前, 制约我国PtG技术工业应用的瓶颈是电解制氢效率和电与天然气的价格。相比于发达国家, 中国新能源发电技术还不成熟, 转化效率低, 二次转换成本高, 因此, 要想提高我国PtG技术的经济性实现其应用, 除继续进行CO2甲烷化技术的开发外, 也应加快新能源发电核心技术的研发, 完善电网的运行机制和系统。
CO2是温室气体中排放量最大的气体, 主要来自化石燃料和生物质, 从这些能源物质中获取能量的过程必然伴随CO2的排放, 因此开发高效的捕集与应用技术是实现CO2资源化利用并减少其温室效应的主要途径。甲烷化反应可以将CO2转化为能源物质CH4实现碳基能源的循环, 对能源利用具有重要意义。随着CO2甲烷化研究的不断开展, 对其反应机理的认识将会越来越清晰, 而Ni基催化剂也有望在CO甲烷化后实现在CO2甲烷化中的工业应用。目前, 除催化剂尚处于研究阶段外, H2的供给也在一定程度上制约了CO2甲烷化技术的规模化应用, 而随着我国新能源利用技术的发展, 新能源发电制氢的成本将大大降低。通过新能源发电制氢并联合CO2甲烷化的PtG技术, 其成本将会越来越符合规模化应用的要求, 有望成为未来CO2资源化利用重要组成。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|
| [61] |
|
| [62] |
|
| [63] |
|
| [64] |
|
| [65] |
|
| [66] |
|
| [67] |
|
| [68] |
|
| [69] |
|
| [70] |
|
| [71] |
|
| [72] |
|
| [73] |
|
| [74] |
|
| [75] |
|
| [76] |
|
| [77] |
|
| [78] |
|
| [79] |
|
| [80] |
|
| [81] |
|
| [82] |
|
| [83] |
|
| [84] |
|
| [85] |
|
| [86] |
|
| [87] |
|
| [88] |
|
| [89] |
|
| [90] |
|
| [91] |
|
| [92] |
|
| [93] |
|
| [94] |
|
| [95] |
|
| [96] |
|
| [97] |
|
| [98] |
|
| [99] |
|
| [100] |
|
| [101] |
|
| [102] |
|
| [103] |
|
| [104] |
|
| [105] |
|
| [106] |
|
| [107] |
|
| [108] |
|