作者简介:付莹莹,1993年生,女,河北省保定市人,在读硕士研究生,研究方向为光催化。
采用改性活性半焦吸附-Fe/C微电解-Fenton联用技术处理焦化废水,探究联用技术工艺参数对焦化废水化学需氧量(COD)去除率的影响,结果表明:(1) 针对Fe/C微电解处理焦化废水的最佳操作条件为:pH=3,Fe与C质量比2.0:1,Fe/C投加量30 g·L-1,反应时间60 min,反应温度35 ℃;(2) 采用Fe/C微电解-Fenton氧化处理焦化废水最佳操作条件为:过氧化氢投加量25 mL·L-1,pH=3,Fe与C质量比2.0:1,Fe/C投加量30 g·L-1,反应时间8 h。在最佳吸附-Fe/C-Fenton联用工艺条件下操作,对焦化废水COD降解率达到85.23%,COD由199.27 mg·L-1降至29.43 mg·L-1。动力学研究表明,动力学方程能很好的拟合Fe/C微电解降解过程。
The coking wastewater was treated by modified active semi-coke adsorption-Fe/C micro-electrolysis-Fenton technology.Effects of process parameters on COD removal of coking wastewater were explored.Results showed that:(1) the optimal operating conditions for Fe/C micro-electrolysis treatment of coking wastewater were pH=3, m(Fe): m(C)=2.0:1,Fe/C dosage of 30 g·L-1,reaction time of 60 min,reaction temperature of 35 ℃;(2) the optimum operation conditions for the coking wastewater treatment with Fe/C micro-electrolysis-Fenton oxidation were 25 mL·L-1 of H2O2,pH=3, m(Fe): m(C)=2.0:1,Fe/C dosage 30 g·L-1,reaction time 8 h.Under optimal reaction conditions,COD degradation of the coking wastewater reached 85.23%,and COD decreased from 199.27 mg·L-1 to 29.43 mg·L-1.Kinetic studies showed that kinetic equations could well fit the Fe/C microelectrolysis degradation process.
焦化废水是原煤在高温干馏、煤气净化和化工产品精制过程中产生的一种有毒的难降解废水, 废水排放量大, 成分复杂, 除了氨、氰和硫氰根等无机污染物外, 还含有酚、油类、萘、吡啶、喹啉、蒽等杂环及多环芳香族化合物(PAHs)[1], 低浓度酚能使蛋白变性, 高浓度酚能使蛋白沉淀, 对皮肤、黏膜有强烈的腐蚀作用, 也可抑制中枢神经系统或损害肝、肾功能。废水中多环芳烃不仅难以降解, 还会致癌, 污染物不仅色度高, 而且在水中以真溶液或准胶体的形式存在, 性质非常稳定[2], 焦化废水的大量排放对生态环境和人类健康造成了极大威胁。
焦化废水的深度处理方法有吸附法、生物化学法、高级氧化法、微波法和膜分离法[3], 其中, 吸附法主要利用吸附剂的吸附性能对焦化废水中的物质进行脱除, 但本质是使被吸附的物质从液相转移到固相, 并没有从根本上达到降解大分子污染物的目的; 高级氧化法是指通过不同途径产生具有高反应活性的羟基自由基(· OH), 再利用其强氧化性将水中有机污染物降解, 生成小分子物质甚至直接矿化转化为CO2和水, 从而降解水中难以处理的污染物[4]。本文对改性活性半焦吸附-Fe/C微电解-Fenton联用技术处理焦化废水进行实验研究。
实验用废水取自山西省临汾市某焦化厂, 颜色为淡黄色, COD为(189212) mg· L-1, pH=7.3。
ECO6 COD快速消解仪; HJ-4A多头磁力加热搅拌器; T6新世纪紫外可见分光光度计; AL204分析天平; 管式炉。
重铬酸钾、硫酸亚铁铵、浓硫酸、硫酸银、硫酸汞、氢氧化钠和过氧化氢均为分析纯; 还原铁粉。
分析方法采用重铬酸钾法。
粒径小于100目的还原铁粉和粒径小于100目的改性活性半焦。
半焦改性吸附实验:将原料半焦进行化学改性, 向实验装置中投加一定数量的改性半焦, 将一定量污水加至反应器, 进行吸附实验。
Fe/C微电解实验:改性半焦吸附饱和后, 向实验装置中投加一定数量已处理好的还原铁粉, 采用稀H2SO4调节焦化废水pH值, 连续曝气反应一段时间, 水pH调至9~10, 离心, 取上层清液进行COD测定, 通过控制反应初始pH值、Fe与C质量比和温度等进行工艺参数研究, 确定适宜的工艺条件。
Fenton氧化实验:在Fe/C微电解实验基础上向实验装置中投加一定体积的过氧化氢(体积分数为30%), 连续曝气反应一段时间, 出水pH调至9~10, 离心, 取上层清液进行COD测定, 通过控制过氧化氢投加量、反应初始pH值及Fe与C质量比等条件进行工艺参数研究, 确定适宜的工艺条件。
实验用半焦取自陕西府谷, 用5%过氧化氢在常温、常压下改性活化24 h(改性剂与半焦体积比为1: 1), 改性目的是改变半焦表面官能团, 脱灰以增大半焦比表面积, 优化吸附性能。表1为半焦工业分析数据。
| 表1 半焦工业分析数据 Table 1 Industrial Analysis of semi-coke |
灰分中的多数无机质会对活化造孔过程产生不利影响, 故必须对半焦进行脱灰处理以提高半焦品质[5]。从表1可以看出, 经过5%过氧化氢改性后的半焦挥发分和灰分含量降低, 表明过氧化氢改性对半焦的灰分进行了有效脱除。
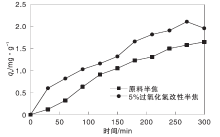
称取原料半焦和改性半焦各1.5 g, 量取原水150 mL置于250 mL烧杯中, 在常温常压下静置吸附, 每隔30 min取一次上层清液, 根据测得的吸光度计算吸附量qe, 结果见图1。
从图1可以看出, 原料半焦经5%过氧化氢改性活化之后, 吸附能力有所提高, 且随着时间的延长, 半焦的吸附量开始逐渐趋于平缓, 表明半焦吸附剂基本达到吸附饱和状态, 经过5%过氧化氢改性半焦的吸附性能优于原料半焦。
Fe/C微电解是利用铁碳之间的电极电位差, 在电解质溶液中形成无数个原电池而发生电化学反应。pH值、Fe与C质量比和温度等工艺条件均能影响其对有机污染物的降解效能。
2.2.1 pH值
废水pH值是影响Fe/C微电解系统处理焦化废水的重要参数, 其电化学反应表达式如下:
Fe+2H2O→ Fe2++H2+2OH-
Fe+2H+→ Fe2++H2
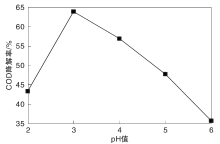
在改性半焦投加量1.5 g、Fe与C质量比为2.0: 1、反应温度35 ℃和连续曝气120 min条件下, 研究废水不同pH值时Fe/C微电解对COD降解率的影响, 结果如图2所示。
由图2可知, pH值显著影响Fe/C微电解对焦化废水COD降解率, 这是因为pH值可显著影响Fe/C电池的氧化还原电位, 进水pH由2增加到6时, 原水COD降解率先升高后降低, 在pH=3时达到最大。进水pH值较低(pH< 3)时, 有部分Fe直接和溶液中的H+发生置换反应, 实际生成的有效Fe/C原电池并不多; pH值升高(pH=3)时, Fe/C电位差使溶液中有较多的Fe2+和[H], 加速大分子污染物的开环断链, 使溶液中的COD值降低; 根据能斯特方程, 继续升高pH值(pH> 3), Fe/C电位差降低, 反应减慢, 并且较高的pH值减慢了阳极Fe的溶出速率, 使COD降解率下降。考虑到调节pH值所用酸的费用以及对于后期设备的维护, 后续实验进水pH=3。
2.2.2 Fe与C质量比
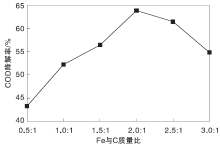
在改性半焦投加量为1.5 g、废水pH=3、反应温度35 ℃和连续曝气120 min条件下, 研究废水在不同Fe与C质量比时Fe/C微电解对COD降解率的影响, 结果如图3所示。
由图3可以看出, Fe与C质量比从0.5: 1增至2.0: 1时, COD降解率升高至63.89%, 随着铁粉投加量增加, 溶液中原电池数量随之增加, 有机物降解率也升高; 继续增加Fe与C质量比至3.0: 1, COD降解率降低。当铁粉投加量过多时, 过多的Fe2+被氧化生成Fe3+, 水解生成Fe(OH)3和Fe(OH)2絮凝沉降到Fe/C表面, 会减少与废水的有效接触面积, 削弱电极反应, 使降解率降低, 并且过多铁粉会消耗溶液中的H+, 使溶液pH值升高, 影响Fe/C微电解效能。故选择Fe与C质量比为2.0: 1作为后续实验的适宜条件。
2.2.3 反应时间
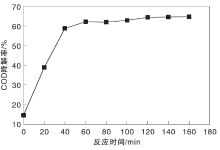
在改性半焦投加量为1.5 g、废水pH=3、Fe与C质量比2.0: 1、反应温度35 ℃和连续曝气120 min条件下, 研究废水在不同反应时间的Fe/C微电解对COD降解率的影响, 结果如图4所示。
由图4可知, 随着反应时间延长, COD降解率增加, 反应时间超过60 min, COD降解率维持约64%。随着反应的进行, 伴随着OH-增加, 溶液pH值上升, 使微电解速率减慢, 抑制反应的继续进行, 当达到一定时间, Fe/C微电解反应基本结束, 故选择最佳反应时间为60 min。
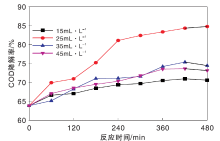
过氧化氢与Fe/C微电解反应生成的Fe2+组成的Fenton试剂具有强氧化性, 其产生的· OH可以高效氧化有机污染物, 使之开环断链从而达到净化水的目的。故过氧化氢投加量对Fenton反应处理效果影响很大, 前期工作研究中探究Fe/C微电解最适宜操作条件为:进水pH=3, 反应温度35 ℃, Fe与C质量比2.0: 1, Fe/C投加量30 g· L-1, 在此基础上, 改变过氧化氢投加量, 在连续曝气8 h条件下, 探究过氧化氢投加量对COD降解效能的影响, 结果如图5所示。从图5可知, 过氧化氢投加量由15 mL· L-1增加到45 mL· L-1时, COD降解率先升后降, 与单独Fe/C微电解处理废水时相比, 单独Fe/C微电解在反应60 min后COD降解率保持约64%, 而 Fe/C微电解耦合Fenton氧化后, 反应时间480 min时, COD降解率增加至85.23%, COD由最初的199.27 mg· L-1降低至29.43 mg· L-1。过氧化氢投加量减小时, COD降解率降低, Fe2+催化过氧化氢生成的· OH减少; 增加过氧化氢投加量时, 过多过氧化氢会氧化Fe2+成为Fe3+, 抑制了· OH的产生, 故COD降解率没有持续增加。后续实验采用过氧化氢投加量为25 mL· L-1。
利用Fe/C微电解降解焦化废水COD的动力学方程进行分析, 根据废水COD浓度随反应时间的变化, 分别以ct、-In
在Fe/C微电解最佳操作条件下, 每隔10 min取样测COD, 反应时间60 min。通过计算得出COD复合函数与时间t的关系并进行线性拟合, 结果如图6所示。
 | 图6 ct、-ln(ct/c0)、(1/ct-1/c0)、1/2* (1/ |
在Fe/C微电解最佳操作条件下, 综合比较零级(图6a)、一级(图6b)、二级(图6c)、三级(图6d)反应动力学的拟合度, 二级反应动力学拟合度最好, R2=0.962 88, 表明线性相关性好, 据此确定Fe/C微电解对于焦化废水COD降解符合二级反应动力学规律, 其反应速率与有机物浓度的平方成正比。
(1) 改性活性半焦吸附剂-Fe/C微电解处理焦化废水最适宜操作条件为:pH=3, Fe与C质量比2.0: 1, Fe/C投加量30 g· L-1, 反应时间60 min, 反应温度35 ℃。
(2) 改性活性半焦吸附剂-Fe/C微电解-Fenton联用技术处理焦化废水最佳实验条件:过氧化氢投加量为25 mL· L-1, pH=3, Fe与C质量比为2.0: 1, Fe/C投加量30 g· L-1, 反应时间480 min。
(3) 采用改性活性半焦吸附-Fe/C微电解-Fenton氧化法处理焦化废水, 废水的COD由最初的199.27 mg· L-1降至29.43 mg· L-1, 降解率达到85.23%。
(4) 在Fe/C微电解最佳实验操作条件下, Fe/C微电解对于焦化废水COD降解符合二级反应动力学规律。
致谢:本论文得到青岛市“ 惠民科技” 燃煤锅炉烟气光催化与过氧化氢氧化脱硫脱硝中试技术研究与开发(17-3-3-71-nsh)、山东电力建设第三工程有限公司燃煤锅炉烟气光催化与过氧化氢氧化脱硫脱硝中试技术研究与开发(20173702021476)以及河北沧州绿源有限公司高浓度有机废水吸附剂(活性焦)生产工艺开发(20170093)项目的资助与支持。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|