作者简介: 李 东,1992年生,男,在读硕士研究生。
采用超声辅助等体积浸渍法制备了K改性Mo掺杂SBA-16催化剂 xK/Mo-SBA-16,评价其对乙烷选择氧化反应的催化性能,并利用XRD、TEM、N2吸附-脱附、UV-Vis、UV-Raman和FT-IR等对催化剂物化性质进行表征,同时考察反应温度和K含量等因素对催化剂性能的影响。结果表明,K的添加提高了产物中醛类选择性。在 V(C2H6): V(O2)=3:1和反应温度550 ℃条件下,0.1K/5.0Mo-SBA-16催化剂上乙醛选择性为17.1%,总醛(包括乙醛和丙烯醛)产率7.4%。碱金属K的添加改变了催化剂中活性组分的结构和分散度,孤立和高分散的MoO4四面体逐渐转变为低聚扭曲的MoOx四面体,可能形成了K2Mo2O7新相。
The K-modified and Mo-doped SBA-16 catalysts,denoted as xK-Mo-SBA-16,were prepared by ultrasound-assisted incipient wetness impregnation method.Catalytic performance of those catalysts for selective oxidation of ethane were evaluated.The physicochemical properties of all the prepared samples were characterized by means of XRD,TEM,N2 adsorption-desorption,UV-Vis,UV-Raman and FT-IR.Influences of reaction temperature and K loading on catalytic performance were investigated.The experiment results demonstrated that selectivity of aldehydes in products were improved due to the addition of K element.Acetaldehyde selectivity was 17.1% and overall aldehydes (including acetaldehyde and acrolein) yield achieved 7.4% at 550 ℃ over 0.1K/5.0Mo-SBA-16 catalyst when V(C2H6): V(O2)=3:1.Structure and dispersion of active component were changed because of K addition.Isolated MoO4 species were transformed to oligomeric twisted MoOx tetrahedra and K2Mo2O7 phase was formed.
面对石油资源短缺的问题, 低碳烷烃选择氧化制低碳烯烃和含氧化合物是解决石油资源供给瓶颈的有效途径之一, 因此积极开展低碳烷烃选择氧化催化剂的制备和研究意义重大。但是在此类反应中, 产物的化学性质较反应物更为活泼, 在氧化性气氛中极易发生深度氧化反应, 因此较难同时获得高转化率和高选择性。
文献[1, 2]表明, 通过选择合适的催化剂载体, 添加相应的助剂以及改进催化剂的合成方法, 可以有效改善活性组分的分散程度, 调节催化剂物化性质, 从而提高催化剂催化活性和目标产物选择性[1]。Zhao Z等[3]研究了具有高分散隔离活性位的Cs-V/SiO2催化剂上乙烷选择氧化反应, 结果表明, 碱金属的添加大大提高了醛类化合物选择性; 高分散隔离活性位的存在改变了选择氧化反应的产物分布, 产生乙醛的同时有一定量的丙烯醛生成。Liu J等[4]将K/Mo-SBA-15催化剂应用于乙烷选择氧化反应, 取得了较好的催化效果。但是此类催化剂中高分散隔离的MoOx物种的结构以及低碳烷烃分子的活化与转化机制仍不明确。
本文以Mo掺杂介孔SBA-16(Mo-SBA-16)为研究主体, 采用超声辅助等体积浸渍法制备碱金属K改性的xK/Mo-SBA-16催化剂, 主要考察碱金属K含量和反应温度对其乙烷选择氧化性能的影响, 探讨碱金属K的添加对催化剂结构和催化性能的影响规律。
物质的量分数5%Mo掺杂SBA-16(5.0Mo-SBA-16)催化剂的制备参照文献[5]。 K改性Mo-SBA-16催化剂的制备:称取计算量KNO3溶于去离子水中, 超声直至KNO3颗粒完全溶解, 将KNO3溶液缓慢滴加到计量的Mo-SBA-16中, 边滴边搅拌, 将湿样于超声仪中分散1 h, 50 ℃ 真空干燥箱中过夜干燥, 550 ℃焙烧6 h, 得到最终产品。催化剂标记为xK/5.0Mo-SBA-16, 其中x为K的物质的量分数(0.05~0.5)。
小角XRD测定在荷兰帕纳科公司X’ Pert型X射线粉末衍射仪上进行, CuKα , λ =0.154 06 nm, 工作电压40 kV, 工作电流40 mA, 扫描范围0.5° ~5° 。
广角XRD测定在德国布鲁克公司D8 Advance型X射线粉末衍射仪上进行, CuKα , 工作电压40 kV, 工作电流30 mA, 扫描速率8° · min-1, 扫描范围10° ~90° 。金属氧化物物相由对比标准XRD数据库(JCPDS)确认。
N2吸附-脱附表征在美国麦克仪器公司ASAP 2010物理吸附仪上进行。0.2 g样品90 ℃脱水1 h升温至350 ℃保持3 h, 在液氮中冷却至77 K, 以N2为吸附质, 采用静态吸附容量法测定样品孔结构数据。
UV-Raman光谱分析在英国雷尼绍公司 inVia型拉曼光谱仪上进行, 激发光源波长244 nm。
TEM表征在日本电子株式会社JEM-2100型透射电子显微镜上进行, 将少量样品加入无水乙醇中超声分散一段时间, 将分散好的样品悬浊液滴在超薄碳膜上, 置于80 ℃烘箱中干燥后测试。
催化剂乙烷选择氧化性能评价在常压固定床微型反应器上进行。0.3 g催化剂过筛(40~60)目后装入石英反应管。反应气组成:V(C2H6): V(O2)=3: 1, N2为稀释气, 气体总流量22 mL· min-1。催化剂在550 ℃和O2气氛中预氧化30 min; 降至反应温度, 将O2切换为反应混合气, 通过程序升温方式控制反应过程的温度(每隔25 ℃取一个数据点, 每个数据点保温35 min, 以保证反应达到平衡)。用自带Ni转化炉的气相色谱(SP3420)在线分析乙烷选择氧化反应的产物。其中, Porapak Q柱分析C2H6、C2H4、CH3CHO和CH2=CHCHO等产物, TDX-01柱分析产物中的HCHO、CH4、CO和CO2。
当n(K): n(Si)=x: 100时, 不同K含量的xK/5.0Mo-SBA-16催化剂的小角和广角XRD图如图1所示。由图1可以看出, 5.0Mo-SBA-16催化剂在2θ =0.74° 和1.3° 出现归属于(110)和(200)晶面的特征衍射峰, 表明5.0Mo-SBA-16样品具有典型的三维立方介孔结构[6], 且长程有序度较好的介孔孔道。当K负载物质的量分数≤ 0.25%时, K改性后也具有两个特征衍射峰, 但随着K含量继续增加, 特征衍射峰逐渐向高角度方向偏移且逐渐宽化, 表明部分K+进入到5.0Mo-SBA-16样品的介孔孔道中, 使得材料的晶胞常数减小。继续增加K负载物质的量分数到0.5%, (110)晶面衍射峰强度继续减弱和变宽, 而(200)晶面衍射峰几乎消失, 表明K含量过高对Mo-SBA-16的介孔结构造成一定程度的破坏, 降低了材料的介孔有序度。
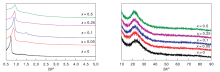 | 图1 不同K含量的xK/5.0Mo-SBA-16催化剂的小角XRD和广角XRD图Figure 1 XRD patterns of xK/5.0Mo-SBA-16 catalysts with different K loading |
由图1还可以看出, 所有材料均在2θ =23° 出现一个归属于无定形SiO2的特征衍射峰, 并没有观察到归属于MoO3或其他新物种的衍射峰, 表明MoOx物种在SBA-16中高度分散。
当n(K): n(Si)=x: 100时, 不同K含量的xK/5.0Mo-SBA-16催化剂的N2吸附-脱附等温线和孔径分布如图2所示。
 | 图2 不同K含量的xK/5.0Mo-SBA-16催化剂的N2吸附-脱附等温线和孔径分布Figure 2 N2 adsorption-desorption isotherms and pore size distribution curves of xK/5.0Mo-SBA-16 catalysts with different K loading |
由图2可以看出, 所有催化剂均呈现出Ⅳ 等温线, 表明样品具有典型的介孔结构。此外, 除了0.5K/5.0Mo-SBA-16催化剂外所有样品均具有H2型滞后环, 与SBA-16介孔分子筛等温线吻合, 表明这些催化剂均具有笼状介孔孔道结构。当K负载物质的量分数0.5%时, 滞后环类型发生明显改变, H2型滞后环变为H1型滞后环, 可能表明0.5K/5.0Mo-SBA-16样品中存在不规整的孔道结构, 与TEM结果一致。从孔径分布来看, 除0.5K/5.0Mo-SBA-16样品外, 所有样品均具有狭窄的孔径分布, 0.5K/5.0Mo-SBA-16样品的孔径分布较宽, 可能表明部分介孔孔道坍塌。
不同K含量的xK/5.0Mo-SBA-16催化剂的织构性能如表1所示。
| 表1 不同K含量的xK/5.0Mo-SBA-16催化剂的织构性能 Table 1 Textural properties of xK/5.0Mo-SBA-16 samples with different K loading |
由表1可以看出, 加入极少量K, 物质的量分数0.05%, 催化剂比表面积急剧降低至522 m2· g-1, 相应孔体积减小, 表明K元素主要位于介孔孔道中。继续增加K物质的量分数至0.25%, 催化剂比表面积和孔体积继续减少, 但平均孔径并未改变, 表明K主要位于载体的笼状介孔中[6]。当K物质的量分数0.5%时, 样品比表面和孔体积分别为248 m2· g-1和0.41 cm3· g-1, 且平均孔径增加为4.8 nm, 较大的孔径可能是形成了堆积孔。
不同K含量的xK/5.0Mo-SBA-16催化剂的TEM照片如图3所示。
 | 图3 不同K含量的xK/5.0Mo-SBA-16催化剂的TEM照片Figure 3 TEM images of xK/5.0Mo-SBA-16 catalysts with different K loading |
由图3可以看出, 5.0Mo-SBA-16催化剂具有规则的介孔孔道结构, 且未观察到MoO3纳米颗粒的存在, 与WXRD表征结果一致。从0.05K/5.0Mo-SBA-16和0.1K/5.0Mo-SBA-16催化剂中观察到较为规整的三维立方介孔结构, 表明少量K的加入未影响载体的孔道结构。随着K含量增加, 催化剂介孔有序度变差, 表明高K含量对样品的孔道结构有一定影响。继续增加K物质的量分数至0.5%, 样品的介孔孔壁上出现了一些断裂, 可能过量的K进入SBA-16的介孔孔道, 堵塞了部分孔道。
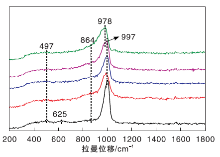
当n(K): n(Si)=x: 100时, 室温下不同K含量的xK/5.0Mo-SBA-16催化剂的UV-Raman谱图如图4所示。由图4可以看出, 5.0Mo-SBA-16样品在497 cm-1和625 cm-1处出现两个弱的拉曼峰, 分别归属于SBA-16介孔分子筛中三元和四元硅氧环的振动峰[7, 8, 9]; 而997 cm-1处强拉曼峰归属于SBA-16表面的Si— OH或样品中Mo=O的振动峰。添加碱金属K后, 625 cm-1处拉曼峰逐渐消失, 可能表明K离子优先沉积在Si— O四元环的位置; 且随着K含量增加, 997 cm-1处拉曼峰强度逐渐减弱且发生红移现象。864 cm-1处拉曼峰归属于二聚的Mo2
2.5.1 乙烷氧化反应
在催化剂0.3 g、V(C2H6): V(O2)=3: 1和气体总流量22 mL· min-1条件下, 反应温度对催化剂xK/5.0Mo-SBA-16乙烷选择氧化反应的影响见表2。
| 表2 不同反应温度对xK/5.0Mo-SBA-16催化剂乙烷选择氧化反应的影响 Table 2 Catalytic performance of xK/5.0Mo-SBA-16 catalysts for selective oxidation of ethane at different temperature |
由表2可以看出, xK/5.0Mo-SBA-16催化剂上乙烷选择氧化反应的产物有乙烯、乙醛、COx和少量的CH4。在相对高的反应温度下有极少量的丙烯醛和甲醛生成。加入碱金属K改性后, 乙醛选择性明显提高。500 ℃时, 0.1K/5.0Mo-SBA-16催化剂获得最高乙醛选择性为20.2%。考虑在500 ℃时, 总醛产率为2.9%, 550 ℃时, 总醛产率为7.4%, 综合考虑, 反应温度选择550 ℃为宜。根据Arrhenius公式计算, 0.1K/5.0Mo-SBA-16催化剂上乙烷选择氧化反应的表观活化能Ea为86.6 kJ· mol-1。
2.5.2 K含量
在反应温度550 ℃和V(C2H6): V(O2)=3: 1条件下, 不同K含量的xK/5.0Mo-SBA-16催化剂催化性能如图5所示。
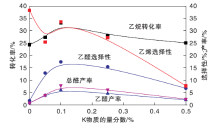 | 图5 不同K含量的xK/5.0Mo-SBA-16催化剂催化性能Figure 5 Effects of K loading on catalytic performance of xK/5.0Mo-SBA-16 catalysts |
由图5可以看出, 随着K含量增加, 乙烷转化率和乙醛选择性均呈现“ 火山型” 曲线, 先增后减。K物质的量分数从0增加到0.1%时, 乙醛选择性从1.2%增加到17.1%。K物质的量分数从0增加到0.05%时, 乙烯选择性骤然降低; 继续增加K物质的量分数至0.1%, 乙烯选择性又缓慢增大; K物质的量分数> 0.1%, 乙烯选择性从33.5%减小到7.3%。乙醛产率和总醛(包括甲醛、乙醛和丙烯醛)产率的变化趋势与和乙烷转化率变化规律相同, 随着K含量增大先增后降。因此, 在此反应条件下, 0.1K/5.0Mo-SBA-16催化剂具有最优的乙烷选择氧化性能。
2.5.2 乙烯氧化反应
在催化剂0.3 g、V(C2H4): V(O2)=2: 1和气体总流量22 mL· min-1条件下, 反应温度对5.0Mo-SBA-16和xK/5.0Mo-SBA-16催化剂上乙烯氧化性能的影响如图6所示。
 | 图6 反应温度对5.0Mo-SBA-16和xK/5.0Mo-SBA-16催化剂上乙烯氧化性能的影响Figure 6 Effect of reaction temperature on catalytic performances of 5.0Mo-SBA-16 and K/5.0Mo-SBA-16 catalysts for selective oxidation of ethylene |
由图6可以看出, 随着反应温度升高, 乙烯转化率增加, K改性后催化剂上乙烯转化率增加幅度明显高于未改性的催化剂, 表明K的添加促进了乙烯氧化反应的发生。乙醛选择性随反应温度的升高略微增加, 但K/5.0Mo-SBA-16催化剂上乙醛选择性明显高于未改性催化剂, 表明K元素的引入是影响乙醛选择性的关键因素。K含量致使乙烯深度氧化反应加剧, 而中等含量的K元素加入则有利于乙醛的形成, 可能是K含量过高会导致乙醛发生深度氧化而降低了乙醛选择性。
反应温度对0.1K/5.0Mo-SBA-16催化剂上乙烯氧化产物选择性的影响如图7所示。
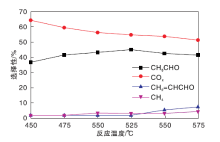 | 图7 反应温度对0.1K/5.0Mo-SBA-16催化剂上乙烯氧化产物选择性的影响Figure 7 Effect of reaction temperature on product selectivity over 0.1K/5.0Mo-SBA-16 catalyst for oxidation of ethylene |
从图7可以看出, 在(450~525) ℃, 0.1K/5.0Mo-SBA-16催化剂上COx选择性随温度的升高从64.2%降到54.3%, 乙醛选择性随温度升高从35.8%增到44.4%。当温度高于525 ℃时, 乙醛选择性开始降低, 而COx选择性降低幅度较小, 同时观察到丙烯醛的生成。结合所有产物选择性随温度的变化趋势, 可能表明产物中丙烯醛是由乙醛产生的。
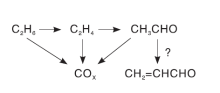
综合所有催化活性评价结果, 推测K/5.0Mo-SBA-16催化剂上乙烷选择氧化反应可能的路径如图8所示, 乙烯可能是形成乙醛的中间产物, 而高温下少量的丙烯醛可能是由乙醛和甲醛缩合而产生[3]。
(1) 碱金属K的添加改变了催化剂中活性组分的结构和分散度, 孤立、高分散的MoO4四面体逐渐转变为低聚扭曲的MoOx四面体, 可能形成K2Mo2O7新相。
(2) 考察了反应温度和K含量对K/5.0Mo-SBA-16催化剂乙烷选择氧化性能的影响。结果表明, 碱金属K的引入提高了乙醛选择性, 且在高温下有少量的丙烯醛形成。在V(C2H6): V(O2)=3: 1和反应温度550 ℃条件下, 0.1K/5.0Mo-SBA-16催化剂上乙醛选择性17.1%, 总醛(包括乙醛和丙烯醛)产率达7.4%。
(3) 考察了K改性前后催化剂的乙烯氧化反应性能, 提出了K改性催化剂上乙烷选择氧化反应的反应途径, 乙烯可能是形成乙醛的反应中间体。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|