作者简介:张玲玲,1993年生,女,河北省衡水市人,在读硕士研究生。
以葡萄糖为碳源,发烟硫酸为磺酸化试剂,分别采用水热碳化法和热解碳化法制备碳基固体酸催化剂。使用扫描电镜、热重分析、X射线衍射和傅里叶变换红外光谱等对催化剂进行表征,并评价催化剂在纤维素水解反应中的性能。结果表明,两种碳化方式制备的碳基固体酸催化剂在形貌上具有很大差异,但结构上均含有—OH、—COOH和—SO3H官能团,对于纤维素的水解反应,在150 ℃反应3 h,纤维素水解率超过60%。
Carbon-based sulfonated solid acid catalysts were prepared using glucose as carbon source and fuming sulfuric acid assulfonation reagent by hydrothermal carbonation and pyrolysis carbonization.Catalysts were characterized by scanning electron microscopy(SEM),thermogravimetry(TG),X-ray diffraction(XRD) and Fourier transform infrared(FT-IR) spectroscopy.The catalyst was tested in hydrolysis of cellulose.Results showed that the catalysts prepared by the two carbonization methods were very different in morphology,but they all contained —OH,—COOH,—SO3H functional groups.For hydrolysis of cellulose,under optimized conditions,cellulose hydrolysis rate was up to 60% or more.
酸催化反应是化工领域重要的反应之一, 酸催化反应的发展趋势是以环境友好的固体酸代替液体酸。近年来, 碳基磺酸化固体酸作为一种全新的可替代液体酸的强酸材料备受关注[1, 2]。
该类材料一般通过对磺酸化多环芳香化合物进行不完全碳化和对诸如蔗糖、葡萄糖、淀粉和纤维素等有机化合物进行不完全碳化后再磺酸化[2]。其中葡萄糖的碳化是近年来受到重视的一种制备碳材料的新技术, 该类催化剂具有催化条件温和、易分离和回收、对环境友好等优势, 广泛应用于催化、吸附、能源存储等领域的研究中[3]。此类催化剂一般分为碳化和磺化两个步骤[13, 14], 碳化分为两种:一是对蔗糖、葡萄糖、淀粉和纤维素等有机化合物进行水热碳化[14], 二是对其进行热解碳化[13]。本文以葡萄糖为原料, 浓硫酸为磺酸化试剂, 采用水热碳化法和热解碳化法制备碳基固体酸催化剂, 采用扫描电镜(SEM)、热重分析(TG)、X射线衍射(XRD)和傅里叶变换红外光谱(FT-IR)对其进行表征, 并比较在纤维素水解反应中的催化性能。
葡萄糖、3, 5-二硝基水杨酸, 天津市光复精细化工研究所; 硫酸、氢氧化钠、酚酞, 北京化工厂; 、酒石酸钾钠、亚硫酸钠, 天津光复科技发展有限公司。以上均为分析纯。
23K开启式真空/气氛管式电炉, 天津市中环实验电炉有限公司; AG-1605空气发生器、NG-1905氮气发生器, 北京科普生分析科技有限公司; ALC-210.4型电子天平, 赛多利斯科学仪器(北京)公司; SHB-Ⅲ 型循环水式多用真空泵, 郑州长城科工贸有限公司; WG-71型电热恒温鼓风干燥箱, 天津市泰斯特仪器有限公司。
热解碳化法:称取适量葡萄糖放入管式炉, 在350 ℃对葡萄糖进行高温碳化10 h, 得碳化产物。
水热碳化法:称取适量的葡萄糖置于水合反应釜中加入适量三氯化铁和去离子水, 在180 ℃反应6 h, 得黑色碳化产物。
磺化:将两种碳化方式得到的产物分别进行磺化, 在110 ℃反应9 h, 得到碳基固体酸催化剂。
采用日本电子株式会社JSM6360LV型扫描电子显微镜对催化剂的结构进行表征; 采用日本理学公司D/max 25900型X射线衍射仪对催化剂结构进行表征; 采用美国 Thermo 公司Nicolet iS10型傅里叶变化红外光谱仪分析催化剂表面的官能团; 采用日本精工DTA/TG6300型差热-热重联用分析仪测定催化剂的热稳定性。
向反应釜中加入适量的催化剂和纤维素及一定量的去离子水, 在150 ℃反应3 h, 过滤得水解液, 采用DNS法测其水解率。
葡萄糖、热解碳化产物、热解碳化磺化产物、水热碳化产物和水热碳化磺化产物的SEM照片如图1所示。
由图1可以看出, 葡萄糖为不规则块状晶体, 晶体相对较大且完整, 长度约150 μ m。经过热解不完全碳化后得到不规则晶体碎块, 长度为(50~100) μ m, 且晶体碎块之间间距相对较大。经过磺化的碳基固体酸催化剂晶体碎块之间间距明显相对变小, 部分碎块之间发生粘连。水热碳化产物为约10 μ m的碳微球结构, 层状相叠, 且小球之间形成许多环状结构堆积在一起, 产生较多空隙, 经磺化所得的催化剂形貌与碳化产物相似, 为约10 μ m的碳微球, 但磺化后的碳微球之间明显发生粘连, 并且之间的空隙减小。
对两种碳化方式得到的产物和磺化产物进行FT-IR分析, 结果如图2所示。
由图2见, 葡萄糖经碳化后, 在约3 220 cm-1处羟基— OH的吸收峰依然存在, 表明两种碳化方式葡萄糖发生的均为不完全碳化。在约1 697 cm-1、1 688 cm-1处的吸收峰为C=O的伸缩振动峰, 在约1 520 cm-1、1 525 cm-1处的吸收峰为羧酸根COO— 的反对称伸缩振动峰。在约1 158 cm-1、1 150 cm-1处的吸收峰为芳环上=CH面内弯曲振动峰, 表明碳化后的产物结构发生变化。在1 029 cm-1、1 190 cm-1处的吸收峰为S=O的对称伸缩振动吸收峰, 表明碳化产物上负载了磺酸基, 但磺化后制备的催化剂仍然保留了碳化产物的基团。以上分析表明, 碳化产物上亲水基团的存在使得磺酸基较容易负载, 两种方式制备的催化剂均含有相同的官能团。
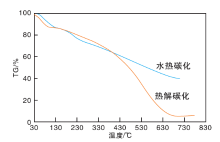
对碳基固体酸催化剂进行热重分析, 结果如图3所示。
由图3可以看出, 两种碳化方法制备的碳基固体酸催化剂在30 ℃开始分解, (50~120) ℃有较为明显的失重现象, 可能是由于催化剂吸附的水分挥发所致。(120~210) ℃的曲线呈现平稳趋势, 表明该温域基本没有失重现象。水热碳化法制备的催化剂在210 ℃以上一直处于失重状态, 但下降速率较平稳, 表明高于210 ℃的分解速率相同。然而, 热解碳化制备的催化剂在(210~400) ℃有失重现象, 可能是由于催化剂脱出小分子物质所致, 在(400~680) ℃发生较明显的失重现象, 并且失重速率较快, 表明400 ℃以上加速了催化剂的分解速率。680 ℃以上趋于平稳, 可能是由于发生积炭所致。由此可见, 两种碳化方式制备的碳基固体酸催化剂在相似的条件下先表现出稳定性, 可用于相同的体系。
为进一步了解固体酸催化剂的碳结构形态, 对两种碳化方式最佳条件下制备的碳化产物和磺化产物进行XRD分析, 结果如图4所示。由图4可以看出, 碳化产物在20° ~30° 出现明显的特征峰, 表明两种碳化产物均为无定型碳结构。磺化产物催化剂在20° ~30° 也出现特征峰, 表明磺化过程对碳化产物结构没有造成影响。碳化产物经磺化后, 衍射峰向高角度方向发生位移, 表明磺化促使碳化产物进一步聚合, 与SEM结果一致。
(1) 通过红外谱图分析, 两种方式葡萄糖碳化均为不完全碳化, 且制备的碳基固体酸催化剂均含有— OH、— COOH和— SO3H等官能团。
(2) 通过热重分析可知, 两种催化剂在(120~210) ℃热稳定性较好。
(3) 由XRD分析可知, 两种碳化方式制备的碳基固体酸催化剂均为无定形碳结构, 磺化过程是碳化产物的进一步聚合。
(4) 通过比较, 两种碳化方式制备的碳基固体酸催化剂水解率相差不大, 推断碳化过程对催化剂影响不大, 磺化是催化剂性能的主要影响过程, 因此, 磺酸基为起催化作用的主要活性基团。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|