作者简介:孙文静,1992年生,女,河北省承德市人,在读博士研究生,研究方向为催化湿式氧化过程及机制研究。
草甘膦是种广谱除草剂,草甘膦废水产量大、可生化性差。以钙钛矿型La0.8Ce0.2Fe0.9Ru0.1O3/TiO2为催化剂,采用湿式氧化(WAO)和催化湿式氧化(CWAO)法对草甘膦废水进行高效降解,并对草甘膦降解机制进行研究。应用XRD和XRF对催化剂进行表征,结果表明,合成的催化剂具有钙钛矿结构,但由于Ru原子半径太大可能没有完全进入钙钛矿骨架,导致CWAO反应后有微量Ru溶出。考察反应温度对草甘膦降解的影响,并对反应过程中C、N、P产物的选择性进行分析,结果表明,提高反应温度和加入催化剂有利于提高草甘膦转化率及对CO2和P3-4的选择性,但反应温度过高不利于生成N2,因为高温下NH3-N更容易被氧化成N-2和N-3。在实验条件下,合适的反应温度为200 ℃,反应180 min草甘膦转化率大于95%,同时对CO2和N2有较高的选择性,分别为54.59%和19.40%。应用计算量子化学计算草甘膦分子的净电荷分布,结果表明,WAO和CWAO中草甘膦反应的断键部位为C—C键、C—P键和C—N键,而后中间产物再进一步被氧化为CO2、N2、 N-2、N-3、P3-4等。
Glyphosate is a broad-spectrum herbicide.In the synthesis process of glyphosate,large amount of wastewater would be produced and biodegraded difficultly.The degradation mechanism of glyphosate by catalytic wet air oxidation(CWAO) on La0.8Ce0.2Fe0.9Ru0.1O3/TiO2 was studied. The catalyst was characterized by XRD and XRF.The results showed that the catalyst had perovskite structure.Ru did not completely enter into the catalyst framework because of too large atomic radius which resulted in dissolution of Ru after CWAO.Effects of reaction temperature on degradation of glyphosate were investigated.Selectivity of products of C,N,P was analyzed.The results showed that the conversion of glyphosate and selectivity of CO2 and P3-4 could be significantly enhanced by addition of catalyst and increasing of reaction temperature.Glyphosate was more likely to be oxidized to N-2 and N-3 instead of N2 at high temperature.After 180 min at 200 ℃,the conversion of glyphosate was greater than 95% while the selectivity of CO2 and N2 were 54.59% and 19.40%,respectively.Combined with the computational quantum chemistry, the mechanism of glyphosate degradation was assumed that C—C,C—N and C—P are the active sites in these WAO and CWAO reactions,and both the CO2,N2,N-2,N-3,and P3-4 could be generated during oxidation process.The net charge numbers of all the atoms were displayed to confirm the possibility and feasibility of the above reactions.
草甘膦于1971年由美国孟山都公司开发成功, 是种广谱除草剂。草甘膦占农药销售额的19%, 中国是全球最大的草甘膦生产国, 草甘膦废水产量大、酸性强、盐度高、难降解有机污染物含量高[1]。美国环境保护署通过实验证明草甘膦在35 ℃下, pH为3, 5, 6和9的水中稳定存在; 草甘膦在自然光照射下, pH为5, 7和9的缓冲溶液中稳定存在[2]。2014年国际癌症研究机构发现草甘膦制剂会增加患B细胞淋巴癌的风险[3]。2015年, 世界卫生组织国际癌症研究机构基于流行病学研究、动物研究和体外研究确定草甘膦为“ 可能对人类致癌” 物质[4]。我国草甘膦废水治理技术存在以下问题:物理法对草甘膦的回收率低[5, 6, 7]、生化法占地面积大且产生大量活性污泥[8, 9]、焚烧法成本较高[10]。催化湿式氧化法(CWAO)是种处理高浓度有机废水的有效方法, 能够处理COD在(10 000~10 0000) mg· L-1的工业废水, 每吨废水运行成本为70~100元, 工业化应用广泛, 可以用来处理制浆废水、印染废水、炼油废水、酿酒厂废水、氧化铝精炼废水、食品工业废水、皮革工业废水及市政废物等[11, 12]。从处理效果及成本方面综合考虑催化湿式氧化对于降解草甘膦废水是种很有前景的应用方法。因此, 开发催化湿式氧化系统高效稳定催化剂并优化反应条件对治理草甘膦废水具有重要意义。
非均相CWAO中常用的催化剂活性组分有贵金属(Pd, Pt, Ru, Ir, Rh)及其氧化物[13, 14]、过渡金属(Mn, Fe, Co, Ni, Cu)氧化物[15]、稀土金属氧化物[16]及上述活性组分组合[13, 17, 18, 19, 20]; 常用的载体有TiO2、γ -Al2O3、CeO2、Zr
以TiO2(阿拉丁试剂, 分析纯, TiO2≥ 99.0%)为载体, La(NO3)3· 6H2O(国药集团化学试剂有限公司, 分析纯, 以La2O3计≥ 44.0%), Ce(NO3)3· 6H2O(国药集团化学试剂有限公司, 分析纯, 纯度≥ 99.0%), Fe(NO3)3· 9H2O(天津市科密欧试剂有限公司, 分析纯, 纯度≥ 98.5%)和RuCl3(南京贵金属厂, 化学纯, Ru≥ 37%)为活性组分前驱体, 采用等体积浸渍法制备催化剂, 其中, 活性组分总量控制为0.002 mol· g-Ti
采用 PANalytical公司X’ Pert PRO型粉末衍射仪进行XRD分析。CuKα , λ =0.154 06 nm, 2θ =20° ~90° , 工作电压40 kV, 工作电流40 mA, 扫描速率5° · min-1。将样品研磨至200目粒度进行测定。测试完毕后进行定性分析。
采用 PANalytical公司Magix 601型X射线荧光光谱仪进行无机元素分析。样品研磨至粉末后使用25 MPa压力压成薄片进行测定。
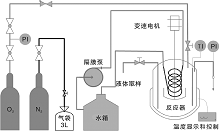
催化湿式氧化采用的高压釜为大连通达反应釜厂制造的一种强磁力旋转搅拌、间歇运行反应器, 型号为CJF-05, 容积0.5 L, 设计压力为10 MPa, 设计温度为300 ℃。催化湿式氧化间歇反应装置如图1所示。
开反应前先用10倍体积N2置换反应器顶部空气, 达到反应温度和压力时间即为反应零点, 反应过程中取样时间分别为10 min、20 min、30 min、60 min、90 min、120 min和180 min, 每次取样3 mL, 共取样7次, 测定每个取样点出水的草甘膦浓度、TOC浓度、TP浓度、P
催化湿式氧化反应后的La、Ce、Fe、Ru、Ti元素的溶出采用美国PerkinElmer 公司Optima 7300DV型电感耦合等离子体发射光谱仪(ICP)进行定量分析。
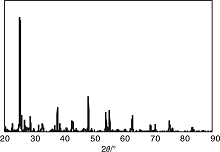
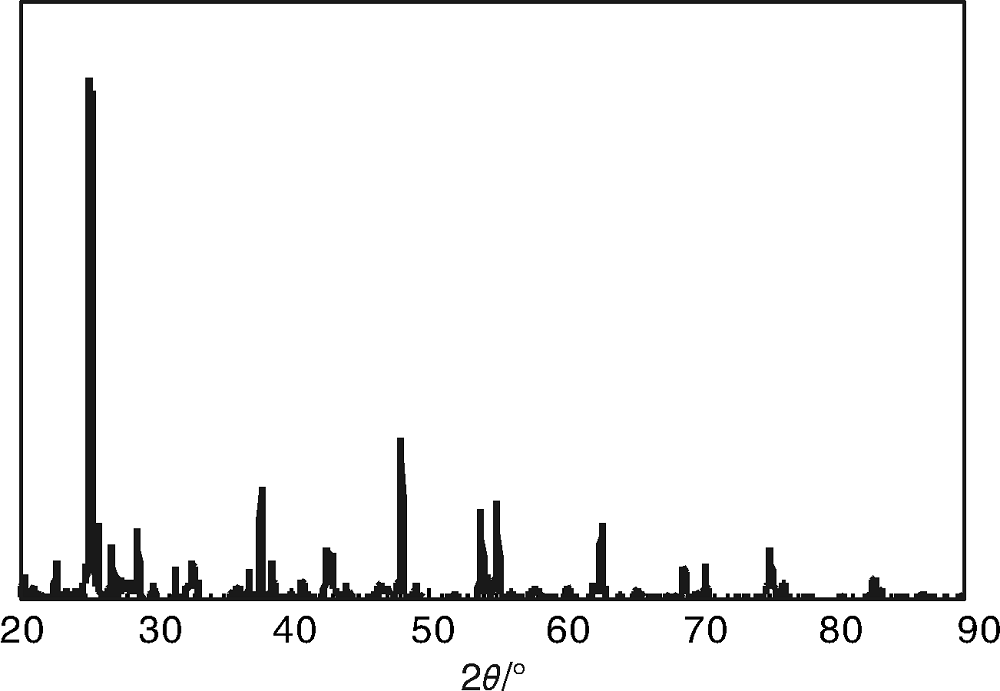
图2为La0.8Ce0.2Fe0.9Ru0.1O3/TiO2催化剂的XRD图。从图2可以看出, 与钙钛矿及锐钛矿相二氧化钛标准衍射图谱相比, 可知制备的催化剂具有钙钛矿相结构。
La0.8Ce0.2Fe0.9Ru0.1O3/TiO2催化剂的XRF表征结果见表1。由表1可知, 合成的催化剂同理论计算值基本吻合, 将Ru作为基准, 表征结果中其余元素含量均大于理论值, 说明实际催化剂中Ru含量偏低。这可能是高温焙烧导致Ru的氧化物升华流失导致的, 因为一般含活性组分Ru的焙烧温度为(350~450)℃[24, 25], 而本文选择的焙烧温度为800 ℃。
| 表1 La0.8Ce0.2Fe0.9Ru0.1O3/TiO2催化剂的XRF表征结果 Table 1 XRF analysis of catalyst |
2.3.1 反应温度的影响
在草甘膦起始浓度为10 000 mg· L-1、反应时间180 min、起始氧分压2.0 MPa和催化剂用量5 g· L-1的条件下, 考察反应温度对草甘膦转化率的影响, 结果如图3所示。
从图3可以看出, 随着温度升高, WAO和CWAO对草甘膦转化率均呈上升趋势, 草甘膦在CWAO中较WAO中更容易被降解。在温度220 ℃下, 无论是CWAO还是WAO在反应60 min后, 均能达到稳定的转化率, 约为98%。
2.3.2 催化湿式氧化选择性分析
由于草甘膦粉剂中的主要杂质为甲醛和亚硝基草甘膦。而甲醛在CWAO中为容易被降解的底物[26], 因此在分析催化剂选择性时基于以下假设:(1)甲醛比草甘膦更容易被矿化; (2)亚硝基草甘膦中磷的降解规律同草甘膦中磷的降解规律相同。
在草甘膦起始浓度为10 000 mg· L-1、反应时间180 min、起始氧分压2.0 MPa和催化剂用量5 g· L-1条件下, 降解草甘膦反应过程中磷的选择性, 碳的选择性和氮的选择性见表2~4。
| 表2 反应过程中磷的选择性分析(%) Table 2 Selectivity analysis of phosphorus in reaction process (%) |
| 表3 反应过程中碳的选择性分析(%) Table 3 Selectivity analysis of carbon in reaction process(%) |
| 表4 反应过程中氮的选择性分析(%) Table 4 Selectivity analysis of nitrogen in reaction process(%) |
从表2可以看出, 随着温度的升高, WAO和CWAO反应对P
因此, 在本体系下, 合适的反应温度为200 ℃, 既可以保证较高的草甘膦转化率又可以对CO2和N2有较高的选择性。
杨民等[27]在140 ℃条件下使用La1.4FeO3.6进行CWAO降解水杨酸反应, 活性组分La溶出量为49.5 mg· L-1, Fe溶出量为15.6 mg· L-1。使用0.45 μ m滤膜过滤, 采用ICP-OES对220 ℃-CWAO反应180 min后出水元素分析显示, Ru溶出量为76 mg· L-1, La、Ce、Fe和Ti均未检出。表明合成的钙钛矿结构在酸性条件下具有很好的稳定性, 同时TiO2载体也具有很好的抗酸性性能。Ru有微量流失, 这可能是采用共浸渍法部分Ru没有进入钙钛矿结构骨架造成的。
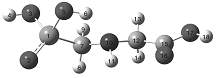
使用Gaussian 09软件对草甘膦分子中各原子所带的净电荷进行计算, 其中用计算量子化学方法和基组为Hartree-Fock和STO-3G, 并用GaussView 5.0可视化草甘膦分子结构图及计算结果, 如图4和表5所示。
| 表5 草甘膦分子净电荷分布图 Table 5 Net charge distribution of glophosate |
在湿式氧化(WAO)中以氧气为氧化剂, 在CWAO中氧气首先被催化剂活化变成活性氧原子[28]。氧气和活性氧原子在参与反应时会首先进攻负电荷多的部位, 因此发生断键的部位为C— C键、C— P键和C— N键, 如生成有机磷化合物、磷酸、甲酸铵、乙酸铵、磷酸铵、乙酸、甲酸等中间产物, 而后中间产物再被进一步氧化为CO2、N2、 N
(1) 提高反应温度和加入催化剂有利于提高草甘膦转化率及对CO2和P
(2) 在实验条件下, 合适的反应温度为200 ℃, 既可以保证较高的草甘膦转化率同时对CO2和N2有较高的选择性, CWAO反应180 min时草甘膦转化率大于95%, 同时对CO2和N2有较高的选择性, 分别为54.59%和19.40%。
(3) 根据计算量子化学模型计算出的草甘膦净电荷分布可知, 在WAO和CWAO中发生断键的部位为负电荷多的部位, 如C— C键、C— P键和C— N键, 而后中间产物再进一步被氧化为CO2、N2、 N
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|