作者简介:王宝,1994年生,男,在读硕士研究生,研究方向为催化化学。
对甘油选择性催化氧化转化为二羟基丙酮的研究进行综述,介绍了负载型催化剂在不同条件下对产物选择性和反应物转化率的影响,以及催化剂的作用机理。阐述了甘油催化氧化存在的问题以及发展前景。从均相到非均相催化,从单金属到双金属负载催化,从金属到非金属催化,甘油氧化反应的研究不断在完善。研究发现用Bi改性的Pt负载催化剂可以有效地将甘油选择性催化氧化为二羟基丙酮,在最优条件下,可获得较高的甘油转化率和二羟基丙酮选择性,但催化剂稳定性较差,有待进一步提高。杂多酸催化剂以及非金属催化剂也存在稳定性差的问题。指出改善催化剂的稳定性将是未来研究的主要方向。
Recent progress in selective catalytic oxidation of biodiesel glycerol to dihydroxyacetone was summarized.Effects of supported catalysts on product selectivity and conversion of reactants under different conditions were introduced.At the same time,mechanism of catalyst was introduced.Unsolved problems and prospects of catalytic oxidation of glycerol were described. From homogeneous to heterogeneous catalysis,from single metal to bimetallic supported catalysts,from metal to non-metal catalysis,the study of glycerol oxidation has been improving.A large number of studies have found that Bi-modified Pt supported catalysts can effectively catalyze selective oxidation of glycerol to dihydroxyacetone.Under optimal conditions,high glycerol conversion and dihydroxyacetone selectivity can be obtained.However,stability of catalyst is poor and needs further improvement.Heteropoly acid catalysts and non-metal catalysts also have problem of low stability.Therefore,stability improvement of catalyst will be one of main problems to be solved in future research.
生物柴油具有可再生、污染物排放量少、对温室效应影响小、易生物降解、材料来源宽泛、安全可靠等优势, 而且分子量不大, 可直接用作燃料, 不需要专用的柴油机, 因而可作为化石燃料的替代品[1], 被认为是种极具潜力的再生资源。随着油价上涨以及化石能源的不断消耗, 生物柴油的需求量急速增加。作为生物柴油副产物的粗甘油, 随着生物柴油生产量的增加而迅速增长, 导致甘油大量过剩[2]。
研究表明, 每产出9 t的生物柴油就会产生1 t副产物粗甘油[3]。大量甘油的副产一方面致使甘油价格下降[4], 另一方面, 副产物的利用不充分导致生物柴油成本增加。因此对甘油进行纵向加工, 以此降低生物柴油的成本, 对促进生物柴油项目的发展、效益和市场竞争力起至关重要的作用[5]。目前, 甘油开发利用已引起广泛关注, 越来越多的研究者为甘油寻找利用途径, 将廉价的甘油转变成更具价值的化工产物[6], 下游产物的开发和利用成为当前科研的主要方向[7]。根据反应条件, 甘油氧化可形成各种产物, 如二羟基丙酮、甘油醛、甘油酸、乙醇酸、羟基丙酮酸、中草酸、草酸、丙醇酸和甲酸等[8]。研究者希望通过合适的催化剂和反应条件来控制反应过程中反应物的转化率以及产物选择性。在众多甘油产物中, 二羟基丙酮是最具有应用前景的高附加值化工产品之一[9, 10]。
本文对近年来生物柴油主要副产物甘油选择性催化氧化转化为二羟基丙酮的研究进行综述, 介绍负载型催化剂在不同条件下对产物选择性和反应物转化率的影响, 同时介绍催化剂的反应机理。
甘油作为基本化工原料, 广泛应用于多个行业近2000多个产品。各行业使用比例为医药6%, 化妆品5%, 烟草6%, 涂料36%, 牙膏35%, 其他12%[11]。
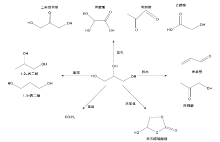
甘油有两种不同的羟基结构, 而这种结构使其易被氧化, 然而不同的反应条件或者催化剂对两种羟基选择性不同[12]。目前, 将甘油作为原料进行下游产品生产的主要过程如图1所示。甘油可以参与氧化、酯化、硝化、醚化、胺化和卤化等多种化学反应, 将廉价的甘油转化为高附加值的化工产品。在一定条件和催化剂作用下甘油经选择性氧化生成甘油酸和二羟基丙酮[13, 14]。经脱水生成丙烯醛[15]、经发酵或氢解生成1, 3-丙二醇[16, 17]、经氢解生成l, 2-丙二醇[18, 19, 20]、经重整生成合成气[21]以及碳酸甘油和缩水甘油等。其中二羟基丙酮由于具有较高的附加值, 有较大的市场需求, 已成为甘油氧化转化研究的热点。
二羟基丙酮是最简单的多羟基酮糖, 极易溶于水、乙醚、乙醇和丙酮等多种溶剂[22]。通常以二聚体的形式存在, 经加热或者溶解就会分解为单体。二羟基丙酮含有多个官能团, 所以化学性质非常活泼, 可合成多种有机化合物, 因此是种非常有价值的化工中间体, 如在工业应用上, 能还原丁二烯、苯乙烯等。作为一种天然的酮糖, 二羟基丙酮可作为一种多功能的食品添加剂, 并且食用后不会对人体产生伤害[23], 还能被微生物降解, 对环境无污染。二羟基丙酮也可作为保鲜剂的主要成分用于水果蔬菜、水产品、肉制品的防腐保鲜[24]。在化妆品行业, 可将二羟基丙酮作为配方原料, 能阻止表皮水分的过度蒸发, 起到防晒、防紫外线辐射和保湿的作用。在医药行业, 二羟基丙酮是种非常重要的医药中间体, 已经用于低血糖与糖尿病患者的治疗上, 还可以治疗某些病毒性的皮肤病, 二羟基丙酮的衍生物制成的药物, 还可用于抵抗艾滋病[25]。二羟基丙酮作为体内糖代谢过程的作用中间产物, 可以代谢猪体内的脂肪, 加快脂肪的消耗速率, 减少消耗蛋白质, 从而使蛋白质增加, 提高猪的瘦肉率[26]。二羟基丙酮还可以和丙酮酸联用, 有效的促进机体的代谢率和脂肪酸的氧化, 燃烧脂肪, 减少体重, 预防相应的疾病, 改善胰岛素的敏感度, 降低胆固醇, 增加血糖利用率, 提高运动员的有氧耐力。在皮革行业, 二羟基丙酮可作为皮革制品的保护剂[27]。二羟基丙酮也可用于制作抗病毒试剂, 如鸡蛋胚胎的培养过程中, 二羟基丙酮能够消灭大部分鸡瘟病毒。
对气相催化氧化甘油生成二羟基丙酮的研究较少。Lari G M等[28]研究了气相催化氧化甘油生成二羟基丙酮, 制备了Fe掺杂不含铝的分子筛催化剂, 在温度350 ℃、甘油流速0.012 mL· min-1、O2与甘油物质的量比为3.5、液态空速52 900 h-1的条件下, 甘油转化率接近100%, 二羟基丙酮选择性可达84%。催化剂表现出高的活性和稳定性主要得益于其结构, 铁的形态以及酸度的影响。低酸度抑制了副反应的进行, 分布较分散的活性位点使铁具有较强的选择性氧化性能。在很大程度上优于基于贵金属的催化剂。
相对来说对液相催化氧化甘油生成二羟基丙酮的研究更为普遍, Painter R M等[29]在室温下以Pd络合物催化液相甘油, 以乙腈为溶剂, 转化率为97%, 目标产物选择性达96%。表明溶剂性质对甘油氧化反应有一定的作用。Chung K等[30]以[(neocupoine)Pd-(OAc)]2(OTf)2为催化剂, 乙腈与水体积比9:1作溶剂, 25 ℃下反应3 h, 甘油转化率达97%, 二羟基丙酮选择性达99%, 70 ℃下反应72 h, 二羟基丙酮产率为65%。通过保护末端羟基来选择性氧化仲羟基, 从而生成二羟基丙酮, 抑制副反应的发生。Crotti C等[31]以Fe(BPA)2(OTf)2为催化剂, 过氧化氢为氧化剂, 催化氧化甘油生成二羟基丙酮。在Fe浓度为0.01 mol· L-1; n(甘油):n(Fe)=35、n(过氧化氢):n(甘油)=2.8、过氧化氢质量分数30%、乙腈与水体积比2:1混合溶液为溶剂、n(双酚基丙烷):n(Fe)=2和温度25 ℃的条件下反应90 min, 产物只有二羟基丙酮和甲酸, 甘油转化率为46%, 二羟基丙酮选择性为53%。通过调整实验条件, 在Fe浓度为0.01 mol· L-1; n(甘油) :n(Fe)=35、n(过氧化氢) :n(甘油)=1.5、过氧化氢质量分数30%、溶剂乙腈与水体积比=2:1、n(双酚基丙烷):n(Fe)=3和25 ℃的条件下, 完全抑制了甲酸的生成, 反应90 min后甘油转化率为17%, 二羟基丙酮选择性高达100%。首次用贱金属铁用于甘油氧化反应, 并有较好的活性, 从成本和产量的角度看具有很好的工业用途, 但催化剂制备繁琐。Wang X等[32]将过渡金属的磺酸盐席夫碱配合物插入Mg-Al 层状双氢氧化物(LDHs)中制备催化剂。研究发现, 以LDH为主体的络合催化剂对甘油氧化反应非常有效。用LDH-[Cr(SO3-salphen)]催化甘油反应, 在0.4 mol· L-1的甘油溶液25 mL、3%的过氧化氢25 mL、常压和60 ℃的条件下反应6 h后, 甘油转化率可以达85.0%, 二羟基丙酮选择性为56.5%。并且催化剂能够循环利用10次以上。载体上负载的配合物及反应条件对甘油氧化反应的作用比较明显。
均相催化剂有很好的活性, 但制备过程繁琐, 反应后续处理复杂, 不易回收。近年来, 在负载型催化剂作用下, 通过氧气氧化甘油生成二羟基丙酮引起广泛关注。甘油结构上有两种不同的羟基官能团, 不同的催化剂在不同的反应条件下对伯羟基和仲羟基的选择性也不同。因此可用不同的负载型催化剂来选择性催化甘油, 从而得到需要的下游产物。
2.1.1 单金属负载型催化剂
Demirel-Gulen S等[34]以Au/C为催化剂, 在1.5 mol· L-1甘油溶液100 mL、甘油与Au物质的量比3 500、NaOH与甘油物质的量比2、氧气压力1 MPa、温度50 ℃和转速1 500 r· min-1的条件下催化氧化甘油生成二羟基丙酮, 甘油转化率为30%, 二羟基丙酮选择性为20%。炭黑载体比活性炭或石墨对反应有更高的活性, 金颗粒的大小在反应中作用明显, 而且碱浓度对反应机理和催化剂选择性起重要作用。Rodriguez E G等[35]用硝酸改性Au/AC催化剂后催化氧化甘油。在NaOH与甘油物质的量比2、氧气压力0.3 MPa、0.3 mol· L-1甘油溶液150 mL、催化剂0.7 g、转速1 000 r· min-1和40 ℃下反应2 h, 二羟基丙酮最高转化率达22%。用含氧基团对催化剂进行改性, 结果表明, 含氧基团是反应中影响较大的因素, 使得金催化剂的活性增强。
Lei J等[36]研究发现, 以Pt/CNTs催化剂催化甘油过程中, 催化剂颗粒大小对反应影响较大。甘油氧化转化频率随催化剂颗粒的粒径从1.5 nm增大到2.5 nm而逐渐增大, 最大达到1 000 h-1, 继续增加催化剂颗粒粒径, 转化频率呈下滑趋势, Pt催化剂的最优粒径为2.5 nm。Lei J等[37]在非碱性条件下, 将Pt负载在活性炭上作催化剂, 在0.1 g· cm-3甘油溶液30 mL、甘油与Pt物质的量比890、氧气流量150 cm3· min-1、60 ℃和转速1 200 r· min-1的条件下反应6 h, 甘油转化率为18.8%, 二羟基丙酮选择性为15.7%, 随着甘油转化率增加, 二羟基丙酮选择性呈下降趋势。Liu S S等[38]利用沉淀法在不同氧化物载体上负载Au, 比较了加碱与不加碱对反应的影响。结果表明, 在NaOH作用下, 二羟基丙酮选择性有所下降, 在无碱条件下以Au/CuO为催化剂、反应温度40 ℃、甘油与Au物质的量比50和氧气压力30 MPa的条件下反应10 h后, 甘油转化率为90.7%, 二羟基丙酮选择性为82.5%。表明无碱条件利于金催化剂催化甘油。柯义虎等[39]也研究了在无碱条件下, 不同氧化物载体对负载型Au催化剂在甘油氧化生成二羟基丙酮反应中催化性能的影响。在80 ℃、氧气初始压力6 MPa、0.1 mol· L-1甘油溶液、甘油和金的物质的量比为100条件下反应2 h, 发现Au/CuO催化剂的活性最好, 甘油转化率为88.8%, 二羟基丙酮选择性为82.6%。催化剂Au/CuO表面的积炭和Cu价态的变化也会造成活性降低。Au/ZnO也有较好的催化活性和较高的二羟基丙酮选择性。循环使用后, 催化活性迅速下降。这主要是反应过程中Zn逐渐流失从而造成结构变化。无碱条件下将Au负载在CuAlO复合物上进行甘油催化氧化反应, 甘油转化率达76.7%, 二羟基丙酮选择性达97.3%, 随着载体中Cu含量降低, 甘油转化率先增后减。Au/CuAlO催化剂在3次重复利用后活性下降较明显, 甘油转化率由76.7%降到7.9%, 二羟基丙酮选择性随之下降。相同的活性组分在不同的条件下, 表现出不同的活性和选择性。表明影响反应的不仅是催化剂, 实验条件对反应的影响也较大。不同载体负载的催化剂, 其性能也有很大差异。雒京等[9]将磺化Salen配体插入水滑石层板间, 用金属离子配合磺化Salen配体得到催化剂, 并在甘油氧化反应中考察其活性。发现含Cu2+离子的催化剂对甘油脱氢有利, 对二羟基丙酮有较高选择性。在60 ℃和pH为7的条件下反应4 h, 甘油转化率达40.3%, 二羟基丙酮选择性达52.9%。第5次循环使用时, 甘油转化率为20.1%, 二羟基丙酮选择性为36.9%, 催化性能下降。
不同负载型单金属催化剂上甘油转化率和二羟基丙酮选择性见表1。单金属负载型催化剂用于甘油催化氧化合成二羟基丙酮反应中, 甘油转化率和二羟基丙酮产率都较低, 而且重复利用性能也差, 但负载型单金属催化剂的研究为后续开发新的催化剂提供了参考和依据。
| 表1 不同单金属负载型催化剂上甘油转化率和二羟基丙酮选择性 Table 1 Glycerol conversion anddihydroxyacetone selectivity on different single metal supported catalysts |
2.1.2 双金属负载型催化剂
Hu W等[46]通过分步浸渍法将Pt-Bi负载在Darco颗粒碳制备催化剂, 在半间歇反应器中研究甘油选择性氧化生成二羟基丙酮。研究了不同金属负载量、载体、催化剂制备方法、Pt和Bi的负载顺序对反应的影响。确定最佳催化剂为质量分数3%的Pt和0.6%的Bi负载于(20~40)目Norit Darco活性炭。催化剂最佳反应条件为初始pH=2、80 ℃和0.2 MPa。在此条件下, 甘油选择性达80%, 二羟基丙酮最大产率为48%。Demirel S等[47]用0.8%Au-0.2%Pt/C作催化剂, 在常压、1.5 mol· L-1甘油溶液150 mL、甘油与Au物质的量比20 000、保持pH=12、氧压1 MPa、转速500 r· min-1和60 ℃的条件下, 甘油转化率达到50%时, 二羟基丙酮选择性为36%。研究了碳载体孔体系对催化剂性能的作用。碳载体依赖于孔隙结构对催化剂活性产生重要影响。此外还发现, 铂能够改善单金属金催化剂活性, 说明第二种金属的加入严重影响催化剂的作用效果。
谢艳丽等[48]研究发现, 将Bi掺入到Pt/C催化剂中, 对甘油氧化生成二羟基丙酮有利。当Pt质量分数为9%、Bi质量分数为5%时, 催化剂活性较好。用空气氧化甘油在55 ℃下反应50 h、甘油全部转化, 二羟基丙酮选择性达50.05%。梁丹等[49]研究发现, 添加适量的Bi能够改善催化剂性能, 有利于提高二羟基丙酮选择性。Pt-5%Bi/C催化剂的活性最高, 甘油转化率为91.5%, 二羟基丙酮选择性为49.0%。研究还发现, 对于Pt-Bi/S-MWNTs和Pt-Sb/S-MWNTs催化剂, 反应起始二羟基丙酮选择性较高, 在60 ℃、氧气流量150 mL· min-1的条件下, 甘油转化率为10%时, 二羟基丙酮选择性分别为86.7%和80.8%。随着甘油不断转化, Pt-Bi/S-MWNTs催化剂上二羟基丙酮选择性大幅度下降, 甘油转化率达到90%时, 二羟基丙酮选择性只有35.6%。根据表征结果, Bi和Sb的加入使得Pt在碳纳米管载体上更好的分散。但与Pt的结合方式则大不相同。Sb与Pt结合形成均匀的金属相, 而Bi则是分散到Pt的晶体结构内部, 变为双金属合金。催化剂性能的改变很可能是由结构变化引起的。周洁等[50]将Bi-Pt双金属负载到H-mordenite上催化甘油合成二羟基丙酮。研究显示, 催化剂比表面积对催化性能影响不明显。催化剂为1%Bi-5%Pt/H-mordenite时, 在80 ℃、甘油(水-乙醇1:1混合溶液的质量分数为10%)和空气流量 20 mL· min-1的最优条件下反应(2~4) h, 甘油转化率达到70.6%, 二羟基丙酮选择性高达 61.0%。使二羟基丙酮选择性升高的原因可能是由于H-mordenite抑制了甘油的裂解。王增龙等[51]将5%Pt-7%Bi负载到镁铝水滑石上作催化剂, 在70 ℃和氧气流速150 mL· min-1的条件下反应6 h, 甘油转化率只有25.1%, 二羟基丙酮选择性为80.6%。不同载体对产物影响较大, 不同条件下产物分布不同, 而且载体的酸碱性对产物分布也有明显影响。Liang L等[52]研究发现, Bi与Pt物质的量比不同, 则Bi对Pt颗粒的包裹程度也不同, Bi在Pt颗粒表面的附着体现了Bi助剂的空间位阻作用, 进而改变了Pt-Bi/C催化剂性能。在0.1 g· mL-1的甘油溶液50 mL, 60 ℃和氧气流速150 mL· min-1的条件下, 浸渍法得到的5.0%Pt-5.0%Bi/C催化剂性能最优, 反应6 h后, 甘油转化率可达到91.5%, 二羟基丙酮选择性为49%。
Hirasawa S等[53]考察了炭黑负载的Pd-Ag催化剂(总负载质量分数2%)催化氧化甘油合成二羟基丙酮。研究发现, 在加入玻璃内衬的不锈钢高压反应釜中、0.3 MPa氧气、80 ℃、转速500 r· min-1和pH=6的条件下, 羟基乙酸会对反应造成影响。加入羟基乙酸会使甘油转化率和二羟基丙酮选择性下降。当Pd与Ag原子比1, 不加入羟基乙酸时, 催化性能最优, 甘油转化率为20%, 二羟基丙酮选择性为82.2%。表明溶剂的加入会在一定程度上影响催化剂的催化效果。Claus S等[47]在Au催化剂的基础上添加助剂金属Pt后, 提高了Au-Pt/C催化剂活性, 在150 mL的1.5 mol· L-1甘油溶液、甘油与Au物质的量比20 000、pH=12、氧气压力1 MPa和转速500 r· min-1的条件下, 0.8% Au-0.2%Pt/C催化剂催化氧化甘油, 甘油转化率为50%时, 二羟基丙酮选择性从26%增加到36%。助剂Pt的加入对反应有促进作用。Brett G L等[54]将1%Au-3%Pt负载于MgO载体, 在甘油与Pt物质的量比为1 000、氧气压力0.3 MPa和温度23 ℃下反应24 h后, 甘油转化率为42.5%, 但主要产物为甘油酸, 对仲羟基选择性下降。第二金属的加入不一定都是促进作用, 还要根据实际需要的结构和性质进行选择。
Bi的加入使得双金属催化剂比单金属有更好的反应活性。研究者也对其他金属进行了考察, 如Pt、Sb、Au和Pd等。效果最明显的还是Bi对催化剂的改性。双金属催化剂是继单金属催化剂的深入研究, 是单金属的二次利用。不同双金属负载型催化剂上甘油转化率和二羟基丙酮选择性见表2。
| 表2 不同双金属负载型催化剂上甘油转化率和二羟基丙酮选择性 Table 2 Glycerol conversion anddihydroxyacetone selectivity on different bimetallic supported catalysts |
2.1.3 三金属负载型催化剂
谢艳丽等[48]将其他金属掺杂到Pt-Bi催化剂中, 制备出不同的三金属负载型催化剂(Pt-Ag-Bi/C、Pt-Pd-Bi/C和Pt-Au-Bi/ C), 并在甘油氧化反应考察催化活性。结果表明, 相比Bi-Pt/C双金属催化剂, 三金属催化剂反而使甘油转化率下降, 二羟基丙酮产率下降。以3%Pt-3%Ag-4%Bi/C作催化剂时, 二羟基丙酮选择性可达100%, 甘油转化率和二羟基丙酮产率却只有0.25%。3%Pt-8%Au-11%Bi/C催化剂作用下, 二羟基丙酮选择性只有68.31%, 甘油转化率只有22.87%, 相比双金属催化剂表现出很大程度的下降。Au的催化活性受到酸性条件的抑制, 导致三金属催化剂整体反应活性较低。Villa A等[43]将Bi渗入到Au-Pt中形成的三金属催化剂(Bi-Au Pt/AC), 在非碱性条件下考察了甘油选择性催化氧化的效果。发现Bi的添加明显改变了Au-Pt双金属催化剂对甘油的选择性, 恒温玻璃反应器中, 在甘油与金属物质的量比500、氧气压力0.3 MPa和温度80 ℃的条件下, 当甘油转化率达到60%时, 二羟基丙酮选择性达到63%。有效的提高了催化剂稳定性, 使其在高转化率下大大改善了二羟基丙酮选择性。Pt基催化剂在反应中很容易发生氧中毒, 氧气压力越大, 催化剂越容易失活。因此, 在催化氧化甘油时, 负载型Pd和Pt催化剂很容易失活。相比Pt基催化剂, Au催化剂能承受的氧分压相对大, 即便是在0.3 MPa下的纯氧中进行反应也不会失去活性。说明金属修饰有一定的促进作用, 但不是越多越好, 三金属反而使得活性下降, 为后续研究修正了研究方向。
2.1.4 催化剂作用机理
目前, 对于甘油氧化反应过程中催化剂的作用机理主要有以下三种观点:
(1) 空间位阻效应:Gallezot P等[55]认为助剂Bi覆盖在Pt纳米颗粒的表面阻碍了催化剂由于副产物的不可逆吸附而引起的中毒, 从而提高了Pt-Bi催化剂的催化活性和二羟基丙酮选择性。Mallat T[56]和Besson M[57]等认为醇在仲羟基氧化过程的副产物及其不可逆吸附导致了催化剂失活; 附着在Pt纳米颗粒表面的Bi助剂金属, 减少了Pt金属表面的活性位点数目, 进而抑制了催化剂的中毒。Worz N[58]和Hu W[59]等考察了甘油催化氧化中的Pt-Bi/C失活原因, 发现氧化生成的甘油酸等副产物吸附在催化剂颗粒的表面导致催化剂中毒, 与Kimura H、Gallezot P等所描述的相一致。然而在Pt/C催化剂中加入Bi依然有失活的迹象, 而且容易使二羟基丙酮发生氧化, 甚至断裂C— C键生成C1和C2等产物。这一点在Nie R等[40]的研究中也曾提到, 认为Bi容易偏析到催化剂的表面和含氧基团共同作用后以Bi2O3附着在Pt颗粒的表面导致Pt和Bi分离, 使得催化剂中毒。Ning X等[60]认为液相中的Bi离子对二羟基丙酮选择性有作用。在Pt-Bi/C反应后的溶液中也发现有Bi离子。反应开始时, 大部分的Bi离子在催化剂的表面吸附, 随着时间的增加, 生成的副产物甘油酸不断积累, 催化剂表面的Bi离子又浸出到溶液中, 处于动态的吸脱附平衡。
(2) Pt-Bi-OH氧化活性位:Besson M等[55, 57]还提出一种观点, 认为Bi原子吸附的氧可能在催化剂表面形成了Pt-Bi-OH活性物种, 该物种作为另一种活性中心催化氧化吸附的甘油分子, 不但加快了反应速率, 还改善二羟基丙酮的选择性。由于金属Bi与氧有较强的亲和性, 使得醇在氧化过程中催化剂的还原电势降低, 防止二羟基丙酮发生深度氧化。
(3) PtBi2合金活性位:谢艳丽等[48]推测金属Pt和助剂Bi形成的PtBi2化合物也可能是甘油氧化的活性位。认为这种结构容易使得甘油仲羟基O— H断键, 形成一个吸附态的醇氧负离子和氢离子。在醇氧负离子作用下, 仲碳上的C— H键优先断裂, 形成二羟基丙酮分子, 并产生一个氢负离子。吸附氧和氢负离子形成水, 将平衡推向二羟基丙酮的生成方向。Nie R等[40]发现在Pt/CNTs催化剂中加入助剂Sb, 会形成PtSb合金纳米粒子。Sb作为助剂能有效的发挥其空间活性位阻作用, 散布在Pt纳米颗粒的晶格中, 形成双金属活性位有效的抑制中间产物发生深度氧化。大大提高了甘油催化氧化反应的活性、改变了二羟基丙酮选择性, 且抑制了二羟基丙酮的进一步氧化。
总体来说, 甘油氧化反应会随着催化剂和反应条件的变化而变化, 对该反应的机理都是根据反应得到的结果进行猜想或推论, 并没有达成一致性结论。所以有必要进一步深入考察甘油氧化反应过程中催化剂的微观结构所起的作用, 进而提出合理的反应机理, 为催化剂研究提供更可靠的依据。
负载型金属催化剂在甘油氧化过程中表现出好的催化效果, 但大多都是贵金属, 而且单金属负载时效果差, 要想获得高的转化率和选择性就需另一种金属对其改性。贵金属负载催化剂会提高生产成本, 不利于工业化生产。相比金属催化剂, 非金属催化剂的成本较小。周洁等[61]用等体积浸渍法制得H3PW12O40/SiO2催化剂, 在固定床反应器上测试
将不同的负载型催化剂用于甘油选择性催化氧化生成二羟基丙酮的反应中, 从均相到非均相催化, 从单金属到双金属负载催化, 从金属到非金属催化, 甘油氧化反应的研究不断在完善。研究过程中对不同催化剂以及反应条件进行优化, 讨论影响反应活性的因素。发现用Bi改性的Pt负载催化剂可以有效地将甘油选择性催化氧化成二羟基丙酮, 在最优条件下, 可获得较高的甘油转化率和二羟基丙酮选择性, 但催化剂稳定性较差, 有待进一步提高。为了降低催化剂成本, 寻找适合工业化生产的催化剂, 对非金属催化剂也进行了研究, 同样存在稳定性差, 失活较快的现象, 改善催化剂的稳定性将是未来研究要解决的问题之一。虽然目前对甘油氧化生成二羟基丙酮的催化剂和反应条件进行了大量研究, 为该过程的研究提供了参考, 但对催化机理缺乏清楚的认识, 很难实现工业化生产。因此要对该过程中的催化作用机理, 反应条件以及催化剂的性能进行深入的研究, 这将是未来甘油氧化的发展方向。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [51] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|
| [61] |
|
| [62] |
|