作者简介:段兆磊,1982年生,男,黑龙江省大庆市人,工程师,研究方向为化学工艺。
将Pd纳米片(Pd NSs)负载到石墨相氮化碳纳米片(CNNSs)表面,制备了Pd NSs/CNNSs催化剂,并采用透射电镜、X射线衍射、红外光谱和X射线光电子能谱对催化剂进行表征。结果表明,Pd NSs和CNNSs通过面面接触,形成紧密接触界面。负载后,Pd NSs具有较高分散性,没有发生明显团聚。将Pd NSs/CNNSs用于催化4-硝基苯酚还原生成4-氨基苯酚。结果表明,Pd NSs/CNNSs能够高效催化4-硝基苯酚还原。室温下,在Pd NSs/CNNSs催化剂、4-硝基苯酚和NaBH4浓度分别为2.1 mg·L-1、0.14 mmol·L-1 和 20 mmol·L-1的条件下,反应速率常数达0.154 min-1,是以Pd NSs为催化剂时的1.77倍。
Pd NSs/CNNSs catalyst was synthesized by Pd nanosheets (Pd NSs) supported onto the surface of graphitic carbon nitride nanosheets (CNNSs) and characterized by transmission electron microscopy,X-ray diffraction,infrared spectroscopy and X-ray photoelectron spectroscopy.The results showed that an intimately contacted interface between Pd NSs and CNNSs was formed through face-to-face contact.Pd NSs showed high dispersion after supporting,and no obvious agglomeration could be found.Pd NSs/CNNSs were employed for catalytic reduction of 4-nitrophenol (4-NP) to 4-aminophenol (4-AP).The results showed that Pd NSs/CNNSs could effectively catalyze the reduction of 4-NP.Under the conditions of room temperature,2.1 mg·L-1 of Pd NSs/CNNSs,0.14 mmol·L-1 of 4-NP and 20 mmol·L-1 of NaBH4,the reaction rate constant reached 0.154 min-1,which was 1.77 times higher than that obtained over unsupported Pd NSs.
以石墨烯为代表的二维纳米片具有特殊的物化和电子性能, 被广泛应用于催化领域[1]。然而石墨烯对大多数化学反应没有催化活性。受石墨烯的启发, 贵金属纳米片引起广泛关注[2]。贵金属纳米片表面原子含量高, 表面原子处于配位不饱和态。在催化反应中这些原子的催化活性远高于体相结构中的原子[3]。因此, 与传统催化剂相比, 贵金属纳米片具有更为优异的催化性能。
近年来开发了多种制备贵金属纳米片的方法[4]。然而高昂的价格和较差的稳定性限制了贵金属纳米片在催化中的应用。以CO限域生长法制备的钯纳米片(Pd NNs)为例, 当Pd NNs置于空气中时会被氧化, 并降解为纳米颗粒[5]。提高贵金属纳米片催化活性和稳定性有多种方法。如在Pd NNs表面包覆一层聚乙炔, Pd NNs表面变为疏水[6]。在催化反应中, 疏水处理有利于吸附疏水性反应物, 脱附亲水性产物, 从而提高催化活性。并且, 表面的聚乙炔可避免Pd NNs烧结和团聚, 提高其稳定性。但该方法过程复杂, 难于大规模应用。
将金属纳米粒子负载于多孔载体可提高其稳定性, 但该方法不适用于纳米片, 因为纳米片尺寸太大, 不能进入到载体的微孔和介孔孔道中[7]。与多孔载体相比, 纳米片具有大得多的可利用表面积。如将Pd NNs负载到TiO2纳米片表面, Pd NNs的稳定性将大幅提高[8]。
目前, 大多数催化剂载体都是无机化合物。与无机载体相比, 有机载体含有大量的功能基团。这些功能基团可有效稳定贵金属纳米片[9]。石墨相氮化碳(g-C3N4)是一种二维有机材料, 被广泛用作催化剂和催化剂载体[10]。通过液相剥离可制备超薄g-C3N4纳米片(CNNSs)[11]。CNNSs含有大量的表面氮原子。这些氮原子可与纳米片中的贵金属原子形成配位。CNNSs的配位作用可调控贵金属原子的电子效应, 并提高其稳定性[12]。
本文将Pd NSs负载到CNNSs表面, 制备Pd NSs/CNNSs催化剂。采用透射电镜、X射线衍射、红外光谱、X射线光电子能谱对催化剂进行表征, 并考察其催化4-硝基苯酚还原性能。
乙酰丙酮钯(99%), 聚乙烯吡咯烷酮(MW=30000)和NaBr (分析纯), Alfa-Aesar公司; N, N-二甲基甲酰胺和NaBH4, 分析纯, 阿拉丁试剂公司; 脲、4-硝基苯酚、盐酸(37%)、丙酮和无水乙醇, 分析纯, 国药集团化学试剂有限公司。
日本电子公司JEM-2011型透射电镜; 日本理学公司D/max 2500型X射线粉末衍射仪; 德国布鲁克公司TENSOR-27傅里叶红外光谱仪; 英国VG科学仪器公司ESCALAB220I-XL型X射线光电子能谱仪; 日本岛津公司UV-2600紫外可见分光光度计。
以脲为前驱体制备CNNSs。将20 g 脲加入带盖的陶瓷坩埚中, 置于马弗炉550 ℃加热4 h, 冷却至室温, 得到淡黄色固体。将1 g所得产物分散于10 mL的0.5 mol· L-1盐酸溶液中, 搅拌0.5 h, 过滤、洗涤、真空干燥后得到载体CNNSs。
Pd NSs通过CO限域生长法制备。将7.5 mg 的乙酰丙酮钯、25 mg的聚乙烯吡咯烷酮和30 mg的NaBr加入到50 mL 含有3 mL的 H2O 和6 mL的 N, N-二甲基甲酰胺的不锈钢高压反应釜中。氮气置换3次后充入1.0 MPa的CO, 80 ℃反应2 h。冰水浴下冷却至0 ℃, 加入10 mL丙酮, 离心分离。将所得产物用乙醇和丙酮混合溶剂洗涤3次, 真空干燥, 得到Pd NSs。
Pd NSs/CNNSs的制备。将50 mg 的CNNSs和2.5 mg 的Pd NSs分别分散于50 mL和10 mL的H2O中, 超声10 min。搅拌下, 将Pd NSs分散液缓慢滴入CNNSs分散液中, 搅拌10 min 后超声0.5 h。将所得产物离心分离, 乙醇洗涤3次后真空干燥, 得到催化剂Pd NSs/CNNSs。
反应体系中Pd NSs/CNNSs、4-硝基苯酚和NaBH4浓度分别为2.1 mg· L-1, 0.14 mmol· L-1和20 mmol· L-1。50 μ L的NaBH4 溶液(1 mol· L-1)加至含有2.5 mL浓度为0.14 mmol· L-1的4-硝基苯酚溶液的比色皿中。 然后加入50 μ L的催化剂分散液(109.2 mg Pd· L-1)开始反应。用紫外可见分光光度计监控反应过程。
图1为CNNSs、Pd NSs和Pd NSs/CNNSs的TEM照片。由图1可见, CNNSs为薄片结构。弯曲的边缘有利于降低表面能, 提高稳定性[13]。Pd NSs为六角片状结构, 直径约为50 nm。将Pd NSs与CNNSs混合, 由于静电和配位作用, Pd NSs负载到CNNSs表面。Pd NSs与CNNSs通过面面接触, 形成二维/二维大面积接触界面。负载后Pd NSs具有较高的分散性, 没有发生明显的团聚。大接触界面增强了Pd NSs与CNNSs之间的相互作用, 提高了材料的稳定性[14]。CNNSs表面的含N功能基团作为配位点, 改善了Pd原子的电子结构, 可提高其催化性能。
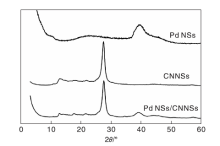
图2为CNNSs、Pd NSs和Pd NSs/CNNSs的XRD图。由图2可以看出, Pd NSs 在40.0° 有一明显衍射峰, 对应于Pd(111)晶面。CNNSs在13.3° 和27.4° 处的衍射峰分别对应于100和002晶面[15]。Pd NSs/CNNSs 同时具有Pd NSs 和CNNSs的衍射峰, 表明Pd NSs 成功负载到CNNSs表面。
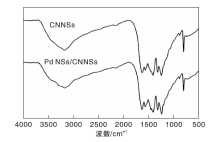
图3是CNNSs和Pd NSs/CNNSs的FT-IR谱图。从图3可以看出, CNNSs和Pd NSs/CNNSs差别不大。在808 cm-1处的尖峰为三嗪单元的弯曲振动, (1 200 ~ 1 650) cm-1为CN杂环的伸缩振动, (3 000~3 600) cm-1的宽峰为N— H和O— H的伸缩振动[16]。N— H和O— H来自CNNSs中的缺陷和表面功能基团。缺陷和表面功能基团是Pd原子的配位中心, 可改善Pd原子的电子结构, 提高其催化活性和稳定性。
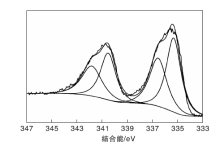
采用XPS对Pd NSs/CNNSs中Pd的化学态进行分析, 结果如图4所示。由图4可知, Pd 3d5/2 XPS波谱可分为两个峰, 335.3 eV归属于零价Pd, 336.5 eV归属于PdO[17]。PdO的摩尔分数达到43%, 说明Pd NSs表面原子含量高。表面Pd原子容易氧化成PdO。
Pd NSs和Pd NSs/CNNSs催化4-硝基苯酚还原生成4-氨基苯酚性能如图5所示。400 nm处的最大吸收用于测量4-硝基苯酚浓度。无催化剂时, 该反应不发生[18]。从图5可以看出, 以Pd NSs为催化剂时, 随着反应的进行, 400 nm处的吸收强度逐渐下降, 表明4-硝基苯酚的浓度下降。同时, 298 nm处产生一新峰, 该峰归属于产物4-氨基苯酚的UV-vis吸收[19]。表明4-硝基苯酚被还原为4-氨基苯酚。反应体系中, NaBH4浓度远大于4-硝基苯酚浓度。因此可以认为反应过程中NaBH4浓度不变, 反应速率常数可通过ln(C/C0)=-kt计算。
其中, C0是4-硝基苯酚的初始浓度, C是反应时间t时的浓度。以Pd NSs为催化剂时, 反应速率常数为0.087 min-1。考虑到Pd NSs的浓度较低, 因此, Pd NSs具有较高的催化4-硝基苯酚还原活性。Pd NSs/CNNSs具有更高的催化活性, 反应速率常数为0.154 min-1, 是Pd NSs的1.77倍。反应8 min后, 以Pd NSs为催化剂时, 4-硝基苯酚转化率为49.5%; 以Pd NSs/CNNSs为催化剂时, 4-硝基苯酚转化率达到71.3%。负载后Pd NSs催化性能显著提高, 这主要归因于CNNSs的载体效应。CNNSs含有大量的含N表面功能基团, 这些功能基团作为Pd原子的配位点, 改善了Pd的电子结构。
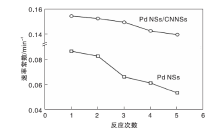
Pd NSs和Pd NSs/CNNSs催化剂稳定性如图6所示。从图6可以看出, 反应5次后, 以Pd NSs为催化剂时, k值由0.087 min-1降到0.053 min-1, 催化活性下降了39.1%, 表明Pd NSs的稳定性较差。Pd NSs的纳米尺寸和较高配位不饱和原子含量是其稳定性较差的主要原因。以Pd NSs/CNNSs催化剂时, k值由0.154 min-1降到0.139 min-1, 催化活性下降了9.7%, 表明负载后Pd NSs的稳定性大幅度提高。CNNSs中氮原子的载体效应是Pd NSs稳定性提高的主要原因。用N原子修饰的石墨烯负载金属纳米粒子后, 金属纳米粒子的稳定性显著提高[20]。CNNSs的N含量远高于N修饰的石墨烯。因此, CNNSs负载后的Pd NSs稳定性大幅提高。
(1) 将Pd NSs负载到CNNSs表面, 制备了Pd NSs/CNNSs催化剂, CNNSs与Pd NSs通过面面接触, 形成紧密接触界面。负载后, Pd NSs具有较高的分散性, 没有发生明显团聚。
(2) 室温下, 以Pd NSs/CNNSs为催化剂, 在Pd NSs、4-硝基苯酚和NaBH4的浓度分别为0.1 mg· L-1, 0.14 mmol· L-1和 20 mmol· L-1的条件下, 反应速率常数为0.154 min-1, 是以未负载的Pd NSs为催化剂时的1.77倍。
(3) 负载后, Pd NSs的稳定性显著提高。反应5次后, Pd NSs/CNNSs为催化剂活性仅下降了9.7%。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|