作者简介:张 明,1971年生,男,高级工程师,主要从事尼龙中间体的研发工作。
以环己烯为原料,采用Zn-CH3COOH为还原剂,经臭氧氧化和还原分解得到1,6-己二醛。讨论溶剂种类、溶剂用量、反应温度、氧气流量、氧化反应时间、还原剂种类、还原分解时间、还原剂用量对环己烯臭氧化合成1,6-己二醛反应的影响。得到较佳反应条件(以0.05 mol 环己烯计)为:采用冰乙酸和1,2-二氯乙烷混合溶剂,冰乙酸6 g,1,2-二氯乙烷30 mL,臭氧化温度(0~5) ℃,O2流量(100~200) mL·min-1,臭氧化反应时间180 min,活化锌粉为还原剂, n(锌粉) : n(环己烯)=1:1,还原分解时间60 min。在该反应条件下,重复实验三次,1,6-己二醛平均收率可达61.6%。
1,6-adipoaldehyde was synthesized by ozone oxidation and reduction decomposition using cyclohexene as material,Zn-CH3COOH as reducing agent.The effects of solvent,amount of solvent,reaction temperature,flowrate of oxygen,ozonization time,reducing agent,restore decomposition time,and amount of reducing agent were investigated.The appropriate reaction conditions (based on 0.05 mol cyclohexene) were that mixture of aceticacid and sym-dichloroethane was solvent,amount of aceticacid was 6 g,amount of sym-dichloroethane was 30 mL,reaction temperature was (0-5) ℃,flowrate of oxygen was (100-200) mL·min-1,ozonization time was 180 min,activated zinc powder was reducing agent, n(zinc powder): n(cyclohexene)=1:1,restore decomposition time was 60 min.Under the above conditions,1,6-adipaldehyde average yield of three times of eartion was about 61.6%.
1, 6-己二醛是一种高效化学杀菌剂, 广泛用于医疗器械、食品器具、禽畜栏舍等的消毒灭菌; 用于石油开采, 抑制硫酸盐还原菌活性; 作为交联剂用于皮革处理、生物组织和人体器官的粘合与修复[1]。
对于1, 6-己二醛的制备, 国内报道较少[2], 国外文献较多, 其中, 1, 2-环己二醇氧化制备1, 6-己二醛的收率较高[3]。烯烃臭氧化反应可使不饱和烯烃氧化裂解为羰基氧化物和羰基化合物, 再经过相应的重排、分解得到醛、酮、酸或酯。臭氧具有氧化能力强、选择性好、反应速度快等优点, 且反应结束后可自行分解, 无污染, 是一种“ 干净” 的氧化剂, 符合当今绿色化工的发展趋势[4]。
本文以环己烯为原料, 臭氧为氧化剂, Zn-CH3COOH为还原剂, 经臭氧化-还原分解制备1, 6-己二醛, 研究1, 6-己二醛的合成工艺。
HD-10氧气型臭氧发生器, 珠海银河发展有限公司; DFY恒温低温反应浴, 巩义市予华仪器有限公司。环己烷、乙酸乙酯、四氯化碳、乙腈, 均为分析纯, 天津市风船化学试剂科技有限公司; 环己烯, 工业品, 中国神马集团有限责任公司; 1, 2-二氯乙烷, 分析纯, 天津市科密欧化学试剂有限公司; 冰乙酸, 分析纯, 天津市化学试剂三厂; 锌粉, 分析纯, 天津市凯通化学试剂有限公司; 甲苯, 分析纯, 派尼化学试剂厂; 溴素, 分析纯, 国药集团化学试剂有限公司。
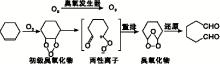
根据相关文献[5, 6], 环己烯臭氧化合成1, 6-己二醛的反应过程如图1所示。环己烯和臭氧反应生成初级臭氧化物, 初级臭氧化物不稳定, 分解成两性离子, 经重排得到臭氧化物中间体, 最后还原得到1, 6-己二醛。
向装有温度计、通气管、冷凝管和磁力搅拌的三口烧瓶中加入一定量的环己烯和有机溶剂, 放入低温反应浴中, 搅拌至温度为0 ℃。调节O2流量, 开启臭氧发生器, 通入O3/O2进行氧化反应。尾气先经KI溶液吸收未反应完全的臭氧, 再通过冰乙酸回收环己烯和有机溶剂。
氧化结束后通2 min N2排除多余的O3/O2, 臭氧化合物不经分离直接进入还原反应。在装有温度计、直形冷凝管、恒压滴液漏斗和电磁搅拌的三口烧瓶中加入一定量的活化锌粉、蒸馏水, 滴加臭氧化合物进行反应, 在N2保护下搅拌一定时间。待反应结束, 抽滤除去未完全反应的锌粉, 反应液转入分液漏斗中静置分层, 得到有机相和无机相。无机相中加入一定体积的1, 2-二氯乙烷进行萃取, 萃取三次, 合并有机相, 水洗2次除去无机盐, 加入一定量的无水硫酸钠干燥, 过滤后旋蒸除去1, 2-二氯乙烷, 减压蒸馏得产品, 称重。
1.4.1 产品组分含量分析方法
采用上海科创色谱仪器有限公司GC-9800TFP气相色谱分析产品组分含量, SE-30毛细管柱(30 m× 0.32 mm× 0.25μ m), 柱箱温度80 ℃, 汽化室温度250 ℃, FID检测器温度250 ℃, 80 ℃ 保温 4 min, 20 ℃· min-1升至200 ℃, 保温2 min。
1.4.2 产品表征
采用东南科创科技有限公司NAR-1T型阿贝折光仪测定产品折光率。
采用美国Nicolet公司10 DX-FTIR型傅立叶变换红外光谱仪表征产品的红外光谱。
采用德国Bruker公司AVⅡ -400型核磁共振仪表征产品氢谱、碳谱。
采用日本岛津公司GPC-GCMS气质联用分析仪测定1, 6-己二醛的质谱图。
产品折光率测定结果
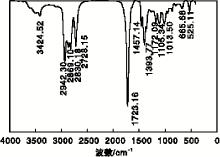
图2为产品的FT-IR谱图。由图2可知, 2 942.30 cm-1、2 869.10 cm-1处的峰归属为-CH2中C— H伸缩振动吸收峰, 2 830.18 cm-1、2 728.15 cm-1处的峰归属为羰基的C— H伸缩振动峰, 1 723.16 cm-1处强吸收峰为羰基的特征吸收峰, 1 457.14 cm-1处中等强度吸收峰为-CH2中C— H变形振动峰, 1 393.77 cm-1处的峰归属为-CH2CO中C— H变形振动峰。
图3为产品的1H-NMR(CDCl3)谱图。由图3可知, δ (9.711~9.723)× 10-6出现的氢信号为-CHO结构中H1; 由于羰基电负性的影响, 信号向低场移动, 化学位移大, 故δ (2.422~2.457)× 10-6处为-CH2CO中的H2; δ (1.591~1.629)× 10-6处信号归属为对称性结构OH1C-CH22-CH32-CH32-CH22-CH1O中的-CH32CH22。
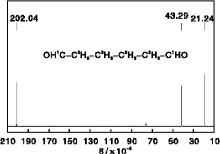
图4为产品的13C-NMR(CDCl3)谱图。由图4可知, 有3组信号, δ 202.04× 10-6处信号为-CHO上的C; -CH2-CHO中亚甲基C受羰基的影响, 故δ 43.29× 10-6处为与羰基相连的亚甲基C; 与羰基距离较远的C受羰基的影响较小, 故δ 21.24× 10-6处为与羰基距离较远的C。
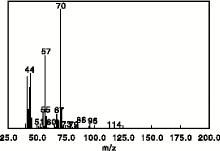
为了更确定合成出的产品为1, 6-己二醛, 采用气-质联用分析, 得到1, 6-己二醛的质谱图, 如图5所示, 与1, 6-己二醛标准质谱图一致。
2.2.1 溶剂种类
环己烯0.05 mol, O2流量140 mL· min-1, n(锌粉) : n(环己烯)=1: 1, 臭氧化温度(0~5) ℃, Br2/CCl4溶液确定反应终点, 考察溶剂种类对臭氧化反应的影响, 结果见表1。
| 表1 溶剂对环己烯臭氧化合成1, 6-己二醛反应的影响 Table 1 Effects of solvents on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
由表1可知, 采用环己烷溶剂时, 臭氧化效果差。采用冰乙酸或乙腈溶剂时, 因不能将产物从水相中很好的萃取出来, 收率较低。采用1, 2-二氯乙烷做溶剂时, 有微量聚合物, 1, 6-己二醛收率60.35%。采用乙酸和环己烷混合溶剂时, 有大量聚合物生成, 1, 6-己二醛收率仅5.53%。采用乙酸与1, 2-二氯乙烷混合溶剂时, 反应液粘度低, 臭氧气体在此溶剂中的分散效果好, 少量极性乙酸的存在使生成的臭氧化物稳定且可用于臭氧化物的还原分解, 1, 6-己二醛收率62.08%收率。综上, 选择乙酸和1, 2-二氯乙烷的混合物做溶剂。
2.2.2 乙酸用量
环己烯0.05 mol, O2流量140 mL· min-1, n(锌粉) : n(环己烯)=1: 1, 臭氧化温度(0~5) ℃, 蒸馏水20 mL, 1, 2-二氯乙烷35 mL, 还原反应1 h条件下, 考察乙酸用量对环己烯臭氧化合成1, 6-己二醛的影响, 结果见表2。
| 表2 冰乙酸用量对环己烯臭氧化合成1, 6-己二醛反应的影响 Table 2 Effects of acetic acid amount on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
由表2可以看出, 1, 6-己二醛收率随冰乙酸用量增加先升高后降低, 冰乙酸用量为4.5 g时, 1, 6-己二醛收率虽然比6 g时略高, 但反应结束后分层时, 油相有少量乳化。故冰乙酸用量宜选择6 g, 即n(冰乙酸) : n(环己烯)=2: 1。
2.2.3 溶剂用量
环己烯0.05 mol, 冰乙酸6 g, O2流量140 mL· min-1, n(锌粉) : n(环己烯)=1: 1, 臭氧化温度(0~5) ℃, 蒸馏水20 mL, 还原反应1 h条件下, 考察1, 2二氯乙烷用量对环己烯臭氧化合成1, 6-己二醛的影响, 以已选定的最佳冰乙酸用量与1, 2-二氯乙烷量混合溶剂与原料的体积比安排实验, 结果见表3。由表3可以看出, 随着溶剂用量的增加, 1, 6-己二醛收率增加并趋于稳定。溶剂用量增加, 环己烯浓度下降, 反应液粘度降低, 有利于反应的进行。当V(混合溶剂): V(环己烯)小于7: 1时, 产品收率较低, 继续增加溶剂用量, 1, 6-己二醛收率趋于稳定。因此选定溶剂用量7: 1为适宜配比, 即以0.05 mol环己烯计, 1, 2-二氯乙烷30 mL。
| 表3 溶剂用量对环己烯臭氧化合成1, 6-己二醛反应的影响 Table 3 Effects of solvent amount on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
2.2.4 臭氧化反应温度
环己烯0.05 mol计, 冰乙酸6 g, 1, 2-二氯乙烷30 mL, O2流量140 mL· min-1, n(锌粉) : n(环己烯)=1: 1, 蒸馏水20 mL, 还原反应1 h条件下, 考察反应温度对环己烯臭氧化合成1, 6-己二醛反应的影响, 结果见表4。
| 表4 反应温度对环己烯臭氧化合成1, 6-己二醛反应的影响 Table 4 Effects of reaction temperature on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
由表4可以看出, 低温有利于臭氧化反应, 但温度过低, 反应速率变慢, 需要大量的能量消耗, 臭氧化温度过高时臭氧分子易分解, 生成的臭氧化物不稳定。综合考虑, 选定较佳反应温度为(0~5) ℃。
2.2.5 O2流量
环己烯0.05 mol, 冰乙酸6 g, 1, 2-二氯乙烷30 mL, 臭氧化温度(0~5)℃, n(锌粉) : n(环己烯)=1: 1, 蒸馏水20 mL, 还原反应1 h条件下, 考察O2流量对环己烯臭氧化合成1, 6-己二醛的氧化反应时间、环己烯转化率、1, 6-己二醛收率的影响, 结果见表5。由表5可以看出, 随着O2流量增加, 1, 6-己二醛收率先增加后减少。O2流量增加, 臭氧产生量增大, 环己烯氧化时间减少, 反应剧烈。气流量增大造成溶剂挥发严重, 带走一定量的烯烃, 同时反应过于剧烈, 传质不够充分可能导致过氧化等副反应增加; O2流量过小, 反应时间延长, 同样造成原料损失及过氧化。因此, 在所选反应条件下, O2流量(100~200) mL· min-1比较合适, 优选O2流量140 mL· min-1, 既可以使环己烯达到较高的转化率又可避免过度氧化, 较好的控制反应终点。
| 表5 O2流量对环己烯臭氧化合成1, 6-己二醛反应的影响 Table 5 Effects of oxygen flow on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
2.2.6 氧化反应时间
环己烯0.05 mol, 冰乙酸6 g, 1, 2-二氯乙烷30 mL, 臭氧化温度(0~5)℃, O2流量140 mL· min-1, n(锌粉) : n(环己烯)=1: 1, 蒸馏水20 mL, 还原反应1 h条件下, 考察臭氧化时间对环己烯臭氧化合成1, 6-己二醛反应的影响, 结果见图6。
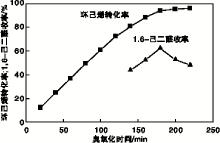 | 图6 臭氧化时间对环己烯臭氧化合成1, 6-己二醛反应的影响Figure 6 Effects of ozonization time on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
由图6可知, 氧化时间增加, 环己烯转化率逐渐增大, 臭氧化时间180 min时, 再继续增加氧化时间, 环己烯转化率增加缓慢。氧化时间增加, 1, 6-己二醛收率先增加后减小, 氧化时间180 min时达到最大值。故选择臭氧化时间为180 min。
2.2.7 还原剂种类
环己烯0.05 mol, 冰乙酸6 g, 1, 2-二氯乙烷30 mL, 臭氧化温度(0~5)℃, O2流量140 mL· min-1条件下, 考察还原剂对环己烯臭氧化合成1, 6-己二醛反应的影响, 结果见表6。
| 表6 还原剂对环己烯臭氧化合成1, 6-己二醛反应的影响 Table 6 Effects of reducing agents on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
由表6可以看出, 采用三苯基磷做还原剂时产品收率最高, 活性锌粉-乙酸时收率次之, 采用亚硫酸钠、亚硫酸氢钠、硫脲做还原剂时效果较差。但三苯基磷做还原剂时产品分离困难, 且还原剂价格较贵。在氧化反应中, 乙酸具有稳定臭氧化物的作用。故采用锌粉-乙酸为还原剂。
2.2.8 还原分解时间
锌粉-乙酸为还原剂, n(锌粉) : n(环己烯)=1: 1, 蒸馏水20 mL, 臭氧化物0.5 h滴加至还原剂中条件下, 考察还原分解时间对环己烯臭氧化合成1, 6-己二醛反应的影响, 结果见图8。
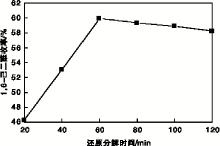 | 图8 还原分解时间对环己烯臭氧化合成1, 6-己二醛反应的影响Figure 8 Effects of restore decomposition time on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
由图8可以看出, 随着还原分解时间的延长, 1, 6-己二醛收率先升高后降低。还原分解时间为60 min时, 1, 6-己二醛收率最高, 原因可能是1, 6-己二醛不稳定, 虽然在N2保护下, 仍不能完全避免醛被氧化。
2.2.9 还原剂用量
Zn-CH3COOH为还原剂, 蒸馏水20 mL, 臭氧化物0.5 h滴加至还原剂中, , 还原分解60 min条件下, 考察还原剂用量对环己烯臭氧化合成1, 6-己二醛反应的影响, 结果见表7。
| 表7 还原剂用量对环己烯臭氧化合成1, 6-己二醛反应的影响 Table 7 Effects of reducing agents amount on 1, 6-adipaldehyde synthesized by ozonolysis of cyclohexene |
由表7可以看出, 随着n(锌粉) : n(环己烯)增大, 1, 6-己二醛收率增加, 但变化量不是很大。为了使臭氧化物还原完全, 且不造成锌粉过量很多, 选用n(锌粉) : n(环己烯)=1: 1。
通过上述反应条件的考察, 结合工业和经济角度考虑, 确定环己烯臭氧化合成1, 6-己二醛较佳反应条件为:采用乙酸与1, 2-二氯乙烷混合溶剂, 以0.05 mol环己烯计, 冰乙酸6 g, 1, 2-二氯乙烷30 mL, 臭氧化温度(0~5)℃, O2流量(100~200)mL· min-1, 活化锌粉为还原剂, n(锌粉) : n(环己烯)=1: 1, 还原分解时间60 min。在该条件下, 环己烯基本转化完全, 重复实验三次, 1, 6-己二醛平均收率可达61.6%。
(1) 系统研究环己烯臭氧化合成1, 6-己二醛工艺中的臭氧化过程和还原分解过程, 通过优化获得了较佳反应条件。 以0.05 mol环己烯计:冰乙酸和1, 2-二氯乙烷做混合溶剂, 冰乙酸6 g, 1, 2-二氯乙烷30 mL, 臭氧化温度(0~5) ℃, O2流量(100~200)mL· min-1, 活化锌粉为还原剂, n(锌粉) : n(环己烯)=1: 1, 还原分解时间60 min。在该条件下, 环己烯基本转化完全, 重复实验三次, 己二醛平均收率可达61.6%。
(2) 针对环己烯臭氧化合成1, 6-己二醛反应, 寻找能提供含O的高活性亲核试剂, 抑制臭氧化物的生成, 提高己二醛收率, 降低生产成本。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|