作者简介:赵玉华,1988年生,女,山东省菏泽市人,在读硕士研究生,研究方向为基于电荷传递的无机纳米材料细胞毒性的机制研究。
采用一种简单的固相研磨方法制备氧化锌及锰掺杂的氧化锌纳米颗粒。利用透射电子显微镜、X射线粉末衍射对样品进行结构表征。以抑菌圈实验,最小抑菌浓度和抗菌动力学曲线对样品抗菌活性进行测试。结果表明,掺杂质量分数0.5%的锰可以显著提高暗态下氧化锌的抗菌活性。与未掺杂氧化锌纳米颗粒相比,其最小抑菌浓度显著减小,失活动力学常数明显增大,而这种活性的提高有可能是锰掺杂导致氧化锌晶体缺陷增多所致。
Nanoparticles of ZnO and Mn-doped ZnO were prepared by a simple solid-state grinding method.Transmission electron microscopy and X-ray powder diffraction were used to characterize structures of the samples.Inhibition zone test,minimum inhibitory concentration and antimicrobial kinetics curve were used to evaluate their antimicrobial activity.The results showed that antimicrobial activity of ZnO nanoparticles doped with Mn mass fraction of 0.5% was remarkably improved in the dark.Compared with undoped ZnO nanoparticles,the minimum inhibitory concentration is significantly reduced,and the inactivation kinetic constant is increased remarkably.The improvement of antibacterial activity may be resulted from the increase of crystal defects of ZnO caused by Mn doping.
氧化锌是一种无机抗菌剂, 具有廉价、无毒和稳定性好的特点, 被广泛应用于各个行业[1, 2, 3, 4]。相对银系抗菌剂, 氧化锌抗菌性较弱[5], 导致在抗菌制品中的添加量较大。Sandeep S K 等[6]通过包裹有机配体和掺杂镁离子提高氧化锌抗菌活性; Anandan M 等[7]通过共沉淀法合成聚乙二醇包裹的氧化锌, 可以显著提高光催化和抗菌活性; Sharma N 等[8]通过化学共沉淀法分别得到了聚乙烯吡咯烷酮包裹的锰和铁掺杂提高氧化锌的抗菌活性。
本文通过简单的固相研磨法制备锰掺杂的氧化锌, 采用XRD及TEM对制备样品的结构及形态进行表征, 并考察样品的抗菌性能。
硫酸锌, 分析纯, 天津市鼎盛鑫化工有限公司; 硫酸锰, 分析纯, 上海化学试剂总厂所属上海试剂二厂; 氢氧化钠, 分析纯, 天津市塘沽滨海化工厂; 蛋白胨, 生物试剂, 北京奥博星生物技术有限责任公司; 牛肉浸膏, 生物试剂, 梁山科晶生物制品有限公司; 氯化钠, 分析纯, 天津市瑞金特化学品有限公司; 金黄色葡萄球菌(ATCC 25923), 南京便诊生物科技有限公司; 去离子水和超纯水均为实验室自制。
上海沪粤明HPY-91型恒温培养摇床, 浙江新丰XFS-280A+型手提式压力蒸汽灭菌器, 济南绿洁LST-ISC-A型超净工作台, 湖南凯达TG16G型高速离心机, 日本理学SmartLab Ⅲ 型号的XRD粉末衍射仪, 日本JEM-1011 型透射电子显微镜等。
1.2.1 氧化锌及锰掺杂氧化锌的制备
称取6.0 g的ZnSO4· 7H2O于干燥的研钵中, 充分研磨均匀; 再加入1.669 2 g的NaOH, 充分研磨均匀; 将反应物在3 000 r· min-1, 3 min的离心条件下, 用去离子水反复离心洗涤, 直至用0.1 mol· L-1的BaCl2溶液在上清液中检测不到白色沉淀; 将得到的沉淀物在90 ℃的烘箱中烘干, 再于200 ℃的条件下热处理2 h, 制得ZnO。
固定氧化锌用量, 按锰掺杂质量分数进行添加MnSO4· H2O, 其他步骤同上, 制得锰掺杂质量分数为5%的ZnO, 标记为5%Mn-ZnO。
1.2.2 抗菌性测试
(1) 测试菌种。本实验利用革兰氏阳性菌-金黄色葡萄球菌进行抗菌活性评价, 细菌的培养及活化均参照常规的生物学方法[9], 整个实验所用菌液浓度为108CFU· mL-1。
(2) 抑菌圈实验。采用滤纸片扩散法进行抑菌圈实验, 以直径为1 cm的滤纸圆片为载体, 用移液枪移取60 μ L含质量分数5%的样品分散液均匀滴涂在圆片上, 自然晾干; 将其紧密的贴合在涂有100 μ L菌液的固体培养基上, 将培养皿放在温度为37.4 ℃的恒温培养箱中培养12 h; 观察抑菌圈的大小。每个样品进行三次平行实验。
(3) 最小抑菌浓度[10, 11]。利用二分法将样品配置成一定的浓度梯度, 分别置于已灭菌的200 mL液体培养基的锥形瓶, 超声分散均匀, 每瓶均加入100 μ L菌液, 放在温度37 ℃, 转速140 r· min-1的摇床里恒温培养24 h; 用移液枪从每个锥形瓶移取100 μ L, 涂布在相应的培养皿里, 刮涂均匀, 置于温度37.4 ℃的恒温培养箱中培养12 h; 观察相对应样品浓度下的培养皿是否有菌落长出; 然后再利用二分法将相应长菌与不长菌的样品浓度区间分成一定的浓度梯度, 重复上述步骤; 最后找出恰好无细菌的样品浓度即最小抑菌浓度。
(4)失活常数k的测定[12]。取0.04 g样品于盛有200 mL已灭菌的液体培养基的锥形瓶里, 超声分散均匀; 然后加入100 μ L菌液, 放在温度37 ℃, 转速140 r· min-1的摇床里恒温培养; 每间隔20 min取出100 μ L定量稀释的培养液进行刮板, 将培养皿放在温度为37.4 ℃的恒温培养箱中培养12 h, 根据平板计数法数菌落。每个样品进行三次平行测试。
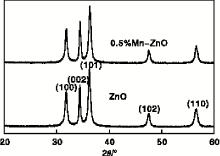
图1为氧化锌和掺杂质量分数0.5%锰的氧化锌样品XRD图。由图1可见, 样品为纯的纤锌矿结构(PDF-#36-1451)氧化锌, 表明锰的掺杂并没有改变氧化锌的物相结构; 根据谢乐公式[13]计算氧化锌及掺杂质量分数0.5%锰的氧化锌粉末的平均粒径分别为17.52 nm和16.9 nm。
图2为氧化锌和掺杂质量分数0.5%锰的氧化锌样品TEM照片。由图2可见, 近似球形的纳米颗粒有轻微团聚, 与纯氧化锌样品相比, 掺杂锰的样品颗粒团聚相对较弱。
无光照条件下, 样品对金黄色葡萄球菌的抑菌圈如图3所示。图3表明掺杂质量分数0.5%锰的氧化锌样品抑菌圈显著变大, 即抗菌性较好。
 | 图3 暗态下不同粉末对金黄色葡萄球菌的抑菌圈Figure 3 Zone of inhibition produced by the powders against Staphylococcus aureus in dark |
为定量比较抗菌活性, 对最小抑菌浓度(MIC)和失活动力学常数(k)进行测试。测试结果表明, 掺杂质量分数0.5%锰的氧化锌为0.000 375 g· mL-1; 氧化锌为0.001 54 g· mL-1。
微生物的失活速率属于一级动力学过程, 可通过Chick-Watson[10]模型进行分析。利用平板计数法, 以不同生长时间微生物菌落数(Nt)与初始时刻菌落数(N0)比的对数值为纵坐标, 以培养时间为横坐标, 做动力学曲线。基于log(Nt/N0)=-kt 求解失活动力学常数, 即斜率k的值。
样品对金黄色葡萄球菌的失活动力学曲线(图4)表明暗态下掺杂质量分数0.5%锰的氧化锌失活常数k为2.5× 10-3 min-1, 大于纯氧化锌的2.1× 10-3min-1。
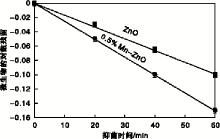 | 图4 暗态下不同粉末对金黄色葡萄球菌的失活常数Figure 4 Deactivation coefficients of Staphylococcus aureus over different powders in dark |
抑菌圈、最小抑菌浓度以及失活动力学常数都表明锰掺杂可以显著提高氧化锌对金黄色葡萄球菌的抗菌性能。最近研究[14, 15, 16]报道表明晶体缺陷可以提高氧化锌释放活性氧物种的能力。我们认为锰掺杂可能增加了氧化锌的晶体缺陷, 从而提高了其活性氧抗菌能力。
使用简单的固相研磨法成功制备了锰掺杂的氧化锌纳米颗粒, 在200 ℃热处理2 h可以显著提高氧化锌抗菌活性。与未掺杂氧化锌纳米颗粒相比, 其最小抑菌浓度显著减小, 失活动力学常数明显增大。而这种活性的提高有可能是锰掺杂导致氧化锌晶体缺陷增多所致。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|