作者简介:徐德康,1993年生,男,在读硕士研究生,研究方向为催化燃烧丙烯腈尾气。
采用等体积浸渍法将过渡金属Cu负载到ZSM-5分子筛上,并与其他金属(Fe、Co、Ag、Pd、Ce)共浸渍得到负载型催化剂,将其用于全组分丙烯腈废气的催化脱除过程。催化活性评价结果表明,丙烯腈在Cu/ZSM-5催化剂上320 ℃可以实现完全转化;掺杂质量分数2%Ce后,丙烯腈的完全转化温度降低到300 ℃,高选择生成N2的温度窗口也变宽,催化剂稳定性高。通过X射线衍射、氮气吸附-脱附、氢气-程序升温还原、氨气-程序升温脱附和X射线光电子能谱等对催化剂的物化性能进行表征,结果表明,催化剂催化氧化丙烯腈尾气的性能依赖于Cu2+的还原能力、催化剂表面弱酸与中强酸含量以及表面Cu2+丰度。
A series of M/ZSM-5 (M=Cu,CuFe,CuCo,CuAg,CuPd and CuCe) catalysts were prepared via an incipient wetness impregnation,and tested in catalytic removal of simulated C2H3CN flue.Results showed that complete conversion of acrylonitrile over Cu/ZSM-5 could be achieved at about 320 ℃.After doping of 2%Ce,complete conversion temperature of acrylonitrile decreased to 300 ℃,window temperature for high selectivity of N2widened,and catalyst stability was high XRD,N2 adsorption-desorption,H2-TPR,NH3-TPD and XPS characterization results showed that catalytic performance for combustion of acrylonitrile depended on reducibility of Cu2+,weak acid and moderate strong acid content and Cu2+ abundance on catalyst surface.
丙烯腈作为一种重要的化工原料, 主要通过丙烯氨氧化法制得。反应完成后, 经回收精制等流程得到产物丙烯腈、乙腈、氢氰酸等, 过程中会产生含丙烯腈的剧毒废气。废气中含丙烯腈、一氧化碳、丙烯、丙烷及少量氮氧化物。根据《石油化学工业污染物排放标准(GB 31571-2015)》, 排放的废气中丙烯腈含量应低于0.5 mg· m-3, 氰化氢含量应低于1.9 mg· m-3。为了满足排放要求, 需对这些污染物进行脱除。
工业上处理丙烯腈吸收塔尾气的方法主要有高温焚烧法[1]和催化氧化法[2]。高温焚烧法是在吸收塔尾气中加入辅助燃料, 通过反应器使其中的可燃物氧化分解, 应用广泛; 催化燃烧法是在催化剂作用下, 使尾气中的可燃物在较低温度(200~400) ℃反应达到完全氧化分解。催化燃烧法在较低温度下运行, 且不需要添加辅助燃料, 可大大节约成本。对于催化燃烧法, 当使用贵金属作为催化剂时, 由于贵金属的氧化性过强, 丙烯腈等含氮化合物很容易转化为NOx, 后续工段需增设NH3-SCR催化剂。如能开发具有较高活性和选择性的燃烧催化剂, 使丙烯腈等含氮化合物和NOx在碳氢化合物混合气体中高选择性先转化为N2, 则尾气中无需补充额外的氨气, 则生产成本降低, 经济效益显著。
针对丙烯腈单一组分催化净化的催化剂主要有分子筛负载催化剂和钙钛矿催化剂。Nanba T等[3, 4, 5]率先在Al2O3、SiO2、TiO2、ZrO2、MgO和ZSM-5等载体上负载不同的过渡金属和贵金属, 结果表明, Ag/TiO2和Cu-ZSM-5催化具有高的N2选择性, Cu-ZSM-5催化剂上丙烯腈在350 ℃能完全转化, N2选择性95%; 而在Ag/TiO2催化剂上, 400 ℃可达到80%的N2选择性。进一步研究发现[6], 即使选择不同晶形的TiO2也无法进一步提高低温活性, 且比表面积较低(小于100 m2· g-1), 因此, 后续的研究主要集中于分子筛催化剂。Liu N等[7]分析比较了不同硅铝比ZSM-5分子筛上负载Cu、Co、Fe制得的催化剂催化氧化丙烯腈的性能, 结果表明, 低硅铝比ZSM-5负载Cu催化剂具有最佳的N2选择性。该团队还制备了Cu/SBA-15[8]和含Cu的钙钛矿结构催化剂[9], 选择性均逊于Cu/ZSM-5催化剂。
本文采用等体积浸渍法将过渡金属Cu负载到ZSM-5分子筛上, 并与其他金属(Fe、Co、Ag、Pd、Ce)共浸渍得到负载型催化剂, 将其用于全组分丙烯腈废气的催化燃烧实验中, 考察催化活性和稳定性, 旨在验证其作为工业化催化剂的可行性。
采用等体积浸渍法制备改性分子筛催化剂。分子筛H-ZSM-5(硅铝物质的量比为27, 南开大学催化剂厂)粉体在20 MPa压片, 筛分(40~60)目的颗粒备用。首先测定分子筛载体的吸水率, 根据吸水率进行催化剂等体积浸渍。称取一定量金属硝酸盐, 溶解、定容, 配制标准液。根据金属负载量, 将标准液稀释成一定浓度的溶液, 完全浸湿载体, 陈化5 h, 烘箱120 ℃放置24 h, 马弗炉中以2 ℃· min-1速率升温至550 ℃, 保持4 h, 冷却后即得xM/ZSM-5催化剂, 其中x表示金属负载质量分数, M代表金属。
X射线衍射测试采用日本理学公司 RINTD/MAX-2500PC 型粉末X射线衍射仪, CuKα , 工作电压40 kV, 工作电流40 mA, λ =0.154 056 nm, 扫描速率5 ℃· min-1, 扫描范围10° ~70 ° 。
比表面积及孔结构测试采用美国康塔仪器公司Autosorb- IQ-XRQ全自动气体吸附分析仪, 测试前, 将样品在300 ℃、真空条件下预处理3 h, 之后在液氮温度下进行吸附-脱附实验, BET方法计算比表面积, t-plot和DFT方法计算孔容和孔径分布。
H2-程序升温还原分析采用美国康塔仪器公司ChemBET Pulsar型化学吸附仪, 每次取约50 mg样品, 置于U型石英反应管中。测试前, 先将样品在500 ℃用He吹扫1 h, 冷却至室温后, 将气路切换为10%H2-Ar混合气, 以10 ℃· min-1升温至900 ℃, 检测并记录信号值随温度的变化。
NH3-程序升温脱附采用美国康塔仪器公司ChemBET Pulsar型化学吸附仪, 每次取约200 mg样品, 置于U型石英反应管中。测试前, 先将样品在500 ℃用He吹扫1 h; 冷却至室温后, 将气路切换为NH3-He混合气吸附1 h, 然后切换气路至He气, 调整TCD基线, 基线平稳后, 以10 ℃· min-1升温至700 ℃, 检测并记录信号值随温度的变化。
X射线光电子能谱采用美国赛默飞世尔科技公司ESCALAB 250型X射线光电子能谱仪, AlKɑ , C1s(284.6 eV)进行电荷校准。
采用固定床反应器评价催化剂性能, 反应器尺寸为ϕ 6 mm× 350 mm, 将1 mL催化剂装入石英管中, 置于管式炉恒温区, 并在催化剂床层中间插入热电偶监测温度变化。气体总流量500 mL· min-1(空速30.000 h-1), 原料气中丙烯腈(ACN)体积分数为0.22%, 丙烯、丙烷(以C3表示)体积分数均为0.06%, O2体积分数为5%, N2为平衡气, 以北京七星华创公司D07-11C型质量流量计控制流量。混合气体经安捷伦7890A型气相色谱测定, FFAP型填充柱进行分离, FID检测器检测丙烯腈、C3含量(丙烯和丙烷不能完全分离); 且气体通过德国益康公司Ecom-J2KN烟气分析仪在线检测NH3和NOx(NO、NO2)浓度, 其中N2O的浓度忽略不计, 从而得到不同温度下丙烯腈、C3转化率及N2选择性。
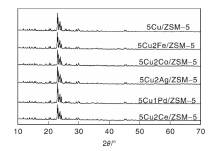
图1为负载不同金属xM/ZSM-5催化剂的XRD图。
由图1可以看出, 在ZSM-5分子筛载体上浸渍质量分数5%Cu时, 催化剂样品仍能保持改性前的结构特征, Cu的引入未导致分子筛结构发生明显变化; 当Cu与其他金属共浸渍时, 在35.6° 和38.7° 并未观察到明显的CuO特征峰, 表明催化剂表面上的CuO呈高度分散状态或CuO含量太低超出仪器的最低检测限。
图2为不同金属负载前后催化剂的N2吸附-脱附等温线, 表1为负载前后催化剂的比表面积和孔结构参数。由图2和表1可以看出, 随着金属负载量增加, 比表面积和孔容均有不同程度下降, 顺序为H-ZSM-5> 5Cu/ZSM-5> 5Cu2Ce/ZSM-5> 5Cu2Fe/ZSM-5> 5Cu2Co/ZSM-5> 5Cu2Ag/ZSM-5> 5Cu1Pd/ZSM-5, 可能是由于少量负载的金属氧化物沉积于分子筛的孔道内, 部分孔道被堵塞。通过DFT方法计算得到的孔径也表明孔径主要集中约1.20 nm处。
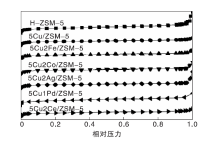 | 图2 负载不同金属xM/ZSM-5催化剂的N2吸附-脱附曲线Figure 2 N2 adsorption-desorption isotherms of xM/ZSM-5 catalysts containing different metals |
| 表1 负载不同金属xM/ZSM-5催化剂的物化结构参数 Table 1 Physical-chemical properties of pure xM/ZSM-5 catalysts containing different metals |
图3为负载催化剂的H2-TPR谱图。由图3可以看出, 5Cu/ZSM-5催化剂具有3个还原峰, 在220 ℃出现的峰归属为孤立Cu2+→ Cu+, 在260 ℃的峰归属为纳米CuO颗粒还原为Cu, 而在约330 ℃的峰则对应于Cu+→ Cu[10]。5Cu2Ce/ZSM-5催化剂在183 ℃、240 ℃和315 ℃具有3个还原峰, 与5Cu/ZSM-5催化剂相比, 还原峰均向低温方向偏移, 表明Ce的掺杂可明显提高催化剂还原性, 从而有利于提高其低温活性。对于5Cu2Fe/ZSM-5催化剂, (330~360) ℃的还原峰归属于Fe3+→ F
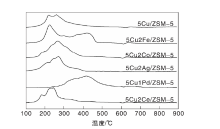 | 图3 负载不同金属xM/ZSM-5催化剂的H2-TPR谱图Figure 3 H2-TPR profiles of xM/ZSM-5 catalysts containing different metals |
为了揭示催化剂表面酸强度及酸量对催化剂性能的影响, 对系列催化剂样品进行NH3-TPD表征, 结果见图4。由图4可以看出, 不同催化剂主要在230 ℃和300 ℃附近出现NH3脱附峰, 低温脱附峰为结合在较弱L酸性位的弱吸附NH3的脱附, 中高温脱附峰为吸附于中等强度B酸性位的N
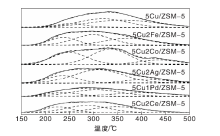 | 图4 负载不同金属xM/ZSM-5催化剂的NH3-TPD谱图Figure 4 NH3-TPD profiles of xM/ZSM-5 catalysts containing different metals |
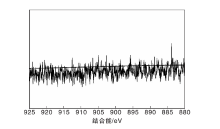
为进一步考察催化剂上金属的存在状态及表面化学环境, 对单组分5Cu/ZSM-5催化剂及活性与选择性最好的5Cu2Ce/ZSM-5催化剂进行XPS表征, 结果如图5和图6所示。由图5和图6可以看出, 5Cu/ZSM-5催化剂在933.6 eV和953.0 eV主要有两个峰, 分别归属于Cu2p3/2和Cu2p1/2, 其中Cu2p3/2又可以分峰为933.4 eV的纳米CuO以及935.2 eV的孤立C
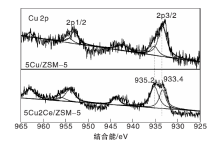 | 图5 5Cu/ZSM-5和5Cu2Ce/ZSM-5催化剂的Cu2p XPS谱图Figure 5 Cu2p XPS spectra of 5Cu/ZSM-5 and 5Cu2Ce/ZSM-5 catalysts |
表2列出5Cu/ZSM-5和5Cu2Ce/ZSM-5催化剂表面活性组分的分布情况。由表2可以看出, 当Cu与Ce共浸渍时, 催化剂表面孤立Cu2+含量大大增加, 表明Ce可以使催化剂表面的活性组分Cu2+增加, 从而提高催化活性。根据分峰结果, 虽然孤立Cu2+和纳米CuO均有增加, 但孤立Cu2+增加的量更显著, 最终使得Cu2+/CuO增大。
| 表2 5Cu/ZSM-5和5Cu2Ce/ZSM-5催化剂表面元素组成 Table 2 Surface atom abundance of 5Cu/ZSM-5 and 5Cu2Ce/ZSM-5 catalysts |
丙烯腈废气在负载不同金属xM/ZSM-5催化剂上的催化燃烧活性如图7所示。由图7可以看出, 丙烯腈转化后的产物除N2外, 还有NO、NO2和NH3, 其中N2O的量忽略不计。5Cu1Pd/ZSM-5催化剂的低温活性最好, 300 ℃时能将丙烯腈完全转化; 5Cu2Ce/ZSM-5也在300 ℃实现丙烯腈完全转化; 其余与Cu共浸渍的催化剂与5Cu2Ce/ZSM-5活性相差不大, 且均在320 ℃时将丙烯腈完全转化, 表明Cu与Fe、Co、Ag共浸渍并未显著提高5Cu/ZSM-5催化剂催化活性。
 | 图7 丙烯腈废气在不同xM/ZSM-5催化剂上的催化燃烧活性Figure 7 Selective catalytic combustion of C2H3CN over xM/ZSM-5 catalysts |
从图7还可以看出, 低于300 ℃时, 随着反应温度增加, 丙烯腈转化率增加, N2选择性增加, 300 ℃时, N2选择性达到100%, 其中5Cu1Pd/ZSM-5催化剂的低温选择性最好, 但随着反应温度升高, N2选择性先急速下降, 后缓慢回升, 是由于低温下Pd具有高的丙烯腈燃烧活性; 随着反应温度增加, Pd组分上生成氮氧化物的选择性增加, 但是当温度高于400 ℃时, Cu组分上HC-SCR反应活性提高, N2选择性增加。而其他催化剂, 反应温度对选择性影响不大, 即使在较高温度500 ℃时, N2选择性均大于95%。仅Ce的掺杂可以使催化剂在更低温度下达到最大的N2选择性。
从图7还可以看出, 随着反应温度逐渐增加, 催化剂对于C3H8/C3H6的活性顺序为5Cu1Pd/ZSM-5> 5Cu2Ce/ZSM> 5Cu2Co/ZSM-5> 5Cu/ZSM-5≈ 5Cu2Ag/ZSM-5> 5Cu2Fe/ZSM-5, 由此可见, 5Cu1Pd/ZSM-5和5Cu2Ce/ZSM-5催化剂催化活性最好, 当丙烯丙烷完全转化时, 其余催化剂还未起活, 其中5Cu2Fe/ZSM-5在350 ℃时, 丙烯丙烷才完全转化, 与H2-TPR结果一致, Fe的掺杂抑制了CuO的还原。
综上所述, 5Cu1Pd/ZSM-5具有最好的丙烯腈和丙烯丙烷低温催化燃烧活性, 但N2选择性最差; 而5Cu2Co/ZSM-5和5Cu2Ag/ZSM-5的低温活性略低于5Cu1Pd/ZSM-5, 但选择性显著优于5Cu1Pd/ZSM-5; 5Cu2Fe/ZSM-5对丙烯丙烷的低温活性较差; 5Cu2Ce/ZSM-5的低温活性和选择性均最佳。
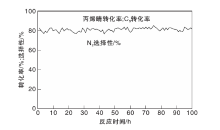
为了准确模拟工业实际工况, 在实验室模拟如下气体组成(体积分数)进行5Cu2Ce/ZSM-5催化剂的稳定性测试:0.06%丙烯腈、0.06%一氧化氮、0.54%一氧化碳、0.09丙烯、0.09%丙烷、5%氧气以及5%水蒸汽, N2为平衡气。空速为30 000 h-1, 固定床反应器入口温度为320 ℃, 结果如图8所示。
由图8可以看出, 丙烯腈和丙烯丙烷可以达到100%转化率, N2选择性约在80%, 反应100 h后转化率和选择性没有明显降低的趋势, 表明5Cu2Ce/ZSM-5催化剂具有良好的稳定性。
(1) 采用等体积浸渍法将过渡金属Cu负载到ZSM-5分子筛上, 并与其他金属(Fe、Co、Ag、Pd、Ce)共浸渍得到负载型催化剂。
(2) 负载型催化剂保持高的比表面积和孔容, 且金属均匀分散。在5Cu2Ce/ZSM-5催化剂上, 300 ℃即可以实现丙烯腈完全转化; 320 ℃时, C3(丙烯丙烷)完全转化, 且N2选择性较高。原因是Ce的掺杂改善了CuO的还原性能, 提高孤立Cu2+的含量所致。
(3) 5Cu2Ce/ZSM-5催化剂具有优良的稳定性, 为丙烯腈尾气催化净化技术的工业应用奠定了基础。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|