作者简介:董朝霞,1992年生,女,河南省三门峡市人,在读硕士研究生。
采用浸渍法制备系列不同负载量的Fe/ZrO2催化剂,用于气相催化裂解1,1,2-三氯乙烷脱氯化氢性能的研究。结果表明,反应温度为350 ℃时,负载Fe质量分数为1%的1Fe/ZrO2催化剂催化活性最好,1,1,2-三氯乙烷转化率约95.0%,顺式1,2-二氯乙烯选择性为91.0%,反应50 h性能稳定不失活,1,1,2-三氯乙烷转化率约92.0%,顺式1,2-二氯乙烯选择性约90.0%。单一ZrO2载体上的脱氯反应初始转化率为90.0%,经过1 h反应即快速失活。ZrO2催化剂失活归因于ZrO2表面酸性较强导致积炭。对于Fe/ZrO2催化剂,Fe物种不但提供新的活性位点,而且降低了催化剂的表面强酸性中心,使催化剂催化活性更高,稳定性更好。
A series of Fe/ZrO2catalysts with different loading amount were prepared by an impregnation method and tested for the gas phase dehydrochlorination of 1,1,2-trichloroethane(TCE) to synthesize cis-1,2-dichloroethylene( cis-DCE).Results showed that 1Fe/ZrO2catalyst with Fe mass content of 1% showed the best activity and stability in 50 h,with 1,1,2-trichloroethane conversion of 95.0% and cis-DCE selectivity of 90.0% when reaction temperature was 350 ℃.The pristine ZrO2catalyst had high initial activity with 1,1,2-trichloroethane conversion of 90.0%,but it deactivated after 1 h of reaction.The results reveal that strong acid sites on ZrO2 surface are responsible for the deposition of coke and consequently catalyst deactivation.The addition of Fe in Fe/ZrO2catalysts decreases amounts of strong acid sites and generates new active sites to enhance activity and stability of catalysts.
氯代有机物(如三氯乙烷)是化工生产中重要的有机溶剂, 广泛应用于还原剂、导热剂、防腐杀菌剂、除草剂以及化工、医药、农药生产原料与中间体, 可通过生产废水排放、废物填埋与焚烧和事故性泄漏等多种途径对环境造成严重污染[1], 如何有效降解氯代有机物是目前关注的一大问题。氯代有机物的毒性主要是由于氯原子的引入, 如能将氯原子以HCl的形式脱除, 即可有效降低其毒性[2]。
气相催化裂解三氯乙烷脱HCl反应具有高效环保的优点, 该反应的主要产物是1, 2-二氯乙烯[3]、顺式-1, 2-二氯乙烯[4, 5, 6]和反式-1, 2-二氯乙烯[7]。施津津等[8]考察了不同孔径硅胶负载的铯盐对1, 1, 2-三氯乙烷脱 HCl 的影响, 发现反应温度为400 ℃时, CsNO3 /278A催化剂催化活性和选择性最好, 这是由于CsNO3的碱性最强, 且278A硅胶孔径大, 负载的碱量最多。Mu X等[9]考察了四烷基氯化鏻高效催化1, 2-二氯乙烷脱HCl的理论研究, 认为静电控制反应性能, 四丁基氯化鏻催化活性高主要是其阴阳离子间的静电相互作用较其他离子液体静电作用弱, 导致碱性最强, 且阴阳离子间的协同作用诱导二氯乙烯C-H和C-Cl键的裂解和H-Cl键的形成。Tang C等[10]考察了Mg/SiO2催化剂催化1, 1, 2-三氯乙烷脱HCl反应, 发现10%Mg/SiO2催化性能最高(转化率达92.0%), 且20 h内不失活, 指出反应过程中形成Mg(OH)Cl物种是反应的活性位点。Song T等[11]从催化剂的酸碱性角度考察了SiO2负载型催化剂对1, 1, 2-三氯乙烷脱HCl反应产物选择性的影响及反应机理, 指出碱性催化剂有利于生成偏二氯乙烯, 中强L酸有利于生成顺式-1, 2-二氯乙烯, 同时酸碱性也会导致反应机理的差别。
催化剂稳定性是评价催化剂性能的重要指标, 也是工业化生产中关注的重要因素。胡益浩等[12]考察了负载型过渡金属催化剂催化裂解三氯乙烷脱HCl反应, 指出催化剂表面的强酸中心是导致催化剂表面积炭、进而引起失活的主要原因。靳燕霞等[13]考察了反应温度对CsNO3/SiO2气相催化裂解三氯乙烷脱HCl合成偏二氯乙烯反应的影响, 发现导致催化剂失活的主要原因是含氯反应产物在低温反应时难以从催化剂表面脱附。为此, 许多学者进行了深入研究, 发现添加一些活性组分如Fe、Ni等金属, 由于与载体之间相互作用, 进而提高催化剂的活性和稳定性。Luo J W等[14]考察了氟化的NiO/Cr2O3催化剂催化1, 1, 1, 3, 3-五氟丙烷脱HF合成1, 3, 3, 3-四氟丙烯, 发现NiO提供了新的酸性位点和较低的酸性密度中心, 从而提高了催化活性和稳定性。宋建冬等[15]考察了FeOx/MgF2催化剂气相催化1, 1, 1, 3, 3-五氟丙烷脱HF反应, 发现Fe的添加明显提高了催化剂催化活性和稳定性(50 h内不失活), 这是由于表面铁物种能够较好地分散在载体表面, 与载体作用形成较多的酸性位点。Wan Haijun等[16]考察了Fe-Al2O3间相互作用对F-T合成反应的影响, 发现Fe-Al2O3间的强相互作用会削弱催化剂表面的碱性, 抑制FeO还原为铁的过程, 从而提高了催化剂的稳定性。Tian Dayong等[17]制备了Ni-Fe/γ -Al2O3催化剂用于CO全甲烷化反应, 发现合适的Ni与Fe比是影响催化活性的关键, Fe的加入可有效提高Ni/g-Al2O3的催化活性。对于三氯乙烷脱HCl反应, 表面酸性中心是反应的活性位点, 但强酸性中心会导致催化剂积炭而失活。基于Fe的加入可增强与载体间相互作用以及可调节催化剂表面酸性来提高催化剂催化活性和稳定性这一优点, 本文采用浸渍法制备系列不同负载量的Fe/ZrO2催化剂, 用于气相催化裂解1, 1, 2-三氯乙烷脱HCl反应, 探究Fe负载量、焙烧温度及反应温度等对其催化性能的影响, 并分析催化剂失活原因。
采用浸渍法制备系列不同负载量的Fe/ZrO2催化剂。
1.1.1 ZrO2载体的制备
称取11.56 g的ZrO(NO3)2, 加入100 mL去离子水, 搅拌溶解得到ZrO(NO3)2溶液; 量取7.5 mL浓氨水于另一烧杯中, 加入100 mL去离子水, 搅拌溶解; 将氨水逐滴加入ZrO(NO3)2溶液中, 同时不断搅拌, 直到pH=9.0, 沉淀完全, 静置, 抽滤。将样品置于烘箱100 ℃烘干过夜, 马弗炉500 ℃焙烧4 h, 研磨, 得到ZrO2白色粉末。
1.1.2 Fe/ZrO2催化剂制备
Fe负载量按质量分数计算, 以Fe质量分数为0.3%的0.3Fe/ZrO2催化剂为例。称取1.00 g的ZrO2粉末, 0.003 g的Fe(NO3)3· 9H2O于蒸发皿中, 加入适量蒸馏水, 搅拌溶解, 超声0.5 h, 浸渍3 h, 90 ℃水浴炒干, 得到淡黄色粉末。将其置于烘箱80 ℃烘干过夜, 得到负载Fe质量分数为0.3%的催化剂, 标记为0.3Fe/ZrO2。负载Fe质量分数为1%、6%、10%的催化剂, 分别标记为1Fe/ZrO2、6Fe/ZrO2、10Fe/ZrO2、10Fe/SiO2。
XRD分析采用德国布鲁克公司D8 ADVANCE X射线粉末衍射仪, CuKα , 波长0.154 2 nm, 扫描范围10° ~90° , 样品测试条件为室温状态和空气气氛中。
采用美国康塔仪器公司Autosorb-1型物理吸附仪测试样品的比表面积及孔性质, 吸附前催化剂在真空中120 ℃预处理4 h, 在-196 ℃条件下吸附N2。
采用美国Thermo Fisher Scientific公司ESCALAB 250Xi型X射线光电子能谱仪, AlKα , 工作电压20 kV, hν =1 486.6 eV, 电子结合能先用表面沉积碳校正(污染碳的结合能C1s为 284.8 eV), 之后采用XPSPEAK41软件进行分峰拟合。
催化剂表面酸性采用自制NH3-程序升温脱附实验装置进行分析, 称取0.2 g的0.3Fe/ZrO2催化剂装于石英管中, 在500 ℃、N2气氛中预处理0.5 h, 流速为20 mL· min-1, 50 ℃吸附NH3时间 0.5 h (20 mL· min-1), 在100 ℃通N2 (30 mL· min-1)吹扫0.5 h, 以除去催化剂表面物理吸附的NH3。之后从60 ℃升温至800 ℃(20 ℃· min-1), 用TCD检测和记录NH3脱附信号。
采用英国Renishaw公司Invia型拉曼光谱仪, 样品压片, 激光波长为325 nm, 扫描范围(100~1 800) cm-1, 保留时间60 s, 扫描4次, 分辨率1 cm-1。
气相催化裂解1, 1, 2-三氯乙烷脱HCl反应在自制固定床反应器上进行。称取0.100 g的1Fe/ZrO2催化剂装入反应管(直径8 mm)中, 将其固定于固定床反应器中, 热电偶插在催化剂的中间位置, 以监测管内实际温度。以20 ℃· min-1的升温速率从室温程序升温至500 ℃, N2气氛(10 mL· min-1)预处理1.5 h; 待温度降至350 ℃时进行气相催化裂解三氯乙烷脱HCl反应。N2通过装有1, 1, 2-三氯乙烷的饱和器(饱和器于冰浴中冷却), 将其带入催化剂床层(N2流速10 mL· min-1), 反应产物用安捷伦6890型气相色谱(FID)分析(DB1毛细管柱, 色谱柱30 m× 0.32 mm)。
BET测试结果显示ZrO2载体及0.3Fe/ZrO2、1Fe/ZrO2、6Fe/ZrO2、10Fe/ZrO2催化剂比表面积分别为41.5 m2· g-1、40.6 m2· g-1、40.1 m2· g-1、38.1 m2· g-1、37.8 m2· g-1, 表明随着FeOx含量增加, 催化剂比表面积有所下降, 归因于FeOx堵塞了ZrO2载体的孔道。
图1是反应前后ZrO2载体及Fe/ZrO2催化剂的XRD图。从图1可见, 新鲜Fe/ZrO2催化剂呈现单斜相ZrO2的衍射峰(PDF#37-1484), 随着Fe负载量增加, 并未对催化剂衍射峰产生明显影响。图中未出现铁物种的特征衍射峰, 表明Fe物种在ZrO2表面可能是高度分散状态。反应前后Fe/ZrO2催化剂的衍射峰没有观察到任何变化, 表明ZrO2的结构在反应过程中保持完整。
 | 图1 反应前后ZrO2载体、Fe/SiO2和Fe/ZrO2催化剂的XRD图Figure 1 XRD patterns of fresh and spent ZrO2support, Fe/SiO2and Fe/ZrO2catalysts |
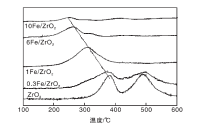
图2是反应前ZrO2载体及Fe/ZrO2催化剂的NH3-TPD谱图。
从图2可见, ZrO2载体在380 ℃和490 ℃出现两个明显的脱附峰, 分别归属于ZrO2的强酸中心和弱酸中心[18, 19, 20]。负载Fe质量分数为0.3%、1%、6%、10%的Fe/ZrO2催化剂脱附峰温度逐渐降低, 且脱附峰数量减少, 表明负载Fe后的催化剂ZrO2的强酸中心数目明显下降并消失, 弱酸中心数目先增后减, 1%Fe/ZrO2催化剂的弱酸中心数目最大。这可能是由于Fe物种单层高度分散于ZrO2载体上, 首先覆盖了载体的强酸中心, 然后进一步覆盖弱酸中心[21, 22]。表明氧化铁的酸性很弱, 且酸中心数目很少。
图3是ZrO2载体和1Fe/ZrO2催化剂反应前后的XPS谱图。由图3可以看出, 反应前ZrO2载体的Zr3d5/2结合能在182.6 eV处谱峰归属于Z
图4为ZrO2载体、Fe/SiO2和Fe/ZrO2催化剂气相催化裂解三氯乙烷脱HCl性能。从图4可以看出, ZrO2载体的初始活性很高, 达到90.0%, 10Fe/SiO2催化剂的初始活性达到78.0%, 0.3Fe/ZrO2催化剂的初始活性达到95.0%, 但1 h内均会出现明显的失活现象。随着Fe负载量增加, 1Fe/ZrO2、6Fe/ZrO2、10Fe/ZrO2催化剂的活性超过95.0%, 且在10 h未出现失活现象, 表明Fe的加入可以明显提高催化剂的活性和稳定性。这是由于尽管催化剂的表面酸性中心是该脱氯反应的活性中心[12], 但ZrO2和0.3Fe/ZrO2催化剂上存在强酸中心且数目较多, 使得氯化物与催化剂表面强酸性位强相互作用, 导致催化剂表面积炭失活。由图4还可以看出, 10Fe/SiO2催化剂上顺式-1, 2-二氯乙烯选择性最低, ZrO2、0.3Fe/ZrO2和1Fe/ZrO2催化剂上顺式-1, 2-二氯乙烯选择性较高(约92.0%), 随着Fe负载量增加, 6Fe/ZrO2和10 Fe/ZrO2催化剂上顺式-1, 2-二氯乙烯选择性下降为85.0%。 这是由于加入一定量的Fe在提供新活性位点的同时, 也覆盖了ZrO2载体的部分强酸性位点, 且催化剂的表面酸性随着Fe负载量的增加逐渐减小。综上所述, 1Fe/ZrO2催化剂催化性能最好, 1, 1, 2-三氯乙烷转化率约95.0%, 顺式-1, 2-二氯乙烯选择性91.0%。
 | 图4 ZrO2载体、Fe/SiO2和Fe/ZrO2催化剂气相催化裂解三氯乙烷脱HCl性能Figure 4 Catalytic performance of ZrO2support, Fe/SiO2 and Fe/ZrO2 catalysts for dehydrochlorination of trichloroethane |
表1是焙烧温度、反应温度对1Fe/ZrO2催化剂气相催化裂解1, 1, 2-三氯乙烷脱HCl性能的影响。从表1可知, 随着1Fe/ZrO2焙烧温度升高, 气相催化裂解1, 1, 2-三氯乙烷脱HCl反应的催化活性逐渐减小, 焙烧温度500 ℃的催化活性最好, 顺式-1, 2-二氯乙烯选择性最高。反应温度对气相催化裂解1, 1, 2-三氯乙烷脱HCl反应的催化活性影响很大, 随着反应温度降低, 1, 1, 2-三氯乙烷转化率逐渐减小, 顺式-1, 2-二氯乙烯选择性逐渐增大, 表明低温条件有利于顺式-1, 2-二氯乙烯生成。因此, 1Fe/ZrO2最佳反应条件为焙烧温度500 ℃, 反应温度350 ℃。
| 表1 焙烧温度和反应温度对1Fe/ZrO2催化剂气相催化裂解1, 1, 2-三氯乙烷脱HCl性能的影响 Table 1 Effects of calcinations and reaction temperature on gas phase catalytic dehydrochlorination of 1, 1, 2-trichloroethane over 1Fe/ZrO2 catalyst |
图5是反应温度350 ℃条件下, 不同Fe前驱体对1Fe/ZrO2催化剂气相催化裂解1, 1, 2-三氯乙烷脱HCl性能的影响, Fe(NO3)3前驱体以1Fe/ZrO2表示, FeCl3前驱体以1FeCl3/ZrO2表示。
 | 图5 Fe前驱体对1Fe/ZrO2催化剂气相催化裂解1, 1, 2-三氯乙烷脱HCl性能的影响Figure 5 Effects of Fe precursor on gas phase catalytic dehydrochlorination of 1, 1, 2-trichloroethane over 1Fe/ZrO2 catalyst |
从图5可以看出, 两种前驱体制备的催化剂, 催化活性完全相同, 1, 1, 2-三氯乙烷转化率稳定约94.0%, 顺式-1, 2-二氯乙烯选择性约92.0%, 且反应10 h未出现失活现象, 表明Fe前驱体对Fe/ZrO2催化剂的脱氯性能影响不大。
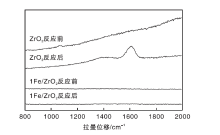
图6是反应前后ZrO2载体和1Fe/ZrO2催化剂的拉曼光谱图。由图6可以看出, 反应前的ZrO2没有出现拉曼振动峰, 但反应后的ZrO2在1 380 cm-1和1 600 cm-1处出现明显的拉曼振动峰, 均归属为碳物种的振动峰[29], 而1Fe/ZrO2催化剂在反应前后均未出现明显的拉曼振动峰。表明反应过程中ZrO2表面有积炭产生。
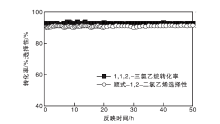
1Fe/ZrO2催化剂上气相催化裂解1, 1, 2-三氯乙烷脱HCl反应稳定性实验结果见图7。由图7可以看出, 反应50 h催化剂未出现失活现象, 转化率稳定约92.0%, 顺式-1, 2-二氯乙烯选择性稳定在90.0%。由此可知, 在脱HCl反应过程中, 催化剂表面积炭是导致失活的主要原因, 而积炭产生的主要原因是催化剂的表面强酸中心[12], 与图2结果一致。由于ZrO2的酸性较强, 容易发现积炭, 所以催化剂失活很快。
(1) ZrO2上气相催化裂解1, 1, 2-三氯乙烷脱HCl反应的活性很高, 达到90.0%, 但1 h内就快速失活, 主要是由于ZrO2表面存在强酸中心且数目较多, 导致催化剂表面积炭而失活。
(2) Fe/ZrO2催化剂气相催化裂解1, 1, 2-三氯乙烷脱HCl反应的催化活性和反应稳定性明显高于ZrO2。1Fe/ZrO2催化剂表现出最好的催化活性, 在反应温度为350 ℃时, 1, 1, 2-三氯乙烷转化率约95.0%, 顺式-1, 2-二氯乙烯选择性91.0%, 且50 h内稳定不失活。
(3) Fe/ZrO2催化剂催化活性提高的主要原因是Fe2O3或反应过程中生成的Fe-O-Cl物种不仅提供了新的反应活性位点, 而且覆盖了载体的强酸中心, 降低了催化剂的表面酸度。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|