作者简介:黄雪松,1994年生,男,安徽省铜陵市人,在读硕士研究生,研究方向为水处理。
采用水热和沉淀两步合成法制备AgBr/Zn3(OH)2V2O7·2H2O催化剂,研究其在可见光下降解亚甲基蓝溶液的性能,并考察催化剂用量、亚甲基蓝溶液初始浓度、pH值以及盐浓度对光催化性能的影响,评价AgBr/Zn3(OH)2V2O7·2H2O催化剂的重复使用性能。结果表明,在前驱液pH为10、120 ℃水热10 h、Ag与Br物质的量比为0.20条件下制备的复合催化剂在可见光下反应120 min后,1.0 g·L-1的催化剂对10 mg·L-1的亚甲基蓝溶液脱色率达到85.2%。NaCl对亚甲基蓝的降解起抑制作用,Na2SO4对亚甲基蓝的降解起促进作用。催化剂重复使用4次后,光照120 min后的亚甲基蓝溶液脱色率可达66.4%。催化剂对不同初始浓度亚甲基蓝溶液的光催化降解符合一级动力学模型。
AgBr/Zn3(OH)2V2O7·2H2O catalyst was prepared by hydrothermal and precipitation two-step synthesis method and tested in degradation of methyl blue solution under visible light.Effects of catalyst amount,initial concentration of methyl blue solution,pH,and salt concentration on photocatalytic performance was investigated and reusability of AgBr/Zn3(OH)2V2O7·2H2O catalysts was evaluated.The results showed that,after 120 min reaction under visable light,decolorization rate of 10 mg·L-1 methylene blue solution reached 85.2% over 1.0 g·L-1 composite catalyst prepared under conditions of pH 10,hydrothermal temperature of 120℃ for 10 h,and Ag/Br molar ratio of 0.20.NaCl inhibited degradation of methylene blue while Na2SO4 promoted degradation of methylene blue.After 4 times of repeated use of the catalyst,decoloration rate of methylene blue solution reached 66.4% after light irradiation for 120 min.The photocatalytic degradation of methylene blue solution with different initial concentrations over the catalyst met first-order kinetic model.
染料废水因其高色度、成分复杂和可生化性差及“ 三致” 毒性等成为影响我国水环境安全的重要因素之一[1, 2, 3]。与传统废水处理技术相比, 光催化氧化技术具有更强的氧化能力, 能有效破坏染料分子中的芳香基, 将其转化为H2O和CO2等小分子, 最终实现完全矿化[4, 5, 6]。
钒系化合物具有优良的电化学和光学特性, 是一种重要的功能材料, 早期被广泛用于电极材料、光学材料和磁性材料等领域[7, 8, 9]。焦矾酸锌是一种钒酸锌类材料, 结构特殊, 近年来, 研究者对其关注度逐渐上升。
焦矾酸锌[Zn3(OH)2V2O7· 2H2O]晶体属于六方晶系, 结构为多孔框架结构, Zhang S Y等[10]室温下用简单的液相沉淀法合成了直径(2~3) μ m的Zn3(OH)2V2O7· 2H2O微球, 探究了沉淀时间、反应温度及溶液pH值等与产物形貌的关系, 并将制备的焦矾酸锌于350 ℃焙烧2 h得到Zn3(VO4)2, 其具有焦矾酸锌的形貌特征, 初始放电容量较高, 循环充放电性能较好。
为提高焦矾酸锌的光催化性能, 近几年逐渐开始了对焦矾酸锌的改性研究, 如利用不同的过渡金属进行掺杂、金属氧化物的改性以及非金属化合物来制成复合材料等, 均能提高光催化活性。
本文旨在研究通过改变目标污染物的pH值、催化剂用量、污染物溶液的初始浓度以及盐效应等因素探究对AgBr/Zn3(OH)2V2O7· 2H2O催化剂光催化性能的影响因素, 考察催化剂重复使用性能, 并对不同初始浓度亚甲基蓝溶液的光催化降解采用Langmuir-Hinshelwood模型进行动力学分析。
采用水热和沉淀两步合成法制备催化剂, 按Zn与V物质的量比为3∶ 2称取一定量的Zn(NO3)2· 6H2O和NaVO3· 2H2O分别溶于蒸馏水中, 再将NaVO3溶液超声30 min后, 边搅拌边缓慢加入Zn(NO3)2溶液中, 继续磁力搅拌30 min得到前驱液, 用浓氨水调节前驱液的pH=10, 搅拌均匀, 转移至反应釜中, 120 ℃水热10 h。待反应釜自然冷却至室温后, 过滤, 用蒸馏水洗涤数次, 80 ℃条件下烘干, 即得焦矾酸锌。
取一定量的焦矾酸锌加入蒸馏水中, 超声分散10 min后进行磁力搅拌, 向其中逐滴加入一定体积0.01 mol· L-1的AgNO3溶液, 避光搅拌30 min; 再向上述混合液中逐滴加入与AgNO3溶液等体积0.01 mol· L-1的NaBr溶液, 继续避光搅拌4 h; 最后将沉淀物过滤, 用蒸馏水洗涤数次, 80 ℃烘干, 即得到AgBr/Zn3(OH)2V2O7· 2H2O催化剂。
以亚甲基蓝为探针污染物, 进行可见光催化降解实验。
将催化剂加入亚甲基蓝溶液中, 先避光磁搅拌30 min进行暗吸附, 在暗吸附开始和结束时分别取一定量溶液, 离心分离后取上清液, 在664 nm处测吸光度; 暗吸附结束后, 取下避光罩, 打开镝灯, 将反应器移至光源正下方, 固定光源与反应液面的距离约15 cm, 连接冷凝水, 在磁力搅拌下进行光催化反应。每隔20 min取一定量溶液, 离心分离取上清液, 在664 nm处测吸光度。
本实验光催化效果用未扣除暗吸附时的溶液脱色率(η 1)和扣除暗吸附时的溶液脱色率(η 2)表示。
采用日本日立公司S-3400N Ⅱ 扫描电子显微镜, 不同Ag与Br物质的量比催化剂的SEM照片如图1所示。由图1可以看出, 焦钒酸锌呈六方片状, 随着Ag与Br物质的量比增加, 焦钒酸锌表面的小颗粒逐渐增多, 表明负载效果良好, 选择Ag与Br物质的量比为0.20制备AgBr/Zn3(OH)2V2O7· 2H2O催化剂。
固定亚甲基蓝浓度为10 mg· L-1以及溶液原始pH值, 在不同催化剂用量条件下进行光催化降解实验, 结果如图2所示。
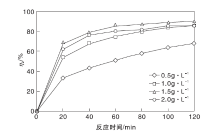 | 图2 催化剂用量对亚甲基蓝溶液脱色率的影响Figure 2 Effects of photocatalyst amounts on decolorization rate of methylene blue solution |
由图2可以看出, 随着催化剂用量增加, 亚甲基蓝溶液脱色率先升后降, 催化剂用量1.5 g· L-1时, 溶液脱色率达到最大; 反应120 min时, 催化剂用量1.0 g· L-1, 溶液脱色率达到85.2%。原因可能是随着催化剂用量增加, 反应体系中能提供的活性点位也增加, 可以产生更多的活性物质降解亚甲基蓝, 脱色率逐渐上升, 但催化剂用量超过一定限度时, 会使溶液浊度增大, 降低可见光穿透能力, 导致溶液脱色率下降。
固定催化剂用量为1.5 g· L-1和溶液原始pH值, 考察亚甲基蓝溶液初始浓度对溶液脱色率的影响, 结果如图3所示。
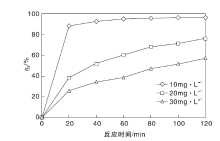 | 图3 不同初始浓度亚甲基蓝溶液的降解曲线Figure 3 Degradation curves of methylene blue solution with different initial concentrations |
由图3可以看出, 随着亚甲基蓝溶液初始浓度提高, 溶液脱色率逐渐降低。可能原因是:(1) 当催化剂用量一定时, 催化剂提供的活性位是固定的, 当亚甲基蓝溶液初始浓度较低时, 需要降解的污染物较少, 可以在短时间内达到较好的脱色效果; (2) 随着亚甲基蓝溶液初始浓度提高, 大量亚甲基蓝分子被吸附在催化剂表面, 占据了催化剂的活性位, 产生的活性物质数量将减少, 不利于反应的进行; (3) 亚甲基蓝溶液初始浓度提高, 降低了溶液的透光性, 不利于光催化反应的进行。
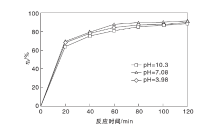
固定催化剂用量为1.5 g· L-1和亚甲基蓝溶液初始浓度10 mg· L-1, 用盐酸溶液和氢氧化钠溶液调节溶液pH值, 进行光催化降解实验, 结果见图4。
从图4可以看出, 光催化效果基本不受亚甲基蓝溶液pH值的影响, 表明催化剂性质较稳定, 在弱酸、中性、弱碱性溶液中均可以表现出良好效果。
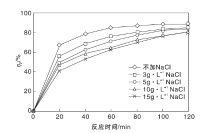
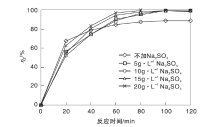
在催化剂用量为1.5 g· L-1、亚甲基蓝溶液初始浓度为10 mg· L-1、溶液原始pH值条件下, 依次加入不同浓度的NaCl和Na2SO4进行光催化降解实验, 结果见图5和图6。
从图5可以看出, NaCl对光催化降解亚甲基蓝具有一定的抑制作用, 随着NaCl浓度提高, 催化剂对亚甲基蓝的吸附性能降低, 原因可能是Cl-与亚甲基蓝分子产生竞争吸附, 导致催化剂对亚甲基蓝吸附能力降低, 进而影响光催化性能。从图6可以看出, Na2SO4对光催化反应起一定的促进作用, 原因可能是硫酸根和亚甲基蓝分子为竞争吸附关系, 因而催化剂对亚甲基蓝的吸附减少, 另外由于硫酸根可以和光生空穴反应生成硫酸根自由基, 而硫酸根自由基氧化能力很强, 能够氧化大多数有机物。
在催化剂用量为1.5 g· L-1、亚甲基蓝溶液初始浓度为10 mg· L-1和溶液原始pH值条件下, 进行光催化降解实验, 每次实验结束将反应溶液静置沉淀后分离, 催化剂在室温下晾干, 作为下一次实验的催化剂, 结果见图7。
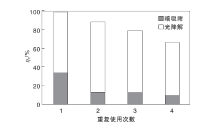 | 图7 光催化剂重复使用次数对光催化性能的影响Figure 7 Effects of recycling times of photocatalyst on photocatalytic performance |
由图7可以看出, 随着催化剂重复使用次数增加, 溶液脱色率逐渐降低。在第4次重复实验结束后, 溶液脱色率仍可达到66.4%, 而光催化脱色率变化较小, 表明溶液脱色主要为催化剂光催化作用。此外, 催化剂对亚甲基蓝的吸附性能随着使用次数的增加有明显下降, 可能是溶液总脱色率η 1降低的原因, 即存在上次重复实验中催化剂表面残留未完全降解的亚甲基蓝或中间产物占据了部分的活性位, 导致催化剂对亚甲基蓝的吸附较少, 从而脱色效果降低。总体来看, 制备的AgBr/Zn3(OH)2V2O7· 2H2O催化剂光催化性能较稳定。
对不同初始浓度亚甲基蓝溶液的光催化降解采用Langmuir-Hinshelwood模型进行动力学分析, 结果见图8和表1。
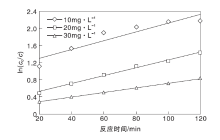 | 图8 不同初始浓度亚甲基蓝溶液的动力学分析Figure 8 Kinetic analysis of methylene blue solution with different initial concentrations |
| 表1 亚甲基蓝溶液的动力学分析数据 Table 1 Kinetic analysis data of methylene blue solution |
由图8和表1可以看出, 随着亚甲基蓝溶液初始浓度升高, 反应速率不断下降, 不同初始浓度亚甲基蓝溶液的光催化降解均符合一级动力学模型。
(1) 前驱液pH=10、120 ℃水热10 h、Ag与Br物质的量比为0.20条件下制备的AgBr/Zn3(OH)2V2O7· 2H2O催化剂, 在可见光下能够有效降解亚甲基蓝溶液, 反应120 min后, 1.0 g· L-1的催化剂对10 mg· L-1亚甲基蓝溶液脱色率达到85.2%。
(2) 随着催化剂用量增加, 溶液脱色率先升后降, 本实验条件下催化剂用量为1.5 g· L-1时, 溶液脱色率最大; 随着亚甲基蓝溶液初始浓度升高, 溶液脱色率呈降低趋势; 亚甲基蓝溶液pH值对光催化降解效果影响不大, 均能保持较高的光催化活性。
(3) NaCl对亚甲基蓝的光催化降解起抑制作用, 而Na2SO4对亚甲基蓝的光催化降解起促进作用。
(4) 随着催化剂重复使用次数增加, 亚甲基蓝总的脱色率下降, 但光催化脱色率基本没有变化, 且光催化脱色在总脱色率中的占比增加, 表明AgBr/Zn3(OH)2V2O7· 2H2O催化剂具有较稳定的光催化活性。
(5) 亚甲基蓝的光催化降解过程符合一级动力学模型, 随着亚甲基蓝溶液初始浓度增大, 反应速率不断下降。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|