作者简介:张启彦,1993年生,女,山东省青岛市人,在读硕士研究生,主要从事光电催化研究。
将钛酸四丁酯与氧化石墨烯/镁铝层状双金属氢氧化物(GO/LDHs)通过水热合成原位生长法制备二氧化钛-氧化石墨烯/镁铝层状双金属氢氧化物(TiO2-GO/LDHs)复合光催化剂,对TiO2、TiO2-GO和TiO2-GO/LDHs的物相结构和表面形态进行表征。模拟太阳光条件下催化剂对有机染料罗丹明B和抗生素四环素的光催化降解效果。结果显示,GO的加入使TiO2颗粒分散的更加均匀,不易团聚。TiO2-GO 对罗丹明B的降解效果优于单一TiO2,表明GO的加入扩展了TiO2的光响应范围,抑制了电子-空穴对的复合。TiO2-GO/LDHs的降解效果优于TiO2-GO,表明LDH捕获光生空穴,加速氧化反应,生成更多的强氧化性羟基,可以更好地降解污染物。
The TiO2-GO/LDHs composite photocatalyst was prepared by hydrothermal synthesis from butyl titanate and graphene oxide/MgAl-layered double hydroxides (GO/LDHs).The phase structure and surface morphology of TiO2,TiO2-GO and TiO2-GO/LDHs were characterized.The photocatalytic degradation activity of catalyst for organic dyes Rhodamine B and antibiotic tetracycline under solar light condition was simulated.The results show that the addition of GO could significantly disperse TiO2.The degradation activity of TiO2-GO for Rhodamine B is better than that of single TiO2,which indicates that the addition of GO enlarges the light response range of TiO2 and inhibits the recombination of electron-hole pairs.The degradation activity of TiO2-GO/LDHs is better than that of TiO2-GO,which indicates that LDHs can capture photogenic holes,accelerate oxidation reaction and produce more strongly oxidized hydroxyl groups,which can better degrade pollutants.
随着大气污染的加剧, 人们对空气质量的要求越来越高, 光催化技术在处理环境问题中的应用迅速发展。在众多光催化剂中, TiO2因稳定性好、催化效率高、无毒无害、廉价易得等特性受到关注, 成为研究热点[1, 2, 3, 4]。但TiO2约为3.2 eV的宽带隙导致其对可见光的利用率低, 并且光生电子-空穴对的高复合等缺陷限制了TiO2的应用。为提高半导体光催化剂的催化活性, 开发出多种方法对光催化剂进行改性, 如离子掺杂法、贵金属沉积法、染料敏化法、半导体复合法以及使用电子传导载流子等[5, 6, 7]。将其他金属和/或半导体与TiO2复合形成光活性异质结, 导致电荷复合减少, 变窄的带隙使光吸收从紫外光向可见光扩展, 是增强TiO2可见光区灵敏度的常用方法[8]。
自2004年英国曼彻斯特大学物理学家安德烈· 海姆和康斯坦丁· 诺沃肖洛夫发现单层石墨烯以来[9], 因其高强度、高透明度、高比表面积、高电荷载流子迁移率以及灵活性和环境稳定性等优越性能而备受追捧, 成为近几年关注的新型碳材料之一, 掀起了应用开发和产业化的热潮[10]。在TiO2和氧化石墨烯(GO)复合过程中, TiO2激发的光生电子可以通过渗流机制从导电带转移到石墨烯, 二维平面π -π 共轭结构使石墨烯有非常优良的电子导电性, 可以有效抑制电子-空穴对的复合[10]。Ti-O-C化学键的形成使TiO2禁带宽度变窄, 在可见光区即表现出光化学活性, 扩展了TiO2的光响应范围[1]。
在环境修复中, 层状双金属氢氧化物(LDH)由于低成本、无毒、易制备, 成为优于其他材料的光催化材料[8]。层状双金属氢氧化物捕获光生空穴生成强氧化性的羟基自由基, 用来降解污染物。其制备方法简单, 实验室条件下可以低成本人工合成[11, 12, 13]。
本文采用水热合成原位生长法制备不同质量比的TiO2-GO/LDHs复合光催化剂, 研究其在模拟太阳光下对有机染料罗丹明B和抗生素四环素的降解效果, 并采用X射线衍射、扫描电子显微镜、高分辨透射电子显微镜、拉曼光谱和紫外-可见分光光度仪等对催化剂进行表征。
钛酸四丁酯, 化学纯, 国药集团化学试剂有限公司; 石墨, 1 200目, 阿拉丁化学试剂有限公司; 六水合硝酸镁、九水合硝酸镁、尿素、无水乙醇、硫酸、盐酸、过氧化氢、高锰酸钾, 分析纯, 国药集团化学试剂有限公司; 实验用水均为超纯水; 氮气, 99.99%。
1.1.1 GO的制备
在200 mL烧杯中加入50 mL浓硫酸, 冰浴条件下加入1 200目石墨粉2 g, 搅拌30 min。缓慢加入7 g的K2MnO4, 搅拌1 h, 升温至35 ℃搅拌2 h。加150 mL去离子水, 95 ℃搅拌30 min。加150 mL去离子水, 滴加30%H2O2直到无气泡产生。趁热过滤, 5%HCl洗涤至加BaCl2无沉淀, 再用去离子水洗涤至pH值接近于7。最后冷冻干燥, 密封保存。
1.1.2 GO/LDHs的制备
0.2 g石墨烯加入80 mL去离子水超声2 h, 加入0.57 g的Mg(NO3)2· 6H2O、1.67 g的Al(NO3)3· 9H2O、0.16 g的尿素超声30 min, 升温至90 ℃搅拌2 h。将混合溶液放入聚四氟乙烯水热罐120 ℃反应12 h, 冷却至室温, 过滤收集底部黑色物质。去离子水和乙醇洗涤数次, 冷冻干燥。
1.1.3 TiO2-GO/LDHs的制备
将7 mL钛酸四丁酯缓慢滴入20 mL无水乙醇, 加入制备好的GO/LDHs(占TiO2质量的2%)得到混合溶液A, 超声30 min。将10 mL去离子水和15 mL无水乙醇混合得到溶液B。将溶液B缓慢滴加到溶液A中, 并持续搅拌。将混合溶液超声30 min, 搅拌15 min, 重复数次至溶液混合均匀。将溶液放入聚四氟乙烯水热罐120 ℃水热12 h, 陈化24 h, 过滤收集底部灰色物质, 冷冻干燥。干燥后的固体颗粒在氮气氛保护下, 500 ℃焙烧2 h, 再水合恢复LDH层状结构。最后, 冷冻干燥得到复合型TiO2-GO/LDHs催化剂。
采用德国布鲁克公司D8 ADVANCEX射线粉末衍射仪对催化剂进行物相分析, 工作电压40 kV, 工作电流40 mA, CuKa, l=0.154 06 nm, 扫描范围5° 80° , 扫描速率10° · min-1。
采用日本日立公司S4800扫描电子显微镜, 加速电压5 kV; 采用日本电子株式会社JEM2100高分辨透射电子显微镜, 加速电压200 kV, 观察催化剂的形貌和晶格结构。
采用日本岛津公司UV-2550紫外分光光度仪, 检测波长(200800) nm。
用紫外分光光度法检测罗丹明B和四环素的浓度。将10 mg四环素溶解于0.1 mol· L-1、10 mL盐酸溶液中, 加水定容至100 mL。称取30 mg光催化剂两份, 分别加至10 mg· L-1、50 mL四环素溶液和10 mg· L-1、50 mL罗丹明B溶液中, 黑暗处理10 min以达到吸附解吸平衡。置于氙灯[最大功率500 W(25 A), 电流15 A]下进行光照。每隔固定时间间隔, 收集约2 mL悬浮液并过滤, 滤液中四环素和罗丹明B的浓度使用紫外分光光度计扫描石英比色皿在(200800) nm的吸光度, 检测波长分别为357 nm[14]和554 nm[15]。根据有机染料和抗生素最大吸收带的吸光度变化, 分析光降解过程[16, 17, 18]。
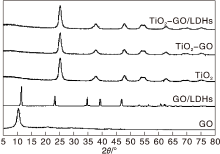
图1为不同催化剂的XRD图。从图1 可以看出, GO/LDHs的复合物中, LDH的衍射峰在11.68° 、23.49° 、34.89° 、39.48° 、46.99° 、60.77° 、62.13° 对应MgAl-LDH的(003)、(006)、(012)、(015)、(018)、(110)、(113)晶面, 与标准化合物的特征峰完全一致(JCPDS:89-5434)。没有观察到石墨烯的特征峰, 推测是由于LDH插层进入石墨烯之间, 使石墨烯片间距增大, 形成单层石墨烯, 10.6° 的氧化石墨烯峰消失[4]。TiO2的衍射峰在25.30° 、37.79° 、48.04° 、53.88° 、55.07° 、62.69° 对应锐钛矿相TiO2的(101)、(004)、(200)、(105)、(211)、(204)晶面, 没有观察到金红石相TiO2的晶面。通过在锐钛矿相TiO2(200)衍射峰上应用谢乐公式计算出平均晶体尺寸约为11 nm。加入GO或GO/LDHs后, TiO2的特征峰基本没有改变, 结晶性较好。
图2为GO、GO/LDHs、TiO2、TiO2-GO/LDH的SEM照片。从图1(a)中可以清楚的看到石墨烯的皱褶结构, 其巨大的比表面积可以提供更多的活性位点。GO/LDHs复合物中可以看见规则的六边形结构(b), 表明生成了LDH, 尺寸约为500 nm。水热法合成的TiO2的粒径尺寸为(1015)nm(c), 与XRD的 计算结果一致。从图1(d)中可以看到TiO2均匀的分散在石墨烯周围[19], 石墨烯的加入有效的限制了TiO2的团聚, 提高反应物和催化剂的接触面积, 从而提高降解效率。
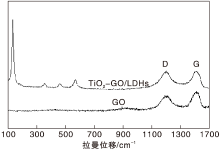
对于石墨烯而言, 拉曼光谱是测定其微观结构特征的有效工具[8]。图3为GO和TiO2-GO/LDH的拉曼光谱。
从图3可以看出, 石墨烯出现两个明显的拉曼峰, G带在1 598 cm-1处, D带在1 357 cm-1处, 分别来源于sp2原子对的伸缩振动和缺陷。与GO的ID/IG值(0.91)相比, TiO2-GO/LDHs的ID/IG值增加到1.02, ID/IG值通常表示石墨材料中sp2杂化的无序程度和平均尺寸, 比值越高, 石墨相的缺陷程度越高[20, 21]。与GO相比, TiO2-GO/LDHs的ID/IG值增加, 表明平面内的sp2区域尺寸减小, 石墨氧化物中氧官能团减少, 氧化石墨烯被还原, 生成还原氧化石墨烯(RGD)。对于TiO2, 由于锐钛矿相的Eg振动模式, 通常在143 cm-1处观察到独立的锐钛矿相TiO2纳米颗粒的尖锐拉曼散射峰。195 cm-1、395 cm-1、512 cm-1和640 cm-1处的峰值对应于锐钛矿相TiO2的不同振动模式[22, 23]。总体而言, 拉曼光谱表明纳米复合物含有RGO和TiO2, 与XRD结果一致。
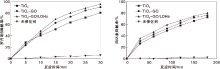
图4显示了在模拟太阳光条件下, GO、TiO2-GO、TiO2-GO/LDHs对罗丹明B 和四环素的光催化降解效果, 以不放催化剂时的降解情况作为对照组。罗丹明B的反应时间为30 min, 每间隔5 min取样一次。四环素的反应时间为180 min, 每间隔30 min取一次样。
从图4可以看出, 不加催化剂时, 罗丹明B降解率仅7%, 四环素降解率仅4%。TiO2-GO在反应30 min后, 对罗丹明B的降解率为91.6%, 反应180 min后, 对四环素的降解率为76%, 优于纯TiO2(81.4%和73.6%)。表明加入GO后, TiO2激发的光生电子从导电带转移到石墨烯上, 抑制了TiO2电子-空穴对的复合, 光催化性能得到提升。TiO2-GO/LDHs对罗丹明B和四环素的降解率进一步增加, 分别达到95.8%和79.6%。表明LDH通过捕获光生空穴, 使电子-空穴对的复合率进一步减小, 生成更多的羟基自由基以降解有机物。
(1) 采用水热合成原位生长法合成了TiO2-GO/LDHs复合光催化剂。XRD结果表明, GO/LDHs的加入对TiO2的结晶度没有明显影响。SEM显示, GO的加入使颗粒物分散更加均匀。
(2) 通过对罗丹明B及四环素的降解, 评价了TiO2-GO/LDHs复合物的光催化降解性能。结果发现, TiO2-GO/LDHs复合光催化剂的光催化性能优于TiO2-GO及纯TiO2, 表明GO/LDHs的加入通过加快TiO2激发的光生电子转移的速率和捕获空穴抑制了光生电子-空穴对的复合, 产生更多降解污染物的羟基自由基。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|