作者简介:张雨萌,1992年生,女,山西省运城市人,硕士,研究方向为环境催化。
采用共沉淀法制备锌铝水滑石,在此基础上分别考察空气和氨气气氛焙烧的类水滑石衍生复合氧化物(LDO)对羰基硫(COS)水解的催化性能。通过氮气吸附-脱附、X光电子能谱(XPS)、X射线衍射(XRD)和程序升温脱附(TPD)等表征手段对催化剂的结构和物化性能进行了系统研究。结果表明,N掺杂LDO增加了材料的碱强度和碱量,减少了表面氧物种OS的含量,提高了材料的稳定性和硫容。反应连续进行1 200 min,COS转化率仍能保持96%。
Zinc-aluminum hydrotalcite was prepared by co-precipitation method.The catalytic hydrolysis performance of carbonyl sulfide (COS) over composite oxides (LDO) derived from zinc-aluminum hydrotalcite by calcining under air and NH3 was investigated.The structure and physic-chemical properties of the catalysts were characterized by the N2 adsorption-desorption measurement,X-ray photoelectron spectroscopy(XPS),X-ray diffraction(XRD),temperature-programmed desorption(TPD) and so on.For N-doping catalyst,the improved catalytic performance(activity,stabitily and sulfur capacity) was due mainly to the decrease of the amount of O species on the surface(OS) and the enhanced basicity.The COS conversion could be attained as high as 96% even after 1 200 min of reaction.
羰基硫化物也称为硫化碳、氧硫化碳, 是一种无色无味的有毒可燃气体, 广泛存在于煤炭、石油化工等行业的工业气体中, 是有机硫的主要赋存形式。在工业生产中, 原料气中的硫化物往往会造成管道设备的腐蚀损耗以及催化材料的中毒失活。此外, 未经有效处理排放的COS不仅会危害人体健康, 还会对大气环境造成严重的影响。
催化水解法因具有反应温度低、适用温域宽、效率高以及能耗低等优点而成为目前工业上应用最为广泛的COS脱除技术。近年来国内开发的COS的水解催化剂主要针对于各种煤制气、化工原料气的脱硫净化, 对于常低温下含低浓度COS的气体处理效果良好。但随着高硫煤以及高硫石油焦造气的逐步开发应用, 工业气体中COS的浓度峰值时常高达1000× 10-6, 对于这样的气体, 多数COS水解催化剂往往在很短的时间内即中毒失活[1]。因此, 开发一种能在常低温下高效稳定处理高浓度COS的水解催化剂具有重要的现实意义。
水解催化剂一般以Al2O3、TiO2为主要组分, 并浸渍一定量的碱金属、碱土金属或过渡金属作为活性组分。而目前共认的脱硫精度最高的脱硫剂是氧化锌, 经氧化锌脱硫剂处理过的原料气硫含量可以达到1× 10-9。文献报道二价和三价金属对类水滑石衍生复合氧化物(LDO)催化剂的硫容量有显著影响, 可改变催化剂的稳定性[2, 3]。基于此, 本文采用共沉淀方法制备锌铝水滑石。COS水解反应为碱催化反应, 催化剂的碱性很大程度上决定了催化剂的活性, 且其活性中心为弱和中等强度的碱位, 因此采用适当的碱修饰方法可以增加催化剂的碱性位, 提高催化剂的活性和稳定性。基于上述, 用NH3焙烧锌铝水滑石对材料进行碱改性形成氮掺杂的复合氧化物, 考察NH3改性对材料的结构、物化性质和COS水解催化性能的影响。
Al(NO3)3· 9H2O、Zn(NO3)2· 6H2O、NaOH和Na2CO3均为分析纯, 国药集团化学试剂有限公司。将0.02 mol的Al(NO3)3· 9H2O和0.06 mol的Zn(NO3)2· 6H2O溶于200 mL去离子水中, 配成溶液A; 将6.4 g NaOH及1.06 g Na2CO3溶于200 mL去离子水中, 配成溶液B; 室温下, 将溶液A、B缓慢滴入搅拌的200 mL去离子水中, 保持pH=10.0~10.5, 连续搅拌反应3 h, 室温下老化过夜; 然后过滤, 并用去离子水洗涤至滤液pH呈中性, 70 ℃下干燥12 h, 120 ℃下干燥12 h, 得到锌铝水滑石前驱体, 标记为ZnAl-LDH; 最后将水滑石前驱体分别置于空气或NH3气氛中, 并在450 ℃下煅烧4 h。将空气和NH3气氛中焙烧后的产物分别标记为ZnAl(A)LDO和ZnAl(N)LDO。
采用石英管固定床反应器, 在常压和90 ℃下进行COS的水解反应。(40~60)目催化剂装填量0.5 mL, 原料气中含COS 1000× 10-6, 水蒸汽1 200× 10-6, N2为平衡气, 流速50 mL· min-1。出口COS、H2S和CO2浓度由气相色谱仪(Agilent 7890B)进行测定。
采用X射线衍射(XRD, X'Pert3 Powder X)对样品物相进行分析, CuKα , 波长0.154 nm, 工作电压和电流分别为40 kV和40 mA。
样品比表面积、孔体积和孔径分布在Micromeritics ASAP 2020气体吸附仪上测试, 测定前样品在300 ℃下真空脱气3 h, 比表面积(SBET)根据BET方法计算得到, 孔分布根据BJH方法计算。
材料的CO2程序升温脱附(CO2-TPD)在Micromeritics Auto Chem 2720型程序升温仪上进行, 50 mg催化剂在He气氛(流速50 mL· min-1)中以10 ℃· min-1的速率升至400 ℃并保持1 h, 而后采用He气吹扫并冷却至室温, 切换至CO2/He混合气(CO2体积分数为20%, 50 mL· min-1)吸附1 h, 最后在He气流(50 mL· min-1)下, 以10℃· min-1的速率升至900℃。
采用X光电子能谱(XPS, Escalab250Xi)测定催化剂表面组成及化学状态, 选用Al Kα X射线为激发源, 光电子能谱以碳的结合能284.8 eV为基准进行校正。
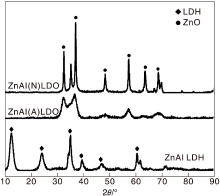
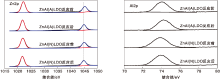
为了研究N掺杂对催化剂结构的影响, 对锌铝水滑石和不同气氛下煅烧的催化剂进行了XRD表征, 结果见图1。从图1可以看出, 未煅烧的锌铝水滑石(ZnAl-LDH)XRD图中出现2θ =11.6° , 23.3° , 35.5° , 39.7° , 47.6° 和60.4° 的特征峰, 这些特征峰分别对应于水滑石(PDF#48-0594)的003, 006, 009, 010, 018和112晶面, 说明成功制备出了ZnAl-LDH。经过空气煅烧后的样品ZnAl(A)LDO的XRD图中ZnAl-LDH的特征峰消失, 而出现了ZnO的特征峰。而ZnAl(N)-LDO的XRD图中2θ =35.0° 归属于ZnAl-LDH, 2θ =32.1° , 36.5° , 47.8° , 57.1° , 63.1° 和68.5° 的衍射峰分别对应ZnO(PDF#75-0576)的100, 101, 102, 110, 103和112晶面。所有样品中均未出现Al2O3的特征峰。对比ZnAl(A)LDO和ZnAl(N)LDO的XRD图可知, ZnAl(N)LDO仍然保留2θ =35.0° 处ZnAl-LDH的特征峰。
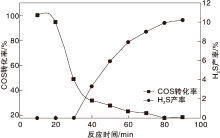
在反应温度90 ℃和空速6 000 h-1的条件下, ZnAl(A)LDO对COS水解的催化性能见图2。
从图2可以看出, COS初始转化率接近100%, 随着反应的进行, COS转化率显著降低, 反应20 min时COS转化率降到94%, 90 min时COS转化率只有19%。而产物H2S的产率初始30 min为0, 随着反应进行, 产率逐渐升高, 90 min时达到10%。由图2可知ZnAl(A)LDO的稳定性较差, 90 min内活性降低了81%。文献报道通过碱处理可以增加催化剂的稳定性[4]。因此, 本研究采用NH3对锌铝水滑石进行处理得到氮掺杂的ZnAl(N)LDO。相同反应条件下氮掺杂的ZnAl(N)LDO对COS水解的催化性能如图3所示。
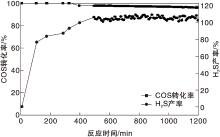
从图3可以看出, COS初始转化率接近100%, 并维持330 min。之后COS转化率开始逐渐降低。反应进行1 200 min时, COS转化率仍能维持在96%。与空气煅烧的ZnAl(A)LDO相比, 氮掺杂的ZnAl(N)LDO稳定性显著提高。最初30 min内, H2S在NH3改性的ZnAl(N)LDO催化剂上的产率基本为0, 在50 min内H2S产率迅速增加到64%。之后随着反应时间的增加, H2S产率逐渐增加到接近100%。在390 min时, COS转化率和H2S产率基本相等。通过对比发现, 经过NH3处理催化剂的活性和稳定性显著提高。
图4为不同样品的N2等温吸附-脱附曲线和孔径分布图。从图4可以看出, 煅烧后的样品等温吸附曲线都属于具有H3型回滞环的吸附曲线, 没有明显的饱和吸附平台, 表明孔结构很不规整, 由片状颗粒材料或由裂隙孔材料给出[5]。从孔径分布图中可知, 两种样品的孔径分布都较宽, 说明其孔道大小都不均匀。其中, ZnAl(A)LDO的孔径比ZnAl(N)LDO分布更宽, 说明ZnAl(A)LDO的孔道大小极不均匀, 且多数分布在(20~60) nm。ZnAl(N)LDO的孔径最广泛分布在25 nm。表1为样品的比表面积和孔结构数据。从表1可以看出, 氨气焙烧得到的ZnAl(N)LDO具有更大的比表面积和孔容, 粒径更小, 可暴露更多的活性位, 因而在水解反应过程中显示出较高的活性。
 | 图4 不同样品的N2等温吸附-脱附曲线和孔径分布图Figure 4 Isothermal adsorption-desorption curves and pore size distribution of samples |
| 表1 样品的比表面积和孔结构数据 Table 1 Specific surface area and pore-structure of samples |
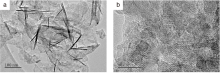
图5为样品ZnAl(A)LDO的TEM照片。
图6为样品ZnAl(N)LDO的TEM照片。与样品ZnAl(A)LDO相比, 氮掺杂能改变ZnAl-LDO的形貌。
样品表面的化学组成及元素化学状态采用XPS进行表征, 结果见图7。在Zn2p轨道的XPS图谱中, 2p3/2对应的是1 021.8 eV, 2p1/2对应的是1 044 eV, 对应于XPS手册中Zn在ZnO中的结合能。在Al2p轨道的XPS图谱中, 结合能74.4 eV对应于XPS手册中Al在Al2O3中的结合能。 与ZnAl(A)LDO相比, ZnAl(N)LDO的Zn2p的结合能向高结合能方向移动, Al2p的结合能向低结合能方向移动; 所有反应后的样品Zn2p和Al2p的结合能都向高结合能移动。
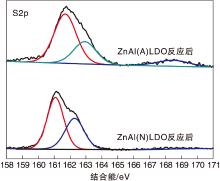
图8为ZnAl(A)LDO和ZnAl(N)LDO反应后样品的S2p XPS谱图。在两种样品反应后的S2p XPS谱图中出现的谱峰分别为硫化物[(161.4± 0.2) eV], S8[(163.5± 0.2) eV]和硫酸盐[(169.7± 0.2) eV]。分析结果发现, 反应后的ZnAl(A)LDO表面上存在硫化物、S8和硫酸盐, 而反应后的ZnAl(N)LDO表面上只检测到了硫化物和S8, 表明在ZnAl(N)LDO催化剂上, 氧物种的大量减少, 从而证明氮对氧的取代。
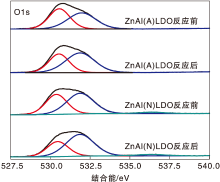
硫沉积是COS水解催化剂失活的主要原因[7]。而材料表面氧物种的状态及其氧化还原性质很大程度上决定了COS和H2S生成沉积的S物种的反应[8]。图9为O1s 的XPS光谱图。O1s XPS光谱可以拟合成结合能为(530.5± 0.2) eV和(532.0± 0.2) eV的两个峰, 分别代表晶格氧(OL)和表面活性氧(OS)。氨气焙烧后的样品晶格氧和表面氧均减少。结合表2, 样品表面组成中测到N元素可以推测出, 氮成功掺杂到了材料的体相中。
| 表2 样品的表面原子组成 Table 2 Surface atomic composition of samples |
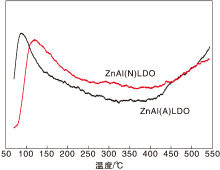
COS的水解反应活性中心为弱和中等强度碱性中心, 因此催化剂的碱性影响其催化活性[9]。图10为催化剂的CO2-TPD。
从图10可以看出, 脱附温度在(100~150) ℃为弱碱性位, (200~300) ℃对应中等强度的碱性位。图中CO2的脱附信号可认为是弱碱性位。氨气焙烧会提高碱性位的强度, 增加碱性位点。因此提高了催化反应的活性与稳定性。
采用共沉淀法分别制备了ZnAl(A)LDO和ZnAl(N)LDO催化剂, 并测试了两种催化剂催化羰基硫水解反应性能。结果表明, 在ZnAl(A)LDO的催化作用下, COS初始转化率接近100%, 但很快失活; 在ZnAl(N)LDO的催化作用下, 反应进行1 200 min后, COS转化率仍能保持96%。ZnAl(N)LDO的催化反应过程, 消耗掉大量的表面羟基, 而ZnAl(A)LDO的催化反应过程, 消耗掉催化剂中的氧物种, 因此两种催化剂生成不同的硫物种沉积在催化剂的表面。结果表明, 通过NH3改性的可以大幅度提高催化剂的稳定性。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|