作者简介:杨志翔,1990年生,男,硕士,研究实习员,主要从事有机分析检测研究。E-mail:312179959@qq.com
探究合成羟甲基吡喃酮衍生物的方法,用BINOL硫脲(Ⅰ~Ⅳ)催化四氢吡喃酮与苯甲醛的不对称Aldol反应,简单、高效催化合成羟甲基吡喃酮衍生物,并考察催化剂的催化性能。结果表明,以Ⅱ( X=10%)为催化剂,CH2Cl2为溶剂,于10 ℃反应,合成的羟甲基吡喃酮衍生物有较好的收率(最高达82%)和较高的对映选择性(最高为86% ee)。
The highly efficient method of synthesizing hydroxymethylpyranone derivatives was explored.In the asymmetric Aldol reaction of tetrahydropyranone and benzaldehyde catalyzed by BINOL thiourea(Ⅰ~Ⅳ),the hydroxymethylpyranone derivatives were synthesized ordinarily and efficiently,and the performance of the catalyst was also investigated.The results show that the hydroxymethylpyranone derivatives has good yield(up to 82%) and high enantioselectivity(up to 86% ee) when the catalyst is Ⅱ( X=10%) under the conditions of 10 ℃ in the solvent CH2Cl2.
在现代有机合成反应中, 构建C-C键的方式很多, 其中不对称Aldol反应是最有效的方法之一。其反应产物β -羟基羰基化合物应用广泛, 尤其在医药生产中有很重要的应用[1, 2, 3, 4, 5]。硫脲作为有机合成中结构单元的一部分, 在杂环骨架的合成中有着广泛的应用[6, 7]。硫脲作为一种氢键供体型的有机小分子催化剂, 其反应机理是通过与底物形成氢键来活化反应试剂, 从而起到催化反应的作用[8]。1998年, Sigman M S等[9]初次报道用含有硫脲结构的化合物催化不对称Strecker反应。随后的发展, 形成了脯氨酸衍生的硫脲类[10, 11, 12]、环己二胺衍生的硫脲类[13, 14, 15]、金鸡纳生物碱衍生的硫脲类[16, 17]为主的硫脲类催化剂, 应用非常广泛。合成的硫脲类化合物作为催化剂并且应用于各种不对称催化反应中, 取得了令人满意的效果。
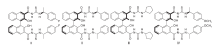
在之前的研究中, 本课题组进行设计并且修饰了(R)-BINOL骨架的3, 3'位置, 通过酰化、取代和加成反应得到硫脲类衍生物, 应用于Sulfa-Michael/Aldol串联反应[18, 19]和Biginelli反应[20]中, 取得很好的催化效果。本文通过修饰BINOL骨架, 合成4种双活性中心、多氢键的对称性双硫脲催化剂(Ⅰ ~Ⅳ , 图1), 用于催化四氢吡喃酮和苯甲醛的不对称Aldol反应, 同时高效合成羟甲基吡喃酮衍生物(图3)。
Unity-400型核磁共振仪, 溶剂为CDCl3(除非特别说明), 内标为四甲基硅烷(TMS); 德国布鲁克公司TENSOR27型傅里叶变换红外光谱仪, KBr压片; WZZ-1型旋光仪; X-6数字显示微熔点测定仪; UHR TOF LC/MS Mass Spectrometer型超高分辨飞行时间质谱仪; LC2000型高效液相色谱仪, 色谱柱为Chiralpak OD-H手性柱, 流动相:V(正己烷):V(异丙醇)=85:15, 流速1.0 mL· min-1, 检测波长254 nm。所用试剂均为分析纯。
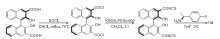
(R)-BINOL-3, 3'-二甲酸按照文献[21, 22, 23]合成, 然后经过酰化反应、取代反应和加成反应得到目标产物Ⅰ ~Ⅳ [24], 见图2。
分别取(R)-BINOL-3, 3'-二甲酸(0.30 g, 0.8 mmol)、SOCl2(0.2 g, 1.6 mmol)缓慢放入至250 mL圆底烧瓶中, 加入40 mL纯化过的CHCl3, 在磁力搅拌下升温至70 ℃, 充分回流, 6 h后, 观察气体完全逸出(氢氧化钠稀溶液吸收尾气), 薄层色谱法检测, 旋转蒸发、浓缩, 得到酰化反应产物。
把100 mL圆底烧瓶置于磁力搅拌器上, 依次加入KCNS(0.2 g, 2 mmol)、PEG-400和40 mL纯化的CH2Cl2, 搅拌, 使PEG-400均匀分散, 把酰化产物(R)-BINOL-3, 3'-二甲酰氯全部溶解于20 mL纯化的CH2Cl2溶液中, 借助恒压滴液漏斗缓慢滴加到溶有KCNS的CH2Cl2溶液中, 过程需要7 min。继续搅拌, 薄层色谱法检测反应, 直到沉淀生成。浓缩, 得黄色固体。
加入20 mL的THF溶解上一步所得的黄色固体, 置于250 mL三口烧瓶中直至全部溶解, 同时容器内充满氮气, 加入(R)-(-)-1-(4-氟苯基)-乙胺(0.24 g, 1.6 mmol), 冰浴条件下反应12 h, 薄层色谱法检测反应完成, 蒸发、浓缩, 柱层析纯化[洗脱剂:V(石油醚):V(乙酸乙酯)=10:1], 得黄色固体Ⅰ , 收率为70%。
以同样的方法合成Ⅱ ~Ⅳ 。
催化剂的表征:
Ⅰ :淡黄色固体, Yield 70%, m.p.(226.8~234.3) ℃, [α
Ⅱ :淡黄色固体, Yield 60%, m.p.(224.5~231.2) ℃, [α
Ⅲ :淡黄色固体, Yield 68%, m.p.(236.3~241.4) ℃, [α
Ⅳ :淡黄色固体, Yield 79%, m.p.(201.1~205.2) ℃, [α
羟甲基吡喃酮衍生物的合成路线如图3所示。
依次称取四氢吡喃酮(0.113 g, 1.250 mmol)、苯甲醛1a (0.027 g, 0.250 mmol), 催化剂Ⅱ (X=10%), HOAc(X=10%)和2 mL的CH2Cl2置于50 mL圆底烧瓶中, 10 ℃条件下磁力搅拌。24 h后减压蒸馏, 柱层析纯化[洗脱剂:V(石油醚):V(乙酸乙酯)=7:1], 得淡黄色固体2a。收率为柱层析分离后的收率, 对映选择性使用Chiralpak OD-H柱的HPLC分析测定。
用同样的实验方法合成2b~2m。表征如下:
2a:Yield 79%, 80%ee, [HPLC, tR=9.12 min(次), tR=21.04 min(主)]; 1H NMR(400 MHz, CDCl3), δ :0.88~1.26(d, J=15.2 Hz, 2H), 1.86(m, 1H), 2.50~2.90(d, J=10.4, Hz, 2H), 3.58(d, J=11.2 Hz, 2H), 4.00(m, 2H), 4.89 (m, 1H), 7.27~7.53(t, J=13.6 Hz, 3H), 8.16(d, J=4.8 Hz, 1H)。13C NMR(100 MHz, CDCl3), δ :43.68, 58.08, 68.34, 70.93, 72.22, 125.53, 125.88, 128.44, 129.35, 134.25, 140.21, 210.01。
2b:Yield 81%, 86%ee, [HPLC, tR=11.02 min(次), tR=21.12 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.13 (s, 2H), 1.41(s, 1H), 2.15(m, 3H), 2.96(d, J=8.0 Hz, 2H), 3.49(m, 1H), 5.44(d, J=8.4 Hz, 1H), 7.48(m, 1H), 8.39(s, 2H).13C NMR(100 MHz, CDCl3), δ :43.99, 49.77, 55.67, 67.25, 69.55, 124.25, 128.11, 130.55, 133.24, 138.52, 147.23, 206.99。
2c:Yield 78%, 82%ee, [HPLC,
2d:Yield 77%, 85%ee, [HPLC, tR=10.49 min(次), tR=21.20 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.09(d, J=8.2 Hz, 2H), 2.02(s, 1H), 2.56(m, 2H), 3.05(m, 3H), 3.99(m, 2H), 5.27(m, 1H), 7.40(d, J=13.6 Hz, 2H), 8.23(m, 1H); 13C NMR(100 MHz, CDCl3), δ :44.83, 46.50, 57.05, 67.31, 68.21, 69.78, 123.84, 123.88, 126.75, 129.55, 148.77, 208.45。
2e:Yield 80%, 83%ee, [HPLC, tR=9.79 min(次), tR=19.86 min(主)]; 1HNMR(400 MHz, CDCl3), δ :1.41(t, J=10.4 Hz, 1H), 2.55(m, 1H), 2.85(s, 1H), 3.33(dd, J=12.3 Hz, 1H), 3.74(m, 2H), 3.93(m, 1H), 4.17(s, 1H), 5.76(m, 1H), 7.01(m, 3H), 7.42(d, J=8.4 Hz, 1H); 13C NMR(100 MHz, CDCl3), δ :43.89, 57.48, 67.70, 68.23, 70.32, 112.79, 114.44, 120.97, 131.39, 143.56, 164.19, 208.71。
2f:Yield 78%, 82%ee, [HPLC, tR=13.82 min(次), tR=21.68 min(主)]; 1HNMR(400 MHz, CDCl3), δ :1.07(m, 1H), 1.63(s, 2H), 2.60(m, 1H), 2.87(s, 1H), 3.37(d, J=4.0 Hz, 1H), 3.72(m, 2H), 4.06(d, J=10.4 Hz, 1H), 5.41(m, 1H), 7.06(s, 1H), 7.28(d, J=8.0 Hz, 2H); 13C NMR(100 MHz, CDCl3), δ :44.04, 57.69, 68.40, 69.86, 70.88, 115.55, 127.03, 127.87, 128.42, 129.97, 136.34, 208.88。
2g:Yield 71%, 72%ee, [HPLC, tR=11.84 min(次), tR=22.98 min(主)]; 1H NMR(400 MHz, CDCl3), δ :2.43(d, J=11.2 Hz, 3H), 2.87(s, 2H), 3.81(m, 2H), 4.15(s, 1H), 4.83(d, J=5.6 Hz, 1H), 5.38(s, 1H), 7.11~7.20(d, J=6.8 Hz, 3H), 7.89(s, 1H).13C NMR(100 MHz, CDCl3), δ :21.46, 43.32, 58.38, 68.35, 70.97, 72.22, 115.87, 123.52, 126.68, 128.49, 130.36, 138.55, 210.19。
2h:Yield 76%, 77%ee, [HPLC, tR=11.25 min(次), tR=20.51 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.28(m, 1H), 2.54(m, 2H), 2.85(s, 1H), 3.37(dd, J=6.8, 10.8 Hz, 2H), 3.88(d, J=12.4 Hz, 3H), 4.14(s, 1H), 4.85(m, 1H), 5.38(d, J=4.8 Hz, 2H), 6.97(d, J=7.6 Hz, 2H), 7.27(d, J=3.2 Hz, 1H)。13C NMR(100 MHz, CDCl3), δ :43.11, 55.30, 56.96, 68.40, 70.88, 113.63, 120.98, 121.02, 126.80, 130.97, 159.64, 164.35, 208.77。
2i:Yield 81%, 83%ee, [HPLC, tR=15.23 min(次), tR=23.95 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.26(m, 2H), 2.51(d, J=4.8 Hz, 4H), 3.98(t, J=6.2 Hz, 3H), 4.12(s, 1H), 5.07(m, 1H), 6.61(d, J=5.6 Hz, 1H), 7.44(d, J=12.8 Hz, 1H); 13C NMR(100 MHz, CDCl3), δ :29.71, 42.91, 65.17, 67.96, 68.51, 112.70, 117.74, 121.25, 129.93, 145.61, 152.82, 207.66。
2j:Yield 82%, 82%ee, [HPLC, tR=14.32 min(次), tR=26.54 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.30(m, 1H), 2.30(m, 1H), 2.59(d, J=3.2 Hz, 1H), 2.83(s, 1H), 3.36(s, 1H), 3.78(t, J=6.4 Hz, 3H), 4.16(s, 1H), 5.61(m, 1H), 6.98(m, 1H), 7.19(s, 1H), 7.47(s, 1H); 13C NMR(100 MHz, CDCl3), δ :42.71, 58.55, 68.59, 69.63, 72.86, 122.30, 127.42, 128.40, 134.49, 136.55, 139.24, 209.73。
2k:Yield 73%, 79%ee, [HPLC, tR=10.89 min(次), tR=21.54 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.26(s, 2H), 1.68(m, 2H), 2.23(d, J=10.0 Hz, 1H), 2.51(s, 2H), 2.72(s, 1H), 3.80(s, 1H), 3.98(s, 2H), 4.74(dd, J=3.6, 4.8 Hz, 1H), 8.05(m, 1H).13C NMR(100 MHz, CDCl3), δ :29.72, 41.99, 42.86, 67.91, 69.51, 126.62, 130.11, 132.21, 133.01, 133.75, 134.60, 208.80。
2l:Yield 72%, 85%ee, [HPLC, tR=11.19 min(次), tR=22.23 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.17(s, 2H), 1.26(m, 2H), 2.61(d, J=7.60 Hz, 1H), 3.98~4.31(m, 2H), 4.83(s, 1H), 7.23~7.99(d, J=5.6 Hz, 3H), 7.96(d, J=5.6 Hz, 2H); 13C NMR(100 MHz, CDCl3), δ :29.31, 41.58, 49.79, 66.32, 70.33, 129.11, 130.98, 133.06, 132.32, 135.41, 136.86, 208.50。
2m:Yield 69%, 77%ee, [HPLC, tR=15.04 min(次), tR=23.39 min(主)]; 1H NMR(400 MHz, CDCl3), δ :1.24(s, 1H), 1.99(s, 1H), 2.55(dd, J=8.0 Hz, 1H), 2.94(d, J=4.4 Hz, 2H), 3.48(s, 2H), 3.79(m, 1H), 4.22(d, J=5.6 Hz, 2H), 5.48(m, 1H), 7.38(m, 1H), 7.67(s, 1H)。13C NMR(100 MHz, CDCl3), δ :44.65, 50.88, 67.54, 68.23, 71.49, 111.40, 118.30, 127.25, 127.41, 132.35, 132.51, 148.71, 208.29。
考察BINOL硫脲类催化剂种类及其用量对合成羟甲基吡喃酮衍生物的影响。在10 ℃时, CH2Cl2作溶剂, 四氢吡喃酮与苯甲醛(1a)的不对称Aldol反应时间为24 h, 对催化剂(Ⅰ ~Ⅳ )的催化性能进行比较, 结果见表1。由表1表明, 在相同反应条件下, 4种轴手性BINOL硫脲催化合成羟基吡喃酮衍生物, 具有高效的催化效果, 得到中等收率(61%~82%ee)和对映选择性(65%ee~86%ee)。虽然都能得到羟基吡喃酮衍生物, 但催化效果不同, 其中Ⅲ 催化剂上的收率和对映选择性最低, Ⅱ 催化上的收率及对映选择性相对较高, Ⅰ 催化剂上的收率虽然高, 但对映选择性较低; 当催化剂Ⅱ 的用量从5%增加到20%时, 收率依次增加, 但对应选择性增加不明显, 所以选择催化剂用量X=10%。
| 表1 催化剂种类及其用量的筛选 Table 1 Screening of catalysts and its dosage |
4种催化剂中, Ⅰ 、Ⅱ 、Ⅳ 都是双手性中心, Ⅲ 是单手性中心-轴手性, 其催化效果明显不一样。原因可能是Ⅱ 是所用手性胺苯环上无取代基, 相比于Ⅳ 的苯环对位上的给电子基团, 催化效果较好, 催化剂Ⅰ 所用的手性胺苯环对位上有氟原子取代基, 氟原子的强吸电子作用抑制了催化剂的催化活性, 因此对映选择性不高; Ⅲ 只有单手性-轴手性, 其收率和对位选择性更低。从原子经济性和催化性能考虑, 选取催化剂Ⅱ , 催化剂用量X=10%。
选取催化剂Ⅱ , 催化剂用量X=10%, 考察溶剂和反应温度对合成产物羟甲基吡喃酮衍生物的影响, 结果见表2。
| 表2 反应温度和溶剂对反应的影响 Table 2 Effect of reaction temperature and solvent on the reaction |
由表2可以看出, 相同条件下, 以CH2Cl2作溶剂时, 收率和对映选择性最高。而以乙醚、乙醇、四氢呋喃、N, N-二甲基甲酰胺为溶剂, 收率和对映选择性均较低; 甲苯中有不饱和键, 用其作为反应溶剂时效果不佳。用CH2Cl2作溶剂, 升高反应温度至20 ℃时, 合成的产物羟甲基吡喃酮衍生物收率和对映选择性明显降低; 降低反应温度至0 ℃, 产物羟甲基吡喃酮衍生物收率和对映选择性也没有增加。综合考虑, 确定反应温度为10 ℃, CH2Cl2作为溶剂。
在最优的实验条件即以Ⅱ (X=10%)为催化剂, CH2Cl2为溶剂, 于10 ℃反应, 合成羟甲基吡喃酮衍生物2a~2m, 结果见表3。
| 表3 最优实验条件下合成羟甲基吡喃酮衍生物 Table 3 Synthesis of hydroxymethylpyranone derivatives under optimal experimental conditions |
由表3可以看出, 在催化剂Ⅱ 作用下, 四氢吡喃酮和苯甲醛及衍生物的反应, 都能高效地进行不对称Aldol反应, 有较高的收率(69%~82%)和较高的对映选择性(72%ee~86%ee)。尽管苯甲醛及其衍生物苯环上的取代基种类不同, 但反应都能高效地进行, 表明催化剂的普适性很好; 苯甲醛苯环上取代基的能力作用不同, 产物的收率和对映选择性也不同, 充分说明取代基的取代能力对不对称直接Aldol反应有着重要的影响, 电负性较大的卤素种类与位置不同, 合成的羟甲基吡喃酮衍生物结果也不同。
(1) 合成了BINOL硫脲衍生物, 作为催化剂应用于四氢吡喃酮与苯甲醛的不对称Aldol反应中。在反应温度10 ℃, CH2Cl2作溶剂, Ⅱ (X=10%)为催化剂中, 扩充了四氢吡喃酮和苯甲醛及其衍生物的反应底物, 得到收率高达82%和对映选择性高达86%的羟甲基吡喃酮衍生物2a~2m。
(2) 该方法具有反应操作简单、原子经济等优点。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|