作者简介:曹小华,1994年生,女,陕西省延安市人,在读博士研究生。
采用等体积浸渍法制备La、Ce改性的MCM-41催化剂,考察不同稀土金属元素对甲硫醇催化分解活性位点的调控作用。采用N2吸附-脱附、XRD、XPS、H2-TPR和NH3/CO2-TPD等对La、Ce改性催化剂进行物理化学性能测试,确定稀土元素La、Ce在催化剂中存在的形态和作用。研究表明,甲硫醇催化分解存在两步反应,低温条件下甲硫醇催化分解生成甲硫醚中间体,高温条件下甲硫醚进一步催化分解生成硫化氢和甲烷等小分子产物。对于10%Ce/MCM-41催化剂,表面活性氧是甲硫醇催化分解的低温活性中心,强酸性位点是甲硫醇催化分解的高温活性中心,二者在反应中起协同催化作用,而对于10%La/MCM-41催化剂,强酸性位点是甲硫醇催化分解的活性中心。
Rare-earth elements (La and Ce) modified MCM-41 catalysts were synthesized by the conventional incipient wetness impregnation method.The effects of different rare earth elements on controlling the active sites for catalytic decomposition of methyl mercaptan were investigated.The physical and chemical properties were characterized by N2 adsorption-desorption,XRD,XPS,H2-TPR,NH3/CO2-TPD analysis,and the morphology and effect of rare-earth elements in the catalyst were determined.Result showed that two-step reaction was occurred in the catalytic decomposition of methyl mercaptan.At low temperature,methyl mercaptan was decomposed to intermediates DMS (CH3SCH3).At high temperature,DMS was further decomposed to small molecular products such as CH4 and H2S.For the 10%Ce/MCM-41 catalyst,surface active oxygen species are the active center at low temperature while the strong acid site is the active center at high temperature.For the 10%La/MCM-41 catalyst,strong acid site is the active center for the catalytic decomposition of methyl mercaptan.
挥发性有机硫化物(VOSCs)作为恶臭气体的特征污染物, 具有嗅觉阈值低、恶臭污染强烈和对人体健康损害大的特点。其中, 甲硫醇作为VOSCs的典型代表, 在常温下是一种无色、有烂洋葱味的气体, 嗅觉阈值体积分数0.4× 10-9[1], 具有易挥发、高毒和高腐蚀性等特点[2, 3]。对人体具有急性毒害作用, 影响人类的中枢神经系统, 吸入较低浓度时造成恶心和头疼, 而较高浓度时会出现麻醉状态, 高至一定含量时甚至可引起呼吸麻痹致死[4]。此外, 甲硫醇来源广泛, 主要来源于废水处置、卫生填埋、蛋氨酸合成以及石油加工过程等[5, 6, 7]。甲硫醇的存在对环境质量、人类身心健康和生产生活均会产生极大的危害, 因此对甲硫醇进行处理尤为重要。目前, 已报道的去除甲硫醇的方法主要有催化分解法[8, 9]、催化氧化法[10, 11]、碱液吸收法[12, 13]和生物处理法[14]等。其中, 催化分解法操作简单、不需要额外添加剂, 且产物多为小分子物质[15]。因此, 近年来对于甲硫醇催化分解的研究受到广泛关注[8, 9, 12]。目前, 催化分解处理甲硫醇的催化剂主要集中在CeO2基和HZSM-5分子筛催化剂, 前者催化分解甲硫醇温度较低, 约450 ℃就可以将甲硫醇完全转化, 但稳定性极差, 约10 h开始失活[16, 17]; 后者稳定性较好, 约(20~30) h开始失活, 但转化温度高达600 ℃[18, 19]。后期通过掺杂或负载稀土元素对这两类催化剂进行改性[8, 18, 20], 但效果不好, 主要原因是对活性中心认识不统一。部分学者认为对于甲硫醇催化分解反应主要是氧化还原性能起催化作用[9, 21], 如变价稀土元素Ce4+和Ce3+相互转化的过程中伴随大量活性氧物种和氧空位的产生, 进一步发生氧硫交换, 从而降解甲硫醇; 另外一部分学者认为, 主要是强酸性位点起催化作用[15, 19, 20], 强酸性位点以断裂C— S键的方式催化分解甲硫醇。通常情况下, 氧化还原性和强酸性位点是相互关联且伴生存在, 如具有氧化还原性的Ce4+和Ce3+通常充当路易斯酸酸性位点的作用, 因此很难独立描述氧化还原性和强酸性位点在催化分解甲硫醇反应中的作用。本文引入具有氧化还原性能的变价稀土金属元素Ce, 作为以氧化还原性为活性中心的代表, 引入没有氧化还原性能、没有变价, 但可提供酸碱性中心的La作为以强酸性位点为活性中心的代表, 排除HZSM-5自身强酸性的影响, 选择几乎没有酸性的MCM-41介孔分子筛为催化剂载体, 研究稀土引起的酸性作用对甲硫醇催化分解活性的影响, 进行不同稀土元素改性MCM-41对甲硫醇催化分解活性中心调控作用的研究。
六水合硝酸铈、六水合硝酸镧, 分析纯, 上海阿拉丁生化科技股份有限公司; 十六烷基三甲基溴化铵、正硅酸乙酯、氨水, 分析纯, 天津市光复精细化工研究所; 去离子水, 自制。
采用溶胶-凝胶法制备了有机-无机杂化介孔氧化硅材料MCM-41, 以十六烷基三甲基溴化铵(CTAB)和正硅酸乙酯(TEOS)分别作为模板剂和硅源。将14 g的CTAB和54 mL的NH3· H2O室温下溶解于635 mL去离子水中。连续搅拌, 将57.6 mL的TEOS逐滴加入上述溶液, 得到的凝胶用去离子水洗涤、过滤, 104 ℃干燥24 h, 马弗炉中1 ℃· min-1升温至300 ℃保持1 h, 再升温至500 ℃保持5 h, 即得到孔道呈六方有序排列、大小均匀、孔径可在(2~10) nm连续调节和比表面积大的MCM-41分子筛。
以MCM-41分子筛为载体, 以六水合硝酸镧和六水合硝酸铈为活性组分前驱体, 采用传统等体积浸渍法制备不同稀土元素La、Ce改性MCM-41的催化剂10%La/MCM-41和10%Ce/MCM-41。
采用德国布鲁克公司的D8 ADVANCE测定催化剂晶相结构, CuKα , λ =0.154 06 nm, 扫描范围 5° ~85° , 晶相结构采用Jade6.0软件分析计算。
N2吸附-脱附采用NOVA2000型分析仪测量催化剂表面孔结构和比表面积。测试前300 ℃真空下预处理1 h, -196 ℃下测定。
采用自行组装的H2-TPR测试设备测定氧化态样品的还原性能。选取0.1 g(40~60)目样品置于石英管中, 100 ℃通入10%H2/Ar以30 mL· min-1吹扫 1 h, 以10 ℃· min-1升温至800 ℃, 采用TCD在线检测氢气信号。
采用实验室自行组装的 NH3/CO2-TPD测量催化剂酸碱性。。
XPS采用赛默飞Escalab 250Xi进行分析样品的化学价态和表面元素相对含量。AlKα , 1 486.6 eV, X射线源。
Casa XPS软件用于样品的分峰和定量处理, 以 C1s的结合能 284.8 eV和Si2p的结合能103.3eV为标准校正荷电子效应。
甲硫醇催化降解活性评价装置为自制固定床反应器系统, 使用程序升温反应方式进行。将0.2 g(40~60)目样品置于ϕ 10 mm× 6 mm石英管中部。检查装置气密性良好后引入预混合总流量30 mL· min-1、体积分数0.5%和CH3SH(氮气做平衡气)为反应气。反应温度从300 ℃升温至650 ℃, 以25 ℃间隔进行催化活性评价, 并在600 ℃用0.2 g10%La/MCM-41和10%Ce/MCM-41催化剂分别进行稳定性测试。反应产物用装有一台火焰离子化检测器(FID)和一台火焰光度检测器(FPD)的气相色谱进行在线检测。其中, 装有PQ柱的FID检测器用来检测CH4、C2H4和CH3SH等碳氢化合物; 装有HP-Plot/Q毛细柱的FPD检测器用来检测CH3SH、H2S、COS和CS2等含硫分子。
10%La/MCM-41和10%Ce/MCM-4催化剂的XRD图如图1所示。
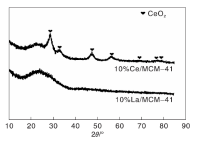 | 图1 10%La/MCM-41和10%Ce/MCM-41催化剂的XRD图Figure 1 XRD patterns of 10%La/MCM-41 and 10%Ce/MCM-41 catalysts |
由图1可以看出, 10%Ce/MCM-41催化剂具有(111)、(200)、(220)、(311)、(400)、(331) 和(420)等晶面特征峰(PDF 43-1002), 对应典型的氧化铈立方萤石结构(CaF2)[22]。而在10%La/MCM-41催化剂上没有检测到任何La物种的晶相, 表明La在MCM-41上分散均匀, 未达到最低检测限。
MCM-41和稀土元素La、Ce改性MCM-41催化剂的结构性能如表1所示。
| 表1 MCM-41和稀土元素La、Ce改性MCM-41催化剂的结构性能 Table 1 Textural properties of parent and rare earth (La, Ce) modified MCM-41 catalysts |
由表1可以看出, 改性后的催化剂比表面积均有所下降, 其下降趋势依次为MCM-41> 10%La/MCM-41> 10%Ce/MCM-41, 这可能是由于焙烧后金属氧化物进入MCM-41介孔孔道, 致使孔道堵塞, 引起比表面积、孔容及孔径下降。在10%Ce/MCM-41催化剂上下降程度相比更为突出, 表明其结构被破坏更为严重, 这也解释了其活性和稳定性差的原因。
10%La/MCM-41和10%Ce/MCM-41催化剂的XPS谱图如图2所示。由图2可以看出, 由于自旋轨道耦合的相互作用, La3d在(832~860) eV被分裂成5/2和3/2两个轨道。电子结合能835.5 eV和852.1 eV两个主峰归属为La3+或氧化镧物种和碳酸盐反应生成的碳酸氧镧物种[15][La2Ox(CO3)y], 峰位略高于文献[23]报道位置, 这是由于La物种在催化剂表面上以La2O3低配位团簇形式存在于表面La2Ox(CO3)y(0≤ x, y≥ 3)层中, 因此La物种结合能高于常规La2O3结合能[24]。10%La/MCM-41催化剂C1s进一步证明碳酸氧镧物种的存在, 在电子结合能289.5 eV处归属为碳酸盐物种[25], 与La3d结果一致; 10%Ce/MCM-41催化剂C1s没有扫描到任何碳酸盐物质, 表明很难形成碳酸铈物相。10%Ce/MCM-41催化剂的Ce3d谱图中, v'和u'归属为Ce3+物种, v、v''、v'''、u、u''和u'''归属为Ce4+物种[16, 26], 表明在10%Ce/MCM-4 催化剂上Ce以Ce3+和Ce4+形式存在。
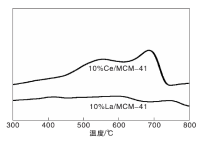
10%La/MCM-41和10%Ce/MCM-41催化剂的H2-TPR谱图如图3所示。Wei Y等[27]报道, 氧化铈在(400~800) ℃有2个明显的H2消耗峰, 分别对应表面晶格氧和体相晶格氧的还原。由图3可以看出, 10%La/MCM-41几乎可以认为没有任何还原峰出现, 即没有氧化还原性。原则上, La和Ce都属于稀土金属元素, 应该具有相似的氧化还原性能, 但由于其外层电子分布存在一定差异, 因此其氧化还原性能明显不同。
据文献报道, 催化分解甲硫醇的活性中心除了氧化还原性[17, 21], 还有催化剂表面的酸性中心[15, 28]。10%La/MCM-41和10%Ce/MCM-41催化剂的NH3-TPD和CO2-TPD谱图如图4所示。由图4可以看出, La和Ce改性后的MCM-41催化剂均具有弱酸性(150~300) ℃和强酸性(500~900) ℃。相比之下, 弱酸强度相差不大, 但10%La/MCM-41催化剂的强酸性较10%Ce/MCM-41偏向高温位置, 具有更强的强酸性。研究报道, 强酸性过强会导致催化剂积炭严重, 引起催化剂中毒而失活[15]。然而, 10%La/MCM-41比10%La/MCM-41的活性和稳定性更好, 这与XPS检测到的碳酸氧镧物种密切相关。众所周知, 碳酸氧镧物种同样可为催化剂提供额外的碱性中心(弱碱中心160 ℃和强碱中心730 ℃), 见CO2-TPD表征, 这种碱性中心有利于酸性甲硫醇分子的吸附活化。此外, 碳酸氧镧物种可以和积炭发生反应生成CO和CO2等物质, 起到消炭作用[29, 30], 具体见反应方程式:
La2O2CO3+C→ La2O3+2CO
La2O(CO3)2+C→ La2O3+2CO+CO2
因此, 结合活性测试、稳定性测试、NH3-TPD 及 CO2-TPD 等表征结果, 表明La3+比Ce4+具有更强的酸性, 从而导致10%La/MCM-41催化剂在高温段催化活性更高。同时, 理论上来讲更强的酸性也容易生成更多的积炭, 而稀土La引入生成的碳酸氧镧物种能够很好地抑制和消除催化剂积炭, 从而进一步提高催化剂催化分解甲硫醇的稳定性。
10%La/MCM-41和10%Ce/MCM-41催化剂催化分解甲硫醇的活性和稳定性如图5所示。由图5可以看出, 10%La/MCM-41和10%Ce/MCM-41分别在575 ℃和600 ℃实现CH3SH分子的完全降解, 二者在完全催化降解甲硫醇温度上差别不大。但是, 在低温段[(300~475)℃]如425 ℃、10%Ce/MCM-41催化分解甲硫醇转化率达60%, 而此时10%La/MCM-41催化剂转化率仅为20%; 在高温段[(475~650)℃]如550 ℃, 10%La/MCM-41催化分解甲硫醇转化率达98%, 而10%Ce/MCM-41催化剂转化率仅为50%。由此可见, 低温段10%Ce/MCM-41催化剂活性较好, 高温段10%La/MCM-41催化剂活性较好, 这与常规催化剂活性测试现象不同。对于催化分解恶臭气体甲硫醇, 催化剂稳定性是另外一个重要标准。10%La/MCM-41和10%Ce/MCM-41催化剂几乎都在120 h开始失活, 而10%La/MCM-41催化剂在失活过程中失活较慢, 136 h时二者转化率相差近40%, 稳定性提高可能是La物种的引入提供了部分活性中心所致。10%La/MCM-41和10%Ce/MCM-41催化分解甲硫醇活性中心存在明显不同。
 | 图5 10%La/MCM-41和10%Ce/MCM-41催化剂催化分解甲硫醇的活性和稳定性Figure 5 Activity and stability of 10%La/MCM-41 and 10%Ce/MCM-41 catalysts for catalytic decomposition of methyl mercaptan |
由图5还可以看出, 10%Ce/MCM-41催化剂活性测试中存在一个明显的“ 跳跃现象” , 原因可能是存在两步反应过程。
10%La/MCM-41和10%Ce/MCM-41催化剂催化分解甲硫醇产物分布如图6所示。甲硫醇首先催化分解生成中间体甲硫醚和硫化氢(2CH3SH→ CH3SCH3+H2S), 随着温度升高, 甲硫醚进一步分解生成甲烷和硫化氢等小分子产物(CH3SCH3→ H2S+CH4)。由图6可以看出, 在10%Ce/MCM-41催化剂上, 第一步反应的温度节点与催化剂相比向低温方向前移了50 ℃, 这是由于Ce的氧化还原性(见H2-TPR)会产生表面活性氧物种, 从而更容易活化C— S键和S— H键, 进而生成中间体甲硫醚; 第二步反应是甲硫醚进一步分解。从NH3-TPD可见, 10%Ce/MCM-41相比10%La/MCM-41催化剂的强酸性较弱, 导致其高温段活性较低, 最终呈现“ 跳跃现象” 。
 | 图6 10%La/MCM-41和10%Ce/MCM-41催化剂催化分解甲硫醇产物分布Figure 6 Products distribution of catalytic decomposition of methyl mercaptan over 10%La/ MCM-41 and 10%Ce/MCM-41 catalysts |
由图6还可以看出, 10%La/MCM-41催化剂高温段催化分解甲硫醇转化率明显高于10%Ce/MCM-41催化剂。从NH3-TPD可知, La3+产生比Ce4+更强的强酸性, 容易断裂C— S键来催化分解甲硫醇, 这解释了10%La/MCM-41在高温段催化分解甲硫醇活性好的现象。而更强的强酸性理论上会生成更多积炭, 但La物种引入生成的碳酸氧镧物种(见XPS)可消除生成的积炭, 从而使其稳定性得以改善。此外, 低温时含碳产物总量约3 000 mg· kg-1, 表明大部分甲硫醇分子被吸附在催化剂上; 高温完全转化时含硫产物总量几乎达到5 000 mg· kg-1, 但含碳产物仅约3 000 mg· kg-1, 表明积炭是两类催化剂中毒的主要原因。结合H2-TPR和NH3-TPD可知, 表面活性氧对第一步反应的促进作用更为明显, 而强酸性位点在第二步反应起催化活性作用。综上所述, 10%La/MCM-41催化剂催化分解甲硫醇的活性中心即为强酸性位点, 而10%Ce/MCM-41催化剂则为氧化还原性能和强酸性位点协同作用。
(1) 采用不同稀土元素La 和Ce对 MCM-41进行改性, 并用于甲硫醇催化分解实验, 结果表明, 稀土元素可以调控甲硫醇催化分解的活性中心。
(2) 对于具有变价的稀土金属元素如Ce, 氧化还原性能和强酸性位点起协同催化作用。对于没有变价的稀土元素如La, 强酸性位点是甲硫醇催化降解的活性中心。
(3) Ce4+和Ce3+的引入, 一方面会提供表面活性氧物种, 促进甲硫醚中间体的活化; 另一方面可作为强酸性位点, 断裂C— S键来提高甲硫醇催化分解活性。
(4) La3+的引入, 一方面可作为强酸性位点促进甲硫醇催化分解; 另一方面生成的碳酸氧镧物种可以有效抑制和消除积炭, 对稳定性的改善起积极作用。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|