作者简介:张郢峰,1978年生,女,硕士,副教授,主要从事多相催化研究。
采用浸渍法和共沉淀法制备了Ni质量分数10%的10%Ni/Ce0.9Gd0.1O1.95催化剂,通过X射线衍射、N2物理吸附与H2脉冲化学吸附、H2程序升温还原等技术表征了催化剂的结构和性质,并考察了其催化甘油水蒸汽重整制氢反应性能。结果表明,浸渍法制备的10%Ni/Ce0.9Gd0.1O1.95-S催化剂的活性最佳,该催化剂上Ni晶粒小、分散度高,形成氧空穴使得催化剂抗积炭能力大大提高,所以活性、氢气选择性较高,稳定性也较好。同时考察了水与甘油物质的量比和泵流速对甘油重整反应性能的影响,发现在水与甘油物质的量比为24:1,泵流速为0.06 mL·min-1的条件下,甘油几乎完全转化,氢气选择性也非常高,而且反应10 h没有失活。
10wt%Ni/Ce0.9Gd0.1O1.95 catalysts were prepared by dipping method and coprecipitation method.The structures and properties of these catalysts were characterized by X-ray diffraction,N2 physical adsorption and H2 pulsed chemical adsorption,and H2 temperature-programmed reduction.Catalysts performance in catalyzing the steam reforming of glycerol to hydrogen were investigated.It was found that the 10wt%Ni/Ce0.9Gd0.1O1.95-S catalyst prepared by the dipping method had the best activity.The catalyst had small Ni grains and high dispersion that form the oxygen vacancies which could greatly improve the resistance of the catalyst to carbon deposition.Therefore,its activity and hydrogen selectivity were high,and its stability was good.At the same time,the effects of the molar ratio of water glycerin and the pump flow rate on the performance of glycerol reforming were investigated.It was found that under the condition of a molar ratio of water glycerin of 24:1,and a pump flow rate of 0.06 mL·min-1,glycerin was almost completely converted,the hydrogen selectivity was very high,and there was no inactivation after 10 hours of reaction.
氢能源是种高效、清洁的二次能源, 且对环境零污染, 能有效解决目前能源短缺问题[1]。甘油是生物柴油的副产品, 随着生物柴油的研究深入, 副产大量甘油。甘油制氢符合能源的可再生要求, 是生物质制氢技术中最具发展前途的技术, 在相关领域引起了广泛关注。当前在甘油水蒸气重整制氢反应研究领域, 主要集中在催化剂活性载体、助剂选择及制备条件控制等方面。Ni 系催化剂具有活性高、成本低等优点, 在甘油水蒸汽重整制氢反应中得到了广泛应用, 但催化剂烧结和积炭问题有待解决。铈基氧化物能储-释氧, 且可与活性组分相互作用, 调节活性组分状态, 氧化消除积炭, 使催化剂稳定性提高。
本文采用浸渍法和共沉淀法制备Ni质量分数10%的10%Ni/Ce0.9Gd0.1O1.95催化剂, 研究在甘油水蒸汽重整制氢反应中催化剂的活性和稳定性。并采用 XRD、BET、TPR、H2脉冲化学吸附等方法表征催化剂的结构。
采用共沉淀法制备Ce0.9Gd0.1O1.95(1)复合氧化物载体。称取一定比例的Ce(NO3)3·6H2O和Gd(NO3)3·6H2O配制金属盐溶液, 沉淀剂为3 mol·L-1的NH3·H2O和3 mol·L-1的(NH4)2CO3等体积混合物。将金属盐溶液与沉淀剂用恒流泵并流滴定到备有50 mL二次蒸馏水的大烧杯中, 30 ℃磁力搅拌, 调节溶液pH值约为10。滴定结束, 继续搅拌30 min后老化1 h。过滤、用水洗涤至中性, 110 ℃恒温干燥过夜, 研细放入马弗炉中700 ℃焙烧4 h。
溶胶-凝胶法制备Ce0.9Gd0.1O1.95(2)复合氧化物载体。配制一定比例的Ce(NO3)3·6H2O和Gd(NO3)3·6H2O金属盐溶液, 按照n(Ce+Gd):n(柠檬酸)=1:1加入柠檬酸, 并用柠檬酸和乙二醇的混合溶液[m(柠檬酸): m(乙二醇)=3:2]将上述溶液饱和。水浴恒温80 ℃搅拌蒸发至溶液粘稠状, 110 ℃恒温干燥过夜, 马弗炉中 700 ℃焙烧4 h。
采用过量浸渍法制备催化剂, Ni浸渍质量分数为10%, 浸渍分两次进行。首先称取约0.495 4 g的Ni(NO3)2·6H2O放入50 mL烧瓶中, 加二次蒸馏水15 mL溶解, 油浴80 ℃磁力搅拌。载体Ce0.9Gd0.1O1.95(1)和Ce0.9Gd0.1O1.95(2)各取2 g, 分别加入烧瓶浸渍5 h。45 ℃下蒸干后移入培养皿中, 110 ℃干燥过夜, 研细放入马弗炉中550 ℃焙烧4 h。按照相同的方法进行二次浸渍, 所得催化剂压片(压力约15 MPa), 破碎, (20~40)目过筛, 得到10%Ni/Ce0.9Gd0.1O1.95-I和10%Ni/Ce0.9Gd0.1O1.95-S催化剂。
采用共沉淀法制备催化剂。一定量的二次蒸馏水中溶解物质的量比为9:1的Ce(NO3)3·6H2O和Gd(NO3)3·6H2O, 加入适量Ni(NO3)2·6H2O搅拌均匀。以Na2CO3为沉淀剂, 并流滴定两种混合溶液, 调节pH值约10, 不断搅拌。滴定结束, 继续搅拌30 min后老化1 h。过滤、用水洗涤至中性, 110 ℃恒温干燥过夜, 研细放入马弗炉中700 ℃焙烧4 h得到10%Ni/Ce0.9Gd0.1O1.95-C催化剂。
催化剂物相结构分析在DMAX-Ⅲ C型X射线衍射仪上测定, Cu靶, 工作电压40 kV, 工作电流40 mA, 扫描速率8o·min-1。
采用美国麦克公司ASAP2020M型全自动快速比表面积及孔隙度分析仪分析催化剂平均孔径和比表面积等。
H2-TPR在AutoChem 2920化学吸附-脱附仪上进行, 分析Ni基催化剂的分散度、表面积和平均粒径, 反应后催化剂积碳情况。
催化剂性能测试使用微型固定床反应器。甘油和水的混合溶液用微量泵输入, (20~40)目催化剂用量100 mg, 反应温度500 ℃, 氮气氛下进行反应。
采用Agilent 6820型气相色谱仪分析甘油转化率, HP-FFAP色谱柱(30 m× 0.25 mm, 250 ℃)毛细管分离柱, FID检测, 载气为高纯N2。气体产物通过Agilent 6820型气相色谱仪进行在线分析, 载气为高纯Ar, 色谱为双检测器, 气体组分分离采用两根Porapak Q(2 m× 2 mm, 230 ℃、250 ℃)填充柱和一根5A分子筛(2 m× 2 mm, 500 ℃)填充柱, TCD检测, 有机组分分离采用HP-FFAP(3 m× 2 mm, 200 ℃)填充柱, FID检测。
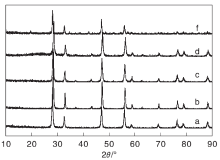
不同方法制备的催化剂XRD图如图1所示。
从图1可以看出, 虽然不同方法制得的催化剂XRD衍射峰相似, 都主要含有Ce0.9Gd0.1O1.95和NiO两种固溶体物相, 但制备方法对衍射峰的强度影响较大。其中, 共沉淀法制备的10%Ni/Ce0.9Gd0.1O1.95-C催化剂中Ce0.9Gd0.1O1.95和NiO固溶体衍射峰均较强, 说明Ce0.9Gd0.1O1.95固溶体晶体化程度较高, NiO晶粒聚集, 晶粒较大。催化剂活性组分和载体之间的相互作用、催化剂活性组分的性质与NiO和载体的晶粒大小密切相关, 进而在反应过程中催化剂的选择性也受到影响。
不同方法制得的催化剂N2物理吸附和H2脉冲测试结果见表1。从表1可以看出, 不同方法制备的催化剂BET比表面积差异较大, 说明催化剂BET比表面积大小受制备方法影响较大。其中共沉淀法制备的10%Ni/Ce0.9Gd0.1O1.95-C催化剂BET比表面积最小。由表1还可以看出, 不同方法制得的催化剂Ni分散度有较大差异。采用共沉淀法制备的10%Ni/Ce0.9Gd0.1O1.95-C催化剂, 由于活性金属Ni组分包覆于载体中, 所以分散度较小。
| 表1 不同催化剂的N2物理吸附和H2脉冲结果 Table 1 Physisorption and H2-pulse analysis of catalysts |
图2为不同方法制备的催化剂H2-TPR谱图。
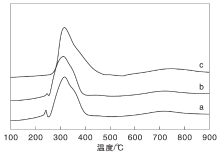 | 图2 不同方法制备的催化剂H2-TPR谱图 (a)Ni/Ce0.9Gd0.1O1.95-I; (b)Ni/Ce0.9Gd0.1O1.95-S; (c)Ni/Ce0.9Gd0.1O1.95-CFigure 2 H2-TPR spectra of catalysts prepared by different methods |
从图2可以看出, 浸渍法制备的两种催化剂分别有三个还原峰, 约出现在240 ℃、320 ℃和730 ℃。结合文献[2]报道, 第一个小的还原峰归属于吸附氧的还原峰, 载体晶格中进入镍后形成氧空穴, 氧空穴吸附氧; 第二个还原峰则是载体表面CeO2还原峰与载体上分散的小晶粒NiO还原峰的重叠峰, 结合文献[3]报道, 纯NiO还原温度约在360 ℃, 比催化剂中NiO还原温度高, 这是因为催化剂中NiO颗粒小于纯的NiO颗粒。已有文献[4, 5, 6, 7]报道, 在CeO2负载的金属催化剂上, 金属吸附氢会对载体产生溢流效应, 小晶粒NiO还原出的Ni0对载体有氢溢流作用, 使得载体表面的CeO2还原温度向低温方向移动。最后一个还原峰属于体相CeO2还原峰。共沉淀法制备的催化剂只有320 ℃和750 ℃左右的两个还原峰。第一个峰是载体表面CeO2还原峰与载体上分散的小晶粒NiO还原峰的重叠峰, 另一个还原峰是体相CeO2的还原峰。总体上, 浸渍法制备的两种催化剂上NiO与载体体表面CeO2的叠加还原峰向低温方向偏移, 表明共沉淀法制备的催化剂中NiO与分散在载体中的CeO2较难还原。
2.4.1 制备方法对催化性能的影响
在压力101.324 kPa, 温度500 ℃, 水与甘油物质的量比为24:1, 泵流速为0.06 mL·min-1, 载气N2流速为33 mL·min-1的条件下, 不同方法制得的10%Ni/Ce0.9Gd0.1O1.95催化剂催化甘油水蒸汽重整反应制氢性能见图3。
 | 图3 不同催化剂催化甘油水蒸汽重整反应制氢反应性能 (a)Ni/Ce0.9Gd0.1O1.95-I; (b)Ni/Ce0.9Gd0.1O1.95-S; (c)Ni/Ce0.9Gd0.1O1.95-CFigure 3 Catalytic performance for hydrogen production from glycerol steam reforming of catalysts |
由图3可以看出, 反应初始阶段, 三种催化剂上甘油转化率都较高, 其中浸渍法制得的10%Ni/Ce0.9Gd0.1O1.95-I催化剂上甘油转化率为96.5%, 10%Ni/Ce0.9Gd0.1O1.95-S催化剂上甘油转化率约为100%, 共沉淀法制得的10%Ni/Ce0.9Gd0.1O1.95-C催化剂上甘油转化率为81.9%。同时浸渍法制得的两种催化剂稳定性较好, 而在10 h的反应时间内, 共沉淀法制得的催化剂一直在失活。
由图3还可以看出, 浸渍法制得的两种催化剂对H2和CO2均有较高的选择性, 对H2的选择性分别是85.6%和81.6%, 而对CO和CH4选择性都较低, 对CO的选择性分别是9.6%和15.8%, 说明这两种
催化剂中的活性成分对甘油水蒸汽重整反应生成H2和CO2更有利, 同时也对水煤气变换反应有促进作用, 而且在10 h的反应时间内, 稳定性保持良好。共沉淀法制得的10%Ni/Ce0.9Gd0.1O1.95-C催化剂上CO选择性较高, 且逐渐增高, H2选择性较低, 且逐渐降低, 说明该催化剂上水煤气变换反应不容易进行。
2.4.2 水与甘油物质的量比对催化性能的影响
在压力101.324 kPa, 温度500 ℃, 载气N2流速为33 mL·min-1的条件下, 以Ni/Ce0.9Gd0.1O1.95-S为催化剂, 考察水分子对甘油水蒸汽重整制氢反应的影响, 结果见图4。
由图4可知, 当水与甘油的物质的量比由6:1提高到12:1时, 甘油初始转化率从97.3%增大到约100%, 当原料中水的比例继续增大时, 甘油初始转化率维持不变, 说明加入水有利于甘油转化, 这与文献报道的热力学结果一致。
水与甘油物质的量比为6:1时, 在反应前6 h内催化剂活性保持稳定, 之后逐渐失活, 当水与甘油物质的量比提高到12:1、18:1时, 也表现了相同的规律, 只是催化剂失活的速率有所不同。当水与甘油物质的量比提高到24:1时, 即使反应10 h后, 催化剂基本没有失活, 说明水与甘油物质的量比增大, 有利于催化剂的稳定性。
H2和CO2的选择性随着水与甘油物质的量比增大逐渐增加, 而CO和CH4的选择性随着水与甘油物质的量比增大逐渐降低, 这与热力学分析的结果[8]及文献[9, 10]报道相符, 这也说明了水煤气转
化反应和甲烷重整反应在较高的水与甘油物质的量条件下进行是比较有利的, 其实质是反应物浓度增大, 反应向正反应方向移动。这可能是因为提高水与甘油物质的量比活化了更多催化剂表面的水分子, 产生的OH基团就更多, 从而与反应物或中间体产生反应, 较多的水分子对载体表面、体相氧的补充和释放也有利。Aupretre A等[11, 12]曾提出亲水性能越好的催化剂载体, 越能高效地使水分子活化, 以便活泼OH基团的产生, 与吸附在活性金属上的碳氧基团反应, 使H2和CO2的选择性提高。
2.4.3 原料流速对催化性能的影响
在压力101.324 kPa, 温度500 ℃, 载气N2流速为33 mL·min-1, 水与甘油物质的量比24:1的条件下, Ni/Ce0.9Gd0.1O1.95-S催化剂上不同原料流速对甘油水蒸气重整反应性能的影响见图5。
 | 图5 Ni/Ce0.9Gd0.1O1.95-S催化剂上原料流速对甘油重整反应的影响 (a)流速0.06 mL·min-1; (b) 流速0.10 mL·min-1; (c) 流速0.14 mL·min-1Figure 5 Effect of feed velocity over Ni/Ce0.9Gd0.1O1.95-S catalyst on glycerol reforming reaction |
由图5可知, 甘油转化率受泵流速影响较大, 当泵流速从0.06 mL·min-1增加到0.10 mL·min-1, 再增加到0.14 mL·min-1时, 甘油起始转化率从99%降低到95.9%, 再降低到92.8%, 即泵流速逐渐增大, 甘油起始转化率逐渐减小。结合文献[9, 13]报道, 这是由于反应物接触催化剂的时间缩短造成的。因为泵流速增大时, 同一时间通过催化剂的反应物分子数增多, 反应物接触催化剂的时间就会缩短, 从而转化率降低。
在反应10 h内, 泵流速为0.10 mL·min-1和0.14 mL·min-1时, Ni/Ce0.9Gd0.1O1.95-S催化剂一直在失活, 相比之下泵流速为0.10 mL·min-1时失活速率较慢一些。虽然甘油转化率随泵流速增大而降低, 但甘油转化量增大了, 反应中催化剂表面积炭形成速率加大, 这就是催化剂失活速率随泵流速增加而增大的原因。
随着泵流速增大, H2选择性逐渐降低, 当泵流速从0.06 mL·min-1增加到0.10 mL·min-1, 再增加到0.14 mL·min-1时, H2选择性从85%降低到80%, 再降低到69%, 但10 h内H2选择性没有降低。
采用浸渍法和共沉淀法制备了Ni质量分数10%的10%Ni/Ce0.9Gd0.1O1.95催化剂, 发现浸渍法制备的10%Ni/Ce0.9Gd0.1O1.95-S催化剂在催化甘油水蒸气重整反应中的活性最佳, 分析TPR及H2脉冲化学吸附表征结果发现, 10%Ni/Ce0.9Gd0.1O1.95-S催化剂上Ni晶粒小、分散度高, 形成氧空穴使得催化剂抗积炭能力大大提高, 使催化剂在甘油水蒸汽重整反应中表现出活性、氢气选择性较高, 且稳定性也好。同时考察了水与甘油物质的量比和泵流速对甘油重整反应性能的影响, 结果发现在水与甘油物质的量比为24:1, 泵流速为0.06 mL·min-1的条件下, 甘油几乎完全转化, 氢气选择性也非常高, 而且反应10 h没有失活。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|