作者简介:施菁欣,1999年生,女,浙江杭州人。
采用水热法合成TiO2纳米管(TNTs),FeCl2·4H2O和稀氨水为原料原位合成磁性钛纳米管(TNTs/Fe3O4),通过氯磺酸对其表面进行改性制备了一类新型的磁性钛纳米管磺酸催化剂(TNTs-SO3H/Fe3O4)。采用FT-IR和TG等对催化剂表面官能团及热稳定性能进行表征。研究该催化剂在乙酰丙酸与正丁醇酯化反应中的催化性能。结果表明,在 n(乙酰丙酸)∶ n(正丁醇)=1∶4、反应温度118 ℃、反应时间6 h和催化剂用量为乙酰丙酸质量的8%时,乙酰丙酸正丁酯收率达95.8%。该催化剂即使在使用5次后仍具有强酸性位和高稳定性,因此具有工业应用潜力。催化剂可通过外加磁场实现回收再利用。
A sulfonated magnetic titania nanotubes (TNTs-SO3H/Fe3O4) was prepared by synthesis of titania nanotubes (TNTs) via hydrothermal method,followed by in-situ synthesis of magnetic titania nanotubes (TNTs/Fe3O4) using FeCl2·4H2O and diluted ammonia as the raw material,and finally modification by solfonation. Surface functional groups and thermal stability of the catalyst were characterized by FT-IR and TG. Catalytic behaviors of the TNTs-SO3H/Fe3O4) for esterification of levulinic acid with n-butanol were studied. n-Butyl levulinate yield of 94.6% was obtained under the following condition: n(levulinic acid)∶ n(n-butyl alcohol)=1∶4,dosage of catalyst=8%(based on mass of levulinic acid),118 ℃ for 6 h. TNTs-SO3H/Fe3O4 exhibited strong acid sites and high stability even after using for five times and is promising as a potential commercial catalyst. The catalyst can be recovered by external magnetic field.
近年来, 由于化石资源的短缺和环境污染的恶化, 可再生能源的开发和利用受到各国政府及科学家的高度重视[1]。生物质是自然界中来源广泛且储存丰富的一种可再生碳资源, 将其化学转化可以生产燃料和各种精细化学品, 被认为是化石资源的理想替代品[2, 3]。乙酰丙酸是生物质衍生出的一种新型生物质平台化合物, 可以与不同醇发生酯化反应来制备乙酰丙酸酯。乙酰丙酸酯是一类重要的有机化学品, 已广泛用作燃料添加剂、增塑剂、芳香剂和溶剂[4, 5]。根据反应所使用的原料不同, 从生物质资源出发转化合成乙酰丙酸酯主要可以通过4种途径来实现, 直接乙酰丙酸酯化法、生物质酸催化醇解法、糠醇和5-氯甲基糠醛醇解[6]。传统直接乙酰丙酸酯化法一般采用均相酸催化剂如硫酸等[7], 近年来, 新型固体酸如超强酸[8, 9, 10]、分子筛[11, 12]和杂多酸[13]等因环境友好及可重复利用等优点而备受关注。
以TiO2为载体键合磺酸基团的催化剂因其活性高受到越来越多的关注[14]。TiO2来源广泛, 化学性质稳定, 通过水热法[15]较易制备出具有更大比表面积和较规整孔道结构的TiO2纳米管(TNTs)。Chen A等[16]采用钛酸纳米管, 以四苯基溴化膦为辅助催化剂, 催化环氧丙烷环加成合成碳酸丙烯反应, 产物收率达99.9%, 活性远高于TiO2粒子和SO2-4/TiO2等催化剂[17, 18]。已有研究报道, 以TNTs为载体, 通过化学键合方法, 可有效构建较稳定的携有磺酸基的固体酸催化剂。周硕林等[19]利用(3-巯基丙基)-三甲氧基硅烷对TNTs进行修饰, 进而氧化合成了磺酸功能化的TNTs催化剂, 将其应用于乙酰丙酸酯的合成反应中, 取得较好效果。但TNTs作为粉末状固体, 比表面积较大, 机械性能不强, 不易与反应体系分离。本文对磁性二氧化钛的磺化改性及其催化合成乙酰丙酸酯的性能进行研究。
TiO2、乙酰丙酸、氯磺酸, 分析纯, 阿拉丁试剂有限公司; FeCl2· 4H2O、氨水〔w(NH3· H2O)=25%〕、丙酮、正丁醇、氢氧化钠、浓盐酸、二氯甲烷, 分析纯, 国药集团化学试剂有限公司。
DF-101B集热式恒温电磁搅拌器, 浙江省乐城电器厂; AVATAR 370红外光谱仪, 美国尼高力公司; STA409PC差热热重扫描量热仪, 德国耐驰公司; Agilent 6890N 型气相色谱仪, 美国安捷伦科技公司。
将0.665 g的FeCl2· 4H2O溶解于蒸馏水, 然后加入1.5 g水热法制备的TNTs, 不断搅拌并加入稀氨水10 mL, 85 ℃恒温加热0.5 h。过滤, 用蒸馏水洗涤, 100 ℃烘干, 得到TNTs/Fe3O4。
称取1.5 g的TNTs/Fe3O4于100 mL蒸馏烧瓶中, 加入50 mL二氯甲烷, 缓慢滴加0.9 mL氯磺酸, 反应回流24 h。过滤后用丙酮洗涤, 100 ℃烘干, 得到磁性钛纳米管磺酸催化剂, 记作TNTs-SO3H/Fe3O4。
在装有球形冷凝管和温度计的三口烧瓶中加入1.16 g(10 mmol)乙酰丙酸、2.97 g(40 mmol)正丁醇和0.1g的TNTs-SO3H/Fe3O4(占乙酰丙酸质量 8 %), 搅拌下加热回流, 反应一定时间。产物经离心分离后采用气相色谱仪进行分析。色谱条件:HP-5弹性石英毛细管柱, FID 检测器, 气化温度250 ℃, 进样温度250 ℃, 柱温180 ℃。
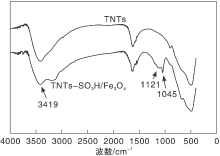
钛纳米管和磁性钛纳米管磺酸催化剂的FT-IR谱图见图1。由图1 可见, 钛纳米管在~3 400 cm-1处宽峰归属于钛纳米管表面吸附水分子或表面羟基O— H键的伸缩振动; 而磁性钛纳米管磺酸催化剂在3 419 cm-1处的特征峰变得较弱, 表明此时钛纳米管表面的大部分羟基与γ -巯丙基三甲氧基硅烷发生键和反应。1 045 cm-1与1 121 cm-1处的特征峰分别归属于— SO3H基团中O=S=O 键对称与反对称伸缩振动[20], 表明磺酸基团已成功键和到磁性钛纳米管上。
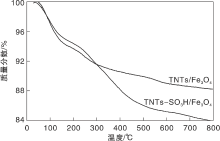
在高纯N2保护下, 升温速率20 ℃· min-1, TNTs/Fe3O4和TNTs-SO3H/Fe3O4的TG-DTG曲线如图2所示。
由图2可见, TNTs/Fe3O4和TNTs-SO3H/Fe3O4在100 ℃的失重为催化剂表面所吸附的水分子, (100~250) ℃的失重可能为TNTs表面的羟基脱离导致, 而TNTs-SO3H/Fe3O4在405 ℃时有比较大的失重, 此时为— SO3H基团的脱离失重。表明— SO3H基团已成功接枝到磁性钛纳米管上。
在n(乙酰丙酸)∶ n(正丁醇)=1∶ 4、催化剂用量为8%(以乙酰丙酸质量计, 下同)、反应时间6 h和反应温度118 ℃条件下, 考察不同催化剂对乙酰丙酸正丁酯收率的影响。
当催化剂为空白、Fe3O4、TNTs、TNTs/Fe3O4和TNTs-SO3H/Fe3O4时, 乙酰丙酸正丁酯收率分别为42.3%、47.1%、68.5%、64.2%和95.8%。结果表明, 空白和Fe3O4也有一定的乙酰丙酸正丁酯收率, 这是因为原料乙酰丙酸对反应的自催化作用。但使用TNTs和TNTs/Fe3O4作催化剂, 乙酰丙酸正丁酯收率提高约20%, 这是因为二氧化碳纳米管表面含有丰富的弱酸性含氧官能团。使用TNTs-SO3H/Fe3O4为催化剂时, 乙酰丙酸正丁酯收率有明显提高, 达95.8%, 表明该催化剂对乙酰丙酸与正丁醇的酯化反应具有良好的催化活性。
在n(乙酰丙酸)∶ n(正丁醇)=1∶ 4、催化剂用量8%和反应温度118 ℃条件下, 考察不同反应时间对乙酰丙酸正丁酯收率的影响。当反应时间为2 h、4 h、6 h、8 h和10 h时, 乙酰丙酸正丁酯收率分别为58.4%、76.8%、95.8%、95.9%和96.2%。酯化反应是一个可逆反应, 达到反应平衡需要一定的时间。随着反应时间增加, 乙酰丙酸正丁酯收率随之升高, 当反应时间为6 h 时, 反应趋于平衡, 再延长反应时间, 产品收率增加幅度减小。因此, 选择合适的反应时间为6 h。
在n(乙酰丙酸)∶ n(正丁醇)=1∶ 4、催化剂用量8%、反应时间6 h 条件下, 考察不同反应温度对乙酰丙酸正丁酯收率的影响。当反应温度为80 ℃、90 ℃、100 ℃、110 ℃和118 ℃时, 乙酰丙酸正丁酯收率分别为25.9%、38.7%、56.2%、83.7%和95.8%。结果表明, 产品收率首先随着酯化反应温度的升高而增加, 在118 ℃时接近最大值, 继续升温, 产品收率反而有所下降。这是因为反应温度过高, 促使副反应发生, 如醇脱水、酯水解等, 对反应不利。因此, 合适的反应温度为118 ℃。
在n(乙酰丙酸)∶ n(正丁醇)=1∶ 4、反应时间6 h和反应温度118 ℃条件下, 考察催化剂用量对乙酰丙酸正丁酯收率的影响。当催化剂用量(占乙酰丙酸的质量分数)为4%、8%、12%、16%和20%时, 乙酰丙酸正丁酯收率分别为60.5%、95.8%、92.6%、90.4%和88.9%。结果表明, 催化剂用量越大, 反应物分子与催化剂表面的活性位点接触越充分, 有利于催化反应的进行。随着催化剂用量的增加, 产品收率逐渐升高, 当催化剂用量为8%时, 产品收率达95.8%。当催化剂用量继续增加到20%时, 收率下降到了88.9%, 主要原因是反应体系中过量的催化剂导致副反应发生。
在催化剂用量8%、反应时间6 h、反应温度118 ℃条件下, 考察不同反应物物质的量比对乙酰丙酸正丁酯收率的影响。反应时原料正丁醇大大过量, 是因为正丁醇可以同时用作反应溶剂, 使反应物充分混合, 提高多相反应效率。当n(乙酰丙酸)∶ n(正丁醇)为1∶ 1、1∶ 2、1∶ 3、1∶ 4、1∶ 5和1∶ 6时, 乙酰丙酸正丁酯收率分别为58.1%、75.8%、88.6%、95.8%、96.1%和96.7%。结果表明, 随着原料物质的量比增加, 乙酰丙酸正丁酯收率随之增大。当n(乙酰丙酸)∶ n(正丁醇)=1∶ 4 时, 乙酰丙酸正丁酯收率达到95.8%, 再增加物质的量比, 产品收率增加不大。因此, 选择n(乙酰丙酸)∶ n (正丁醇)为1∶ 4 适宜。
在n(乙酰丙酸)∶ n(正丁醇)=1∶ 5、催化剂用量12%、反应时间4 h和反应温度120 ℃条件下, 考察催化剂重复使用次数对乙酰丙酸正丁酯收率的影响。当催化剂使用1、2、3、4、5和6次时, 乙酰丙酸正丁酯收率分别为95.8%、93.2%、89.5%、88.7%、86.4%和86.2%。TNTs-SO3H/Fe3O4在磁场下易于分离, 可很好地实现催化剂回收, TNTs-SO3H/Fe3O4重复使用6次后, 乙酰丙酸正丁酯收率从95.8%下降到了86.2%, 下降趋势为先快后慢, 最后保持稳定。此时催化剂仍有较高的催化活性, 表明催化剂活性比较稳定, 催化剂活性降低的原因主要是回收过程中难以避免的质量损失。
(1) 以TiO2纳米管为原料, 与氯化亚铁和氨水通过共沉淀法原位制备了磁性钛纳米管, 通过使用氯磺酸对其表面改性, 制备了一种新型的磁性钛纳米管磺酸催化剂。将其应用于催化乙酰丙酸与醇的酯化反应合成乙酰丙酸酯类化合物, 展示出较高的催化活性。催化剂在反应完成后, 可以在外加磁场的作用下实现快速分离, 从而简化反应操作。
(2) 该催化剂合成乙酰丙酸丁酯的适宜条件为:n(乙酰丙酸)∶ n(正丁醇)=1∶ 4、反应时间6 h、反应温度118℃、催化剂用量8 %条件下, 产物收率可达95.8%。该催化剂具有较好的重复使用性能, 为生物质平台化合物的高效转化提供了新途径。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|