作者简介:吕祎壮,1996年生,男,湖北省襄阳市人,在读硕士研究生,研究方向为甲醇水蒸气制氢催化剂及反应器设计。
采用共沉淀法制备一系列不同质量比的CuO-ZnO-Al2O3催化剂,用泡沫镍作为载体,研究其对甲醇重整制氢性能的影响。采用SEM和XRD等对催化剂进行检测表征,利用自制的平板式制氢反应器对催化剂性能进行检测。结果表明,催化剂在(230~270) ℃表现出良好的催化性能。在一定的质量比范围内,随着CuO含量的增高,甲醇重整制氢性能得到改善。在水醇物质的量比1.5∶1、反应温度250 ℃、反应物流量3 mL·min-1和 m(CuO)∶ m(ZnO)∶ m(Al2O3)=9∶9∶2条件下,CuO-ZnO-Al2O3催化剂性能最好,甲醇转化率为82.4%。
CuO-ZnO-Al2O3 catalysts with different mass ratio were prepared by co-precipitation.These catalysts were carried on foamed nickel to study its effect on hydrogen production by methanol steam reforming.These catalyst were characterized by scanning electron microscopy (SEM),X-ray diffraction (XRD) and their performance was tested on a self-fabricated plate-type hydrogen preparation reactor.The results indicated that the catalysts exhibited good catalytic performance at 230-270 ℃.The methanol reforming performance increased with CuO content in a certain scope of mass proportion.Optimum result,i.e., methanol conversion of 82.4,was obtained under condition as follows:H2O/CH3OH molar ratio of 1.5∶1,reaction temperature 250 ℃,feed flow rate 3 mL/min, m(CuO)∶ m(ZnO)∶ m(Al2O3) molar ratio of 9∶9∶2.
化石能源的使用加速了工业化进程, 但过度的使用会引起环境污染以及能源枯竭, 寻找和开发新的清洁能源势在必行。随着对清洁能源的探索, 氢能源逐渐进入研究者视野。氢气的燃烧产物无污染, 有望代替化石能源成为新的能源载体, 同时, 氢气燃烧热值高, 储量丰富, 使其在众多可再生能源中更具吸引力[1]。但是氢气在运输和储存等方面仍有许多问题[2]。为了解决这些难题, 有学者提出将氢以液态有机化合物形式储存起来, 需要时在低温下就地释放, 从而不产生CO等污染[3]。因此, 甲醇受到科学家广泛关注。甲醇作为制氢原料具有以下优点[4, 5, 6, 7]:(1) 来源广泛且价格低廉; (2) 氢碳比高, 单位质量制得的氢气多; (3) 储运方便; (4) 甲醇水蒸气重整制氢的反应条件温和。此外, 关于甲醇水蒸气重整制氢催化剂的研究也相对成熟, 其体系主要分为:贵金属催化剂[8, 9]、铜基催化剂[10, 11]以及镍基催化剂[12, 13]。在众多催化剂中, 铜基催化剂成本较低, 具有良好的低温催化活性(一般不超过300 ℃), 被广泛应用于甲醇水蒸气重整制氢[7, 14]。
目前国内对以甲醇为原料进行原位制氢给新能源汽车提供能源的报道较少, 因此开展甲醇制氢的催化研究, 开发高性能、低成本和稳定性好的甲醇水蒸气制氢催化剂具有重要的理论及现实意义。由于CuO-ZnO-Al2O3催化剂对于甲醇制氢有低温活性高和产物选择性好等优点成为国内外的研究热点。本文为了确保催化剂活性并解决催化剂高温烧结以及CO中毒, 采用多孔泡沫镍作为载体, 利用发泡金属具有三维网状多孔结构、骨架结构稳定、一定的机械强度和可塑性高等优点, 制备的催化剂具有比表面积大, 通透性好, 催化剂床层传质阻力小, 可避免积炭烧结且可增大原料处理量, 有利于节能降耗。研究不同质量比的CuO-ZnO-Al2O3催化剂对甲醇水蒸气重整制氢的影响, 主要从甲醇转化率和产物选择性来评价各组催化剂性能的优劣。
无水碳酸钠(Na2CO3)、硝酸铜[Cu(NO3)2· 3H2O]、硝酸锌(ZnNO3· 6H2O)、硝酸铝[Al(NO3)3· 9H2O]、甲醇(CH3OH)、无水乙醇(C2H5OH), 分析纯, 国药集团化学试剂有限公司; 泡沫镍, 纯度99.99%, 硕尔科研金属材料有限公司; 皂土, 麦克林化学试剂有限公司; 铝溶胶、去离子水, 自制。
84-1A型磁力搅拌器, 上海司乐仪器有限公司; TDL-60B低速台式离心机, 上海安亭科学仪器厂; DHG-9240A型电热鼓风干燥箱, 上海一恒科学仪器有限公司; GSL 1500X型管式炉, 合肥科晶有限公司; FESEM SU8020型场发射扫描电子显微镜, 日本日立公司; Smart Lab型X射线衍射仪, 日本Rigaku公司; 不锈钢平板式甲醇制氢反应器, 自制。
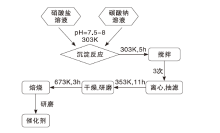
采用共沉淀法制备一系列质量2 g的CuO-ZnO-Al2O3催化剂。催化剂制备流程如图1所示。
按催化剂中3种氧化物的质量比计算并称取Cu(NO3)2· 3H2O、ZnNO3· 6H2O和Al(NO3)3· 9H2O置于同一烧杯中, 加入100 mL去离子水配置成混合溶液。然后按质量计算值1.2倍的量称取Na2CO3置于另一烧杯中, 加入100 mL去离子水配置成碳酸钠溶液。将硝酸盐混合溶液缓慢加入装有碳酸钠溶液的烧杯中进行沉淀反应, pH保持7.5~8。用磁力搅拌器搅拌5 h, 室温条件下完全沉淀, 静置2 h使其陈化, 然后离心、洗涤去除Na+, 最后进行抽滤。滤饼在80 ℃下烘干, 将得到的前驱体研磨均匀后置于管式炉中400 ℃焙烧3 h得到催化剂, 焙烧气氛为空气, 升温速率3 ℃· min-1。焙烧结束后催化剂需研磨均匀才能用于表征和测试。
将焙烧完成的催化剂再次研磨均匀, 称取黏结剂和催化剂置于烧杯中并加入去离子水搅拌均匀配置催化剂浆料。按照反应流道的大小裁剪出合适尺寸的泡沫镍载体, 置于无水乙醇中超声20 min, 去除载体表面的杂质。载体烘干后放入催化剂浆料中, 用浸渍法进行多次负载。最终经过烘干称量算得载体增重约0.3 g。
采用日本日立公司的FESEM SU8020型场发射扫描电子显微镜分析样品微观形貌和化学组分。
采用日本Rigaku公司Smart Lab型X射线衍射仪确定物质的相和晶体结构, CuKα , 工作电压45 kV, 工作电流200 mA, 扫描范围10° ~100° , 扫描速率10° · min-1。
实验在自制的反应器中进行催化剂活性评价, 反应器设计参考文献[15]。反应温度(210~270) ℃, 待反应稳定后, 检测10 min内产物成分及含量。催化剂活性评价装置如图2所示。
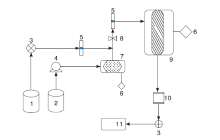 | 图2 催化剂活性评价装置 1.N2; 2.甲醇水溶液; 3.单向阀; 4.微型蠕动泵; 5.流量计; 6.温控仪; 7.蒸发腔; 8.不锈钢接头; 9.反应室; 10.冷凝净化器; 11.色谱仪Figure 2 Experimental apparatus |
反应室的进料是甲醇、水和氮气的气体混合物。甲醇水溶液在混合前通过独立的蒸发腔进料。氮气和混合气的流速由流量计控制。反应室内有均匀排列的反应槽且出口处连接冷凝装置, 使气体进入分别装有氢氧化钠溶液和盐酸溶液的冷凝过滤瓶中, 除掉杂质, 再观察瓶内是否有气泡来判断是否产生氢气和一氧化碳等不溶性气体, 最终在色谱仪上进行气体成分分析和催化剂性能分析。
甲醇转化率及产物选择性计算公式为:
SI=
式中, FI是气态产物中组分I(包括二氧化碳、一氧化碳等)的流量。
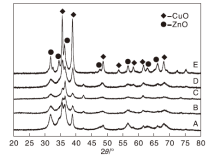
首先将样品磨细磨匀, 然后取适量样品于载玻片凹槽内压平压实, 再置于仪器内测试。CuO-ZnO-Al2O3催化剂的XRD图如图3所示。
由图3可知, 大多数衍射峰出现在2θ =30° ~40° , CuO和ZnO的强峰分别在2θ =35.5° 、38.7° 和48.7° 以及2θ =31.7° 、34.4° 、36.2° 、56.5° 和62.8° , 且CuO和ZnO的衍射峰有一部分重叠。图中未观察到明显的Al2O3衍射峰, 可能是因为Al2O3含量不高, 且Al2O3分散性较好。催化剂中没有加入大量的Al2O3是考虑到其虽然可以促进ZnO和 CuO分散, 但会降低催化剂性能, 然而少量的Al2O3有利于提高催化剂稳定性和机械强度[6, 16]。另外, XRD图还表明, 在Al2O3的低负载情况下没有发现ZnAl2O4和CuAl2O4特征峰, 原因可能是在焙烧温度高于500 ℃条件下才能形成[17]。
由图3还可以看出, 5组催化剂中CuO衍射峰逐渐尖锐, 尤其是催化剂E的变化最为明显, 表明CuO晶粒变大, 原因可能是Cu/Zn质量比增大使CuO分散性变差, 发生团聚现象导致晶粒粗大[16, 18]。而ZnO和 CuO的衍射峰并没有完全分离, 可能是因为ZnO和 CuO之间仍存在一定的相互作用, 有研究表明ZnO和 CuO之间的相互作用可以促进CuO分散, 对催化剂性能有着至关重要的作用[6, 14, 19]。
测试加速电压 5 kV, CuO-ZnO-Al2O3催化剂的SEM照片如图4所示。
由图4可知, 催化剂A出现了晶粒团聚及少量孔洞, 催化剂以颗粒状和团状形式存在, 随着催化剂成分的调整, 晶粒逐渐细化, 催化剂B、C和D的形貌基本一致, 孔洞减少, 催化剂呈类似圆形小颗粒状及少量薄片状。在催化剂B和催化剂D中依然存在颗粒团聚现象, 而催化剂C颗粒分布相对均匀。催化剂E晶粒团聚现象最为明显并伴随产生大量孔洞, 此时催化剂显示为长条状或块状。众所周知, 甲醇水蒸气重整反应发生在催化剂表面, 而团聚现象会减少催化剂比表面积, 进而减少原料气流与催化剂表面接触的机会, 使得催化剂性能下降。结合图3可知, 铜基催化剂中仍需添加其他组分来提高催化剂活性、稳定性及分散性等[19, 20], 表明铜基催化剂中CuO含量并不是越高越好, 当CuO含量过高时, 其他组分无法起到很好的分散作用, CuO会发生晶粒增大和团聚, 最终导致催化剂性能下降[11, 19]。
CuO-ZnO-Al2O3催化剂的成分如表1所示。由表1可知, 实验过程中使用的所有元素均出现在催化剂中。虽然XRD无法证明, 但可以看出氧化铝存在于催化剂中, 并且EDS分析证实不同样品的铜含量逐渐增加。样品中检测出少量的碳元素和氟元素, 可能是在搅拌时采用的聚四氟乙烯搅拌子在持续高速长时间搅拌过程中表面发生磨损所致。
| 表1 CuO-ZnO-Al2O3催化剂的成分 Table 1 Composition ofthe CuO-ZnO-Al2O3 catalysts |
实验设置了水醇物质的量比、催化剂成分配比和反应温度3个变量。各样品在性能测试前需在管式炉中用10%的H2/N2气体于300 ℃条件下活化还原2 h。且测试催化剂性能前, 需对载体进行空白对照实验。反应条件:反应温度250 ℃, 压强0.1 MPa, 水醇物质的量比1.5∶ 1, 反应物流速3 mL· min-1, 装填未负载催化剂的泡沫镍载体。色谱仪未检测到H2和CO2等产物, 且冷凝器收集的液体与甲醇水溶液的进样量相同, 证明实验所选载体对催化反应无影响。催化剂性能通过甲醇转化率和产物选择性来进行评价。
2.4.1 水醇物质的量比
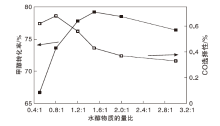
在催化剂用量0.3 g、反应压力0.1 MPa、反应温度230 ℃和进料流量3 mL· min-1条件下, 考察水醇物质的量比对催化剂B[m(CuO)∶ m(ZnO)∶ m(Al2O3)=8∶ 10∶ 2] 的性能影响。
由图5可知, 甲醇转化率及CO选择性均与水醇物质的量比有关。在其他条件相同情况下, 增加水醇物质的量比能促进甲醇转化, 同时抑制副产物CO产生。当水醇物质的量比为0.8∶ 1时, 甲醇转化率仅为73.6%, 当水醇物质的量比为1.5∶ 1时, 甲醇转化率最高为79.2%, 此时CO选择性为0.43%。继续增加水醇物质的量比, 则导致甲醇转化率降低。根据甲醇重整制氢的反应方程及原理分析, 水量的增加有利于甲醇重整反应充分进行, 促进CH3OH转化[20, 21]。此外, 在水醇物质的量比不断增加, 其他条件保持不变情况下, 单位时间内经过反应器的甲醇量减少, 甲醇转化率逐渐降低[21]。且过高的水醇物质的量比也会增加汽化能耗。由于水气变化反应增强, 有更多CO向CO2转化, 导致其选择性下降[23]。因此, 选择水醇物质的量比为1.5∶ 1为宜。
2.4.2 反应温度
在催化剂用量0.3 g、反应压力0.1 MPa、水醇物质的量比1.5和进料流量3 mL· min-1条件下, 考察反应温度对甲醇转化率的影响, 结果如图6所示。由图6可知, 反应温度210 ℃时, 甲醇转化率整体处于一个较低水平, 其中催化剂E的转化率最低, 不足60%。原因可能是因为甲醇重整制氢为吸热反应, 较低的温度不利于制氢反应充分进行[5, 12]。而随着反应温度升高, 甲醇转化率得到显著提高, 反应温度250 ℃时, 催化剂A、B、C和D的转化率分别为78.6%、81.7%、82.4%和79.7%, 其中催化剂B和催化剂C的催化性能相差不大, 但均强于其他催化剂, 再次证明铜基催化剂CuO含量并不是越高越好。5种催化剂性能在250 ℃升高到270 ℃过程中的提高没有之前明显, 此时催化剂C转化率最高为83.6%。原因可能是随着温度升高, 重整反应已经充分进行, 且体系中发生了副反应, 在一定程度上抑制了甲醇重整反应[3, 22]。在不考虑低温反应的情况下认为催化剂C性能较好, 因为催化剂成分配比合适, 在多孔泡沫镍的作用下催化剂分散较均匀, 活性位点较多且未发生明显的高温烧结。
表2为反应温度对催化剂性能的影响。由表2可以看出, 催化剂C的性能相对较优, 表明铜基催化剂CuO含量不是越高越好。随着反应温度升高, 270 ℃时催化剂C的H2转化率最高, 为97.1%。这是由于SRM是一个吸热反应, 升高温度对重整反应有利[7, 22]。由表2还可以看出, CO选择性随着反应温度的升高而升高, 相反CO2选择性随着反应温度的升高而降低。如催化剂C, 270 ℃时, CO2和CO选择性分别为95.8%、0.56%。结合甲醇重整制氢反应方程[22, 23]可以看出, 整个反应体系存在副反应, 且副反应属于吸热反应。所以, 随着反应温度逐渐升高, 副反应也被激活并逐渐稳定, 其会产生微量的CO和CH4等副产物, 导致CO2选择性降低。研究表明, 副产物中的CO即使含量很少(约10× 10-6), 也会使燃料电池发生中毒[14, 22]。因此, 理想的甲醇水蒸气重整催化剂不仅应具有优异的催化性能, 还需一定的抗毒和抗烧结性能, 这不仅可以降低能耗, 还能抑制CO等副产物的生成, 降低产物的后续处理难度。结合图6, 选择催化剂C进行催化剂稳定性分析。
| 表2 反应温度对催化剂性能的影响 Table 2 Effect of reaction temperature on the catalytic performance |
2.4.3 催化剂稳定性
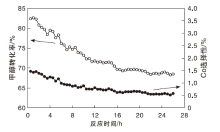
在250 ℃和水醇物质的量比1.5∶ 1条件下, 反应时间对催化剂稳定性的影响如图7所示。
由图7可以看出, 在反应最初12 h, 催化剂活性迅速下降, 甲醇转化率由82.4%降至71.8%, 这主要是由于热烧结[6]。约16 h后, 催化剂C表现出稳定的活性, 此时甲醇转化率和CO选择性各自稳定在68.5%和0.56%。经过26 h持续反应, 甲醇转化率接近70%, 产物中CO选择性不高于0.6%, 催化剂C拥有较好的稳定性。从而证明泡沫镍作为载体使催化剂比表面积增加, 通透性变好, 可避免积炭烧结。
采用共沉淀法制备一系列用于甲醇重整制氢的铜基催化剂, 通过调整催化剂中各组分的配比, 可使晶粒细化, 得到较好的催化效果。结果表明, 用三维网状多孔结构的泡沫镍作为载体制备的催化剂随着铜锌比例的增加, 催化剂性能得到提高, m(CuO)∶ m(ZnO)∶ m(Al2O3)=9∶ 9∶ 2时, 获得性能较好的一组催化剂, 催化剂表面粒子较规则, 分布较均匀, 当比例继续增加, 催化剂性能提高不甚明显。在水醇物质的量比1.5∶ 1、反应温度250 ℃和反应物流量3 mL· min-1条件下, 甲醇转化率较高, 为82.4%, H2转化率为93.4%, 副反应进行程度较低, 原因可能是使用泡沫镍作为载体增加了催化剂比表面积, 使通透性变好, 可避免积炭烧结, 且可增大原料处理量。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|