作者简介:周彦斌,男,在读硕士研究生,研究方向为生物质催化转化。
作为同分异构体的葡萄糖和果糖均可转化生成5-羟甲基糠醛和乙酰丙酸等重要平台化合物。与葡萄糖相比,果糖即使在无催化剂作用下也可进行反应,故葡萄糖异构为果糖的研究具有重要意义。葡萄糖异构方法主要有生物酶法、化学异构法和其他新技术。现阶段国内外研究热点主要集中于高效酶、催化剂的合成和催化体系的优化,建议加强酶结构变化和酶学性质变化及葡萄糖异构的反应机理和动力学模型的研究,从而有效指导合成高效的葡萄糖异构化酶和催化剂,并对反应体系进行优化。
Glucose and fructose as the isomers can be converted into important platform compounds such as hydroxymethyl furfural(HMF) and levulinic acid.The research found that fructose was a more desirable feedstock since it could be dehydrated into HMF easily in varieties of media,even in the absence of catalysts.Thus,fructose should be a better choice as a desirable feedstock for platform chemicals.At present the isomerization methods mainly include enzymatic,chemical and other new techniques.The research on isomerization of glucose was focused on the synthesis of high efficiency enzyme,catalyst preparation and the optimization of catalytic system.It was suggested that the changes of enzyme structure and enzymatic properties and the reaction mechanism and kinetic model of glucose isomerization should be investigated,so as to effectively enhance the development of high efficiency enzyme and catalyst for glucose isomerization,and the catalytic system should be optimized.
生物质是可替代传统化石资源同时生产燃料和化学品的可再生资源。纤维素是自然界中丰富的可再生植物生物质资源, 其结构单元为葡萄糖。葡萄糖和果糖作为同分异构体均可以转化生成5-羟甲基糠醛, 进一步脱水生成乙酰丙酸。因此, 葡萄糖和果糖可作为生产平台化合物5-羟甲基糠醛和乙酰丙酸的重要原料。与葡萄糖相比, 果糖转化合成5-羟甲基糠醛不但转化效率高, 甚至在无催化剂条件下也可合成5-羟甲基糠醛, 果糖比葡萄糖更适合转化合成平台化合物, 葡萄糖异构化成果糖被认为是转化生物质为燃料和化学品的关键化学步骤[1, 2, 3]。
本文主要概述国内外葡萄糖异构化的研究进展, 重点讨论葡萄糖异构化使用的催化剂, 分析仍存在的问题和可能的解决措施, 同时对今后该领域的研究前景进行展望。
葡萄糖异构酶一般称作D-木糖异构酶, 能将D-葡萄糖、D-木糖和D-核糖等醛糖转化为相对应的酮糖, 是应用广泛的酶之一[4, 5]。葡萄糖异构酶在自然界分布较多, 包括细菌、放线菌和真菌均发现存在, 其中以放线菌和细菌中发现的最多[6], 其催化葡萄糖生成果糖反应的转化率为26%~59%。根据葡萄糖异构酶一级结构中N末端一般将其可分为Ⅰ 型和Ⅱ 型[7], Ⅰ 型由于催化温度适中, 对葡萄糖的亲和力和催化效率高, 在生产实践中应用广泛[7, 8]。葡萄糖异构酶是一种胞内酶, 最早研究发现其进入体内后的最适底物为D-木糖[5]。后来研究发现, 在体外也可以将D-葡萄糖转化为D-果糖, 也可将D-木糖和D-核糖等醛糖转化为相对应的酮糖[6]。
酶作为天然生物催化剂, 大多数酶很不稳定, 在工业应用中往往受到缺乏长期运营稳定性和酶无法重复使用等技术障碍。固定化酶增强了酶在储存和使用条件方面的稳定性, 同时方便酶的处理, 简化生物催化的操作过程, 有利于控制反应的进程。同时, 因为酶可以分离再使用, 大幅度降低了酶与酶制剂的成本。固定化酶已成为工业酶制剂应用的重要技术之一[9]。
固定化酶包括物理方法和化学方法。物理方法是指用物理吸附法将酶固定, 由于未改变酶的结构, 可以很好保留酶的活性。包埋法是一种常用的物理固定酶法, 是将酶包埋在凝胶格子或者制成微型胶囊, 然后用于催化反应。刘芳[10]研究了明胶-戊二醛法在共固定化乳糖酶和葡萄糖异构酶中的应用, 并与开孔明胶法和卡拉胶包埋法进行比较, 选择明胶为固定化载体, 通过先包埋再交联的方法共固定乳糖酶和葡萄糖异构酶。以固定化酶的活力回收率为指标, 确定最佳的固定化条件为:pH=8.6, 明胶质量分数为23%, 前交联戊二醛体积分数0.15%, 后交联戊二醛体积分数0.15%, 后交联温度4 ℃, 后交联时间10 min。此时乳糖酶和葡萄糖异构酶的活力回收率分别为32.05%和82.52%。
化学法包括结合法和交联法, 结合法又分为离子结合法和共价结合法, 是将酶通过化学键连接到天然的或合成的高分子载体上, 使用偶联剂通过酶表面的基团将酶交联起来, 形成相对分子量更大、不溶性的固定化酶。其中, 吸附法和共价键法又可统称为载体结合法[11, 12]。
交联法是利用戊二醛、乙二胺和双偶氮苯这类双功能试剂, 能够通过共价键和酶分子形成具有三维结构的网状结构, 但不改变酶的结构和活性。戊二醛是交联法中应用广泛的一种试剂。于海涛[13]以Tween-20和Span-60为复合分散剂, 以烯丙基缩水甘油醚和甲基丙烯酸缩水甘油酯为功能性单体, N, N-亚甲基双丙烯酰胺为交联剂, 制备得到聚合物载体GAMM, 并将其作为葡萄糖异构酶的交联载体应用于葡萄糖异构化反应, 研究发现, 该固定酶不但反应条件温和(65 ℃), 而且催化效率高, 经过18次重复使用后仍保持90%以上的初始活性, 80 ℃固定化酶比游离酶具有更好的热稳定性。
结合法主要是利用载体中共价键或离子键与酶的物理或化学特性将其结合起来, 从而达到酶与载体的结合。载体亲水性基团和比表面积均可影响与其结合的固定化酶活性。由于酶本质是蛋白质, 所以酶分子上活性功能团可以通过化学共价键与载体表面的相关反应集团形成共价结合, 从而将酶分子结合到载体上, 形成固定化酶。Seyhan Tü kel S等[14]利用N, N-亚甲基双丙烯酰胺、甲基丙烯酸缩水甘油脂、烯丙基缩水甘油醚和甲基丙烯酰胺共聚合制得载体, 利用共价结合法固定化葡萄糖异构酶, 结果表明, 在葡萄糖异构果糖的反应过程中, 固定化酶的催化效率是游离酶的3倍以上。
离子结合法是通过离子效应将酶固定在具有离子交换基团的非水溶性载体上的固定化方法。一般认为粒子结合法固定化酶的载体必须具有离子交换基团(如DEA-TEAE-DEAE)、离子交换树脂必须具有聚电解质[12, 13, 14, 15]。袁建国等[16]采用苯乙烯和二乙烯苯聚合再经氯甲基胺化合成了一种强碱性苯乙烯系, 该聚合物具有季胺基团的大孔阴离子树脂结构, 在对嗜热放线菌葡萄糖异构酶固定化的研究中发现, 利用该载体制得的固定化酶具有制作简单、机械强度高、保存期长和重复利用性高等优点。葛玉斌等[17]采用分子沉积法, 在多孔三甲胺基聚苯乙烯载体上成功固定化了双层葡萄糖异构酶, 研究发现, 该双层葡萄糖异构酶固定酶的活性比游离态酶的活性高一倍以上, 而且单位载体负载量大。佟毅等[18]利用分子沉积技术将多孔三甲铵甲基聚苯乙烯作为载体合成葡萄糖异构酶双层固定化酶, 并进行生产, 取得了良好的效果。
化学法异构葡萄糖主要指利用酸或碱催化进行异构化。葡萄糖ɑ -羰基在碱性条件下可通过去质子化形成1, 2-烯醇式中间体, C1原子可继续通过质子化进一步生成果糖, 同时还会生成其差向异构体D-甘露糖[1]。根据反应类型可分为均相催化和非均相催化, 均相催化选用的催化剂主要有无机碱、无机酸和金属盐, 非均相催化选用的催化剂主要有离子交换树脂、金属氧化物和分子筛等[19]。
贾松岩等[20]以无机碱氢氧化钠和有机碱四甲基胍为催化剂, 研究了葡萄糖异构化制果糖的反应, 果糖收率为33%~37%。
Harris D W等[21]以酸为催化剂进行了葡萄糖异构化果糖的研究, 果糖收率很低。Stå hlberg T等[22]发现, 在咪唑离子液体中葡萄糖与硼酸质量比1∶ 1形成的葡萄糖硼酸配合物最有利于葡萄糖异构化成果糖, 同时硼酸会进一步催化果糖脱水生成5-羟甲基糠醛, 产率达42%。虽然效果不如金属氯化物, 但为葡萄糖的有效转化及利用开辟了新途径。
杨艳等[23]以极性非质子溶剂为反应介质, 葡萄糖为底物, CrCl3· 6H2O、SnCl4· 5H2O、AlCl3分别为催化剂, 具备相同阳离子及不同阴离子的一系列B酸性离子液体为助催化剂对葡萄糖异构化进行研究, 结果表明, 金属盐在葡萄糖异构化为果糖及果糖脱水为5-羟甲基糠醛两步都起作用, CrCl3既能促进葡萄糖高效异构化为果糖, 又能促进果糖选择性脱水生成5-羟甲基糠醛, 5-羟甲基糠醛产率高达66.5%; SnCl4也能很好地促进葡萄糖异构化, 但使果糖生成了更多的副产物, 5-羟甲基糠醛产率只有43.9%; AlCl3的异构化能力相对较弱, 对果糖脱水至5-羟甲基糠醛的作用与SnCl4相近, 可使5-羟甲基糠醛产率达到39%。并认为葡萄糖有效异构化为果糖离不开金属氯化物, 溶剂对金属的活性影响不容忽视; 合适的离子液体一方面可促进果糖高效转化为5-羟甲基糠醛; 另一方面与金属相互作用, 促进葡萄糖异构化。
与均相催化剂相比, 非均相催化剂由于催化剂和产物处于不同相中, 产物便于回收。离子交换型树脂、分子筛、水滑石、金属氧化物和沸石分子筛等都可用于葡萄糖的异构化反应, 并表现出较高的活性和选择性。
李常增[24]采用同晶取代法制备Sn-Beta分子筛, 用于催化葡萄糖异构化为果糖, 考察了几种含Sn材料在葡萄糖异构化反应中的性能, 结果发现, Sn-Beta分子筛对葡萄糖异构化反应有较高的反应活性。以水热法合成的Sn-Beta分子筛为催化剂, 葡萄糖转化率和果糖收率分别达到56%和45%。
Delidovich I等[25]采用Mg-Al水滑石催化葡萄糖异构化为果糖, 研究表明, 果糖收率30%, 葡萄糖选择性为89%。 Yang Qiang等[26]发现, 以MPR、有机碱、Na2CO3和DMF合成非均相碱催化剂, 再以磁性氧化铁纳米颗粒合成磁性碱催化剂, 在(80~120) ℃均可有效催化葡萄糖异构化为果糖, 收率15%~31%。
文献[26, 27, 28]在无机碱和氟化物混合体系条件下, 以四乙基氢氧化铵为模板剂, 白炭黑为硅源, B-Beta沸石为晶种, 150 ℃静态晶化成功合成出B-Beta分子筛, 发现Sn-Beta分子筛在反应温度120 ℃和反应时间2 h条件下表现出很高的催化活性, 葡萄糖转化率最高达68.6%, 果糖收率46.2%, 且催化剂重复利用性较好。
由于Beta分子筛具有独特的三维孔道结构以及较大的孔径, 在TS-1这类微孔分子筛上无法发生反应或者反应活性很低的催化反应, 特别是在具有环状或含有支链的催化反应中表现出比TS-1分子筛具有更高催化活性和选择性。Corma A等[29]用Ti-Beta分子筛作为催化剂, 叔丁基过氧化氢为氧化剂, 通过对烯烃的环氧化研究发现, 反应产物和选择性均可达100%, 表现出良好的催化性能。
Taarning E等[30] 以Sn-Beta分子筛作为催化剂对丙糖进行异构化, 结果表明, 以Sn-Beta分子筛作为L酸催化剂, 表现出很高的催化活性和选择性。Moliner M等[31]研究了以Sn-Beta分子筛为催化剂, 水为介质的条件下催化葡萄糖异构反应, 结果表明, 在葡萄糖用量为10%和Sn-Beta分子筛与葡萄糖物质的量比1∶ 50条件下, 果糖收率可达31%, 催化剂具很高的催化活性和较高的果糖选择性, 而且Sn-Beta分子筛可多次重复, 重复利用3次时, 果糖收率仍可达29%。
Stå hlberg T等[32]以离子液体为溶剂, 研究了镧系催化剂催化葡萄糖转化果糖的反应, 结果表明, 在氯化镱或三氟甲磺酸酯与三氟甲磺酸酯共同存在的条件下, 可提高转化效率, 认为在镧系催化剂存在条件下更有利于反应的进行。
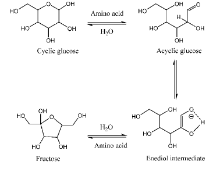
Yang Q等[33]通过对精氨酸、组氨酸和赖氨酸3种碱性氨基酸催化葡萄糖异构为果糖的研究发现, 这3种碱性氨基酸均可催化葡萄糖异构化, 其中, 精氨酸的催化效果最好, 在1 mL水中、葡萄糖质量分数为10%、精氨酸用量为葡萄糖物质的量的10%和温度120 ℃反应15 min条件下, 葡萄糖转化率可达76%, 果糖收率最高达31%。通过对精氨酸催化葡萄糖异构的机理研究认为, 葡萄糖在精氨酸催化下, 葡萄糖异构化首先从非环化的葡萄糖开始, 在异构化过程中, 环化的葡萄糖首先通过C1→ O5醚键的断裂形成非环化结构, 非环化结构的葡萄糖由于热力学结构不稳定, 除了去质子化形成烯醇式中间体, 也可以自发异构化成环化的葡萄糖(见图1), 故认为碱性氨基酸也可作为一种绿色催化剂用于葡萄糖的异构化反应。
近年来, 微波作为一种新型的物理加工方式, 具有无化学残留和安全性高等优点, 微波辅助酶催化反应能增强酶的活性和稳定性[34, 35]。
胡国洲[36]研究了微波处理对葡萄糖异构酶的影响, 结果表明, 处理温度70 ℃, 处理时间5 min, 微波功率为300 W和400 W时, 葡萄糖异构酶的相对酶活分别增加了14.23%和8.42%, 并且高温微波辐射加热对固定化葡萄糖异构酶的稳定性具有显著影响。
Zhao H等[37]发现以离子液体为溶剂, CrCl2可以有效催化葡萄糖制备5-羟甲基糠醛, 同时推测了葡萄糖异构化机理, 提出Cr2+与离子液体的阴、阳离子分别配位, 然后与葡萄糖上两个相邻的羟基结合, 促进葡萄糖开环并异构化形成果糖, 果糖再脱水生成5-羟甲基糠醛, 推测离子液体中金属氯化物催化葡萄糖异构化时就将离子液体与金属中心连接在一起。
Saravanamurugan S等[38]研究了离子液体中金属氯化物的配位性质及催化葡萄糖异构化的机理, 指出异构化过程主要经历以下步骤:金属中心首先与葡萄糖的 O1、O2 结合, 同时 Cl-与O1上H形成氢键促使 O1 去质子化; 然后 O5 被质子化, C1— O5键断开, 吡喃环被打开, 同时Cl与O2上的H形成氢键使H脱离O, 然后C2上的H转移至C1, 最后闭环形成果糖。推测离子液体与金属氯化物间存在着某种相互作用, 从而增强或削弱金属的异构化能力, 尤其是离子液体的阴离子可能起更重要的作用。Stå hlberg T等[39]首次报道了葡萄糖异构酶在DBAO离子液体中可有效异构葡萄糖产生果糖, 果糖收率达54%以上。
无论是利用葡萄糖为原料生产高附加值平台化合物, 还是通过对葡萄糖异构化进行高值化生产利用, 开展葡萄糖异构化为果糖的研究十分必要, 建议进一步开展以下研究工作:
(1) 在酶催化异构化方面, 在现有的研究基础上, 应将将酶的结构变化和酶学性质变化进行定向和定量研究;
(2) 应加大环境友好、高选择性、高催化活性和易循环利用的固体酸催化剂研制以及相关催化机理的研究, 从而提高葡萄糖的转化效率和果糖选择性, 降低生产成本, 提高产品附加值;
(3) 开展催化产物的分离纯化技术研究, 如吸附法和膜分离法等;
(4) 深入研究葡萄糖异构化反应机理和动力学模型, 有效指导葡萄糖异构催化剂体系设计和反应条件选取, 是实现葡萄糖异构化制备果糖和其他平台化合物工业化应用的必要环节。
The authors have declared that no competing interests exist.
作者已声明无竞争性利益关系。The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|